Abstrak
Memahami mekanisme yang mendorong struktur dan dinamika komunitas sangat penting dalam menghadapi meningkatnya perubahan iklim, termasuk meningkatnya kejadian cuaca ekstrem. Ukuran sel merupakan sifat utama organisme kecil yang tunduk pada trade-off antara ketahanan terhadap penggembalaan dan persaingan untuk mendapatkan sumber daya, dan dengan demikian berpotensi untuk menjelaskan dan memprediksi dinamika komunitas dalam menanggapi gangguan. Di sini, kami bertujuan untuk menentukan apakah ukuran sel dapat menjelaskan pergeseran dalam komunitas fitoplankton setelah perubahan kondisi nutrisi dan cahaya yang diakibatkan oleh masukan nutrisi dan bahan organik terlarut berwarna (cDOM) yang disebabkan oleh badai ke danau air jernih yang dalam. Untuk memastikan kondisi lingkungan yang realistis, kami menggunakan desain gradien silang untuk melakukan eksperimen kandang skala besar selama 6 minggu. Ukuran sel menjelaskan struktur komunitas fitoplankton ketika ketersediaan cahaya menurun sebagai akibat dari pasokan cDOM. Awalnya unimodal, dengan spesies bersel kecil yang mencakup hingga 60% dari total biovolume komunitas, distribusi ukuran sel secara bertahap bergeser ke arah spesies bersel besar karena tingkat cahaya menurun setelah penambahan cDOM. Baik nutrisi maupun mesozooplankton tidak memengaruhi pergeseran dalam distribusi ukuran sel. Hasil ini menunjukkan keunggulan kompetitif yang jelas dari spesies yang lebih besar dibandingkan spesies yang lebih kecil pada tingkat cahaya yang berkurang setelah masukan cDOM selama peristiwa badai. Yang penting, pengelompokan spesies dalam dua kelas ukuran yang berbeda menyiratkan bahwa perbedaan ukuran antarspesies sama pentingnya dengan ukuran sel itu sendiri untuk memahami dinamika komunitas. Mengingat bahwa pergeseran dalam distribusi ukuran sel memiliki implikasi yang kuat untuk struktur jaring makanan dan siklus biogeokimia, hasil kami menunjukkan pentingnya menganalisis distribusi ukuran sel organisme kecil sebagai elemen penting untuk memperkirakan dinamika komunitas dan ekosistem dalam menanggapi perubahan lingkungan.
PERKENALAN
Sejak perumusan prinsip pengecualian kompetitif oleh Gause ( 1934 ), para ahli ekologi telah dibuat bingung oleh keanekaragaman spesies yang sangat besar di Bumi. Hal ini menyebabkan Hutchinson ( 1961 ) mengartikulasikan “paradoks plankton” yang terkenal yang berkaitan dengan perbedaan mencolok antara kekayaan spesies komunitas dan jumlah sumber daya yang tampaknya terbatas yang diperebutkan oleh spesies. Awalnya difokuskan pada plankton, paradoks Hutchinson telah diperluas ke keanekaragaman organisme mulai dari bakteri hingga burung (May, 1988 ; Mora et al., 2011 ; Ptacnik et al., 2010 ). Meskipun banyak sekali karya teoritis dan empiris yang menggunakan berbagai komunitas untuk menyelesaikan teka-teki ini, para ahli ekologi tetap tertantang dalam upaya untuk mengungkap pendorong struktur komunitas (misalnya, Chesson, 2000 ; Hubbell, 2001 ; MacArthur & Levins, 1967 ; Scheffer et al., 2018 ), yang terus memicu minat mendasar dalam memahami dinamika dan mekanisme yang mendasarinya. Selain itu, telah menjadi sangat mendesak untuk menentukan hubungan ini mengingat krisis keanekaragaman hayati dan iklim global saat ini. Ini termasuk respons terhadap peristiwa cuaca ekstrem, yang meningkat dalam besaran dan frekuensi dan dapat memiliki konsekuensi yang luas bagi keanekaragaman hayati dan fungsi ekosistem (IPCC, 2023 ).
Jenis peristiwa cuaca yang memungkinkan manipulasi eksperimental untuk menilai peran peristiwa ekstrem dalam menentukan struktur komunitas adalah badai hebat yang memengaruhi danau (Stockwell et al., 2020 ). Selain dampak fisik (Jennings et al., 2012 ; Kasprzak et al., 2017 ), badai sering kali disertai oleh hujan lebat dan limpasan daratan yang membawa nutrisi dan bahan organik terlarut berwarna (cDOM), sehingga mengubah pasokan sumber daya di ekosistem penerima (Cooney et al., 2018 ; Drakare et al., 2002 ; Solomon et al., 2015 ). Dengan menyerap cahaya dengan kuat, terutama dalam rentang spektrum biru, cDOM dengan cepat melemahkan radiasi aktif fotosintesis (PAR) (Kirk, 1994 ; Thrane et al., 2014 ). Peningkatan konsentrasi cDOM dengan demikian tidak hanya membatasi fotosintesis dan produksi primer (Kritzberg et al., 2014 ; Thrane et al., 2014 ), tetapi juga mengubah interaksi kompetitif antar spesies yang jika tidak demikian hidup berdampingan melalui partisi relung sepanjang spektrum PAR (Burson et al., 2019 ; Luimstra et al., 2020 ; Stomp et al., 2004 ).
Pengayaan nutrisi setelah peristiwa badai juga dapat mengubah pola dominasi spesies dan meningkatkan biomassa, menggeser pendorong struktur komunitas dari nutrisi ke kompetisi cahaya (Brauer et al., 2012 ; Hautier et al., 2009 ). Selain itu, limpasan yang disebabkan badai dapat mengubah dinamika produsen dan konsumen dengan cara yang kontras (Solomon et al., 2015 ). Di satu sisi, redaman cahaya oleh cDOM yang dipasok ke danau dapat mengurangi ketersediaan makanan untuk herbivora dan, dengan membatasi kelimpahan hewan penggembala, melepaskan tekanan makan pada produsen primer (Kelly et al., 2014 ). Di sisi lain, rasio pasokan cahaya terhadap nutrisi yang lebih rendah mengakibatkan rasio karbon terhadap fosfor yang lebih rendah dari produsen (Sterner et al., 1997 ) dan berkurangnya radiasi UV dapat bermanfaat bagi herbivora dengan meningkatkan kualitas makanan (Minguez et al., 2020 ) atau mengurangi kerusakan sel (Wolf & Heuschele, 2018 ).
Banyak upaya telah diinvestasikan dalam pendekatan berbasis sifat untuk mendapatkan wawasan tentang struktur komunitas dan respons terhadap perubahan global (McGill et al., 2006 ; Westoby & Wright, 2006 ), termasuk untuk fitoplankton di danau dan lautan (Litchman, 2022 ; Litchman & Klausmeier, 2008 ). Sifat menangkap fungsi biologis fundamental (Litchman & Klausmeier, 2008 ) dan dengan demikian sering berperan penting bagi dinamika komunitas yang didorong oleh persaingan sumber daya (Edwards et al., 2013a , 2013b ; Schwaderer et al., 2011 ). Menilai dampak limpasan yang disebabkan badai pada struktur dan dinamika komunitas memerlukan pertimbangan tidak hanya perubahan dalam hubungan kompetitif tetapi juga dalam interaksi trofik. Ukuran sel telah diidentifikasi sebagai sifat utama yang mengatur perolehan sumber daya, pertumbuhan, reproduksi, dan interaksi trofik (Berger et al., 2014 ; Hillebrand et al., 2022 ; Litchman & Klausmeier, 2008 ; Marañón, 2015 ). Secara khusus, ukuran sel sering kali tunduk pada trade-off antara kemampuan kompetitif untuk memperoleh sumber daya dan resistensi terhadap penggembalaan. Spesies bersel kecil diperkirakan lebih disukai ketika ketersediaan cahaya dan nutrisi rendah karena mereka sering kali memiliki konstanta setengah-saturasi yang lebih rendah untuk penyerapan nutrisi (Edwards et al., 2012 ) dan kemiringan awal yang lebih curam dari kurva fotosintesis-irradiansi (Schwaderer et al., 2011 ) daripada spesies yang lebih besar. Sebaliknya, ketika sumber daya melimpah, spesies yang lebih besar bisa jadi relatif lebih melimpah dalam komunitas jika ukuran memberikan perlindungan yang cukup dari kematian akibat penggembalaan dibandingkan dengan sel yang lebih kecil (Pančić & Kiørboe, 2018 ). Namun, ekspektasi ini berbeda dengan beberapa pengamatan in situ (lihat Marañón, 2015 untuk tinjauan). Misalnya, mortalitas penggembalaan bahkan untuk sel besar dapat menjadi penting (misalnya, Chang et al., 2013 ). Lebih jauh, penskalaan ukuran laju pertumbuhan telah disarankan untuk mendukung dominasi ukuran sel menengah selama mekarnya fitoplankton, yang menghasilkan distribusi ukuran sel unimodal (Marañón, 2015 ; Marañón et al., 2013 ).
Dalam penelitian ini, kami menanyakan apakah ukuran sel dapat menjelaskan pergeseran dalam struktur komunitas fitoplankton setelah badai hebat yang membentuk kembali kondisi lingkungan. Tujuan pertama kami adalah untuk menentukan bagaimana kekayaan spesies merespons masukan nutrisi dan cDOM secara bersamaan, dengan harapan bahwa efek nutrisi diredam oleh redaman cahaya yang dimediasi oleh cDOM. Secara khusus, kami menguji apakah jumlah spesies menurun saat pasokan nutrisi dan cDOM yang disebabkan badai dari daerah tangkapan meningkat. Tujuan kedua adalah untuk menentukan apakah pergeseran yang jelas dalam ukuran sel merupakan pola yang mendasari perubahan dalam struktur dan dinamika komunitas setelah peristiwa badai. Secara khusus, kami menguji apakah spesies bersel kecil mendominasi spesies bersel besar saat keterbatasan cahaya yang disebabkan oleh cDOM meningkat dan apakah spesies bersel besar mendominasi spesies bersel kecil pada ketersediaan nutrisi dan PAR yang tinggi. Untuk mengatasi tujuan ini, kami melakukan eksperimen penutup danau dengan komunitas plankton alami, di mana kami meniru berbagai tingkat pasokan cDOM dan nutrisi, yang mencerminkan masukan ke danau oleh limpasan terestrial selama peristiwa badai. Kami berhipotesis bahwa (1) jumlah spesies fitoplankton akan menurun seiring dengan meningkatnya pasokan cDOM dan ketersediaan nutrisi karena keterbatasan cahaya pada fotosintesis dan terbatasnya penyerapan nutrisi yang bergantung pada cahaya; (2) distribusi ukuran spesies dalam kondisi cahaya rendah dan ketersediaan nutrisi tinggi akan bergeser ke arah sel-sel kecil, yang cenderung memiliki kebutuhan cahaya minimum yang lebih rendah daripada sel-sel yang lebih besar; dan (3), sebaliknya, sel-sel besar akan meningkat kelimpahannya pada tingkat cahaya dan nutrisi yang tinggi karena akses yang cukup ke kedua sumber daya dan tingkat kematian penggembalaan yang lebih rendah daripada yang dialami oleh sel-sel kecil.
METODE
Pengaturan percobaan
Percobaan ini dilakukan di fasilitas kandang besar yang terletak di Danau Stechlin, sebuah danau air jernih dalam di timur laut Jerman (53°08′36′′ LU, 13°01′41′′ BT). Fasilitas ini terdiri dari 24 kandang, masing-masing berdiameter 9 m dan kedalaman sekitar 20 m, sehingga menutup hampir 1300 m 3 air (Lyche Solheim et al., 2024 ). Sebelum percobaan dimulai, semua ikan yang terperangkap di kandang dikeluarkan dengan jaring insang (ukuran mata jaring 6,5 mm) dan air di kandang ditukar dengan air epilimnetik dan hipolimnetik dari danau di sekitarnya untuk memastikan kondisi awal yang sama di antara semua unit percobaan. Air yang dipompa ke dalam kandang dialirkan melalui mata jaring 3 mm untuk mencegah masuknya kembali ikan, termasuk larva.
Kami membuat gradien eksperimental tujuh tingkat nutrisi pada masing-masing tiga tingkat pencoklatan (tidak ada, sedang, tinggi) dengan menambahkan satu denyut nutrisi dan cDOM ke total 21 kandang. Pencoklatan dicapai dengan menambahkan zat humat yang diproses secara industri yang dipasarkan sebagai HuminFeed (HF, HuminTech GmbH, Grevenbroich, Jerman; Scharnweber et al., 2021 ). HF dicirikan oleh kelarutan yang tinggi dalam air, absorbansi PAR yang efisien, ketahanan karbon, dan konsentrasi nutrisi yang rendah. Kami memperoleh tiga tingkat pencoklatan dengan menambahkan 0 (tanpa penambahan HF), 5, dan 10 mg HF L −1 ke kandang, masing-masing disebut sebagai A, B, dan C. Konsentrasi karbon organik terlarut (DOC) rata-rata (±SD) di seluruh percobaan sedikit lebih tinggi di kandang B (5,7 ± 0,5 mg L −1 ) dan C (6,1 ± 0,6 mg L −1 ) daripada di kandang A (5,3 ± 0,5 mg L −1 ). H 3 PO 4 ditambahkan untuk meningkatkan konsentrasi P awal sebesar 18 μg L −1 sebesar 0, 1, 4, 9, 16, 25, dan 36 μg P L −1 , berturut-turut. Nitrogen ditambahkan sebagai NH 4 NO 3 dalam jumlah yang menghormati rasio molar N:P bioavailable danau, yang mendekati rasio Redfield sebesar 16:1. Pulsa nutrisi dan pencoklatan diselesaikan antara 8 dan 10 Juni 2015.
Variabel abiotik dan biotik
21 enklosur yang digunakan dalam percobaan dilengkapi dengan sensor suhu (YSI Inc., Yellow Springs, OH, AS) dan PAR (LI-COR Inc., Lincoln, NE, AS) yang dipasang pada profiler yang merekam profil vertikal per jam pada langkah kedalaman 0,5 m (Giling et al., 2017 ). Koefisien redaman cahaya diperkirakan sebagai kemiringan regresi linier antara ln(PAR) dan kedalaman. Sampel air yang terintegrasi dengan kedalaman dari epilimnion (6–7 m) dikumpulkan dengan pengambil sampel selang seminggu sekali dari 5 Juni hingga 21 Juli 2015. Konsentrasi fosfor total (TP), fosfor reaktif terlarut (SRP), nitrogen total (TN), amonium, nitrit, dan nitrat ditentukan dengan analisis injeksi aliran mengikuti prosedur ISO (FIAStar 5000, FOSS, Höganäs, Swedia).
Kami menguji hubungan antara rata-rata PAR epilimnion pada siang hari dan SRP di semua kandang dan sepanjang percobaan dengan menentukan hubungan log-log antara SRP dan PAR menggunakan model efek campuran linier (LME) yang memperhitungkan ketergantungan kandang terhadap pengukuran. Kami juga menggunakan model LME untuk mengukur peningkatan linier suhu epilimnion dari waktu ke waktu untuk memperhitungkan pengukuran berulang kami. Kami menentukan efek pencoklatan pada hubungan ini dengan membandingkan kemiringan garis regresi dengan analisis kovariansi dengan metode Kenward-Rogers. Semua model LME dihitung menggunakan paket R lme4 (Bates et al., 2015 ).
Kami menganalisis komposisi spesies fitoplankton dan biovolume dari sampel air epilimnetik (250 mL) yang diambil setiap minggu dari 5 Juni hingga 21 Juli dan difiksasi dengan larutan Lugol yang bersifat asam. Spesies diidentifikasi dan dihitung di bawah mikroskop terbalik (Nikon Diaphot, Tokyo, Jepang, dan Leica DMI3000 B, Wetzlar, Jerman). Volume sel spesifik spesies (disebut sebagai ukuran sel di bawah) diperkirakan dari perkiraan bentuk geometris (Komite Eropa untuk Standardisasi, 2015 ). Biovolume spesifik spesies kemudian ditentukan sebagai produk dari volume sel spesifik spesies dan kelimpahan sel. Mesozooplankton diambil sampelnya dengan tarikan jaring vertikal (ukuran mata jaring 90-μm) dari 1,5 m di atas sedimen ke permukaan air dan diawetkan dalam larutan gula-formalin (konsentrasi akhir masing-masing 50% dan 4%). Biomassa spesies mesozooplankton ditentukan dengan mengidentifikasi, menghitung, dan mengukur spesimen di bawah mikroskop terbalik. Biomassa dihitung berdasarkan pengukuran panjang 10–30 spesimen per takson dan hubungan panjang-massa kering yang ditetapkan untuk Danau Stechlin dan populasi lainnya (Bottrell et al., 1976 ; Kasprzak, 1983 ). Karbon biomassa diasumsikan sebesar 50% dari massa kering (Winberg, 1971 ).
Efek pencoklatan (di tujuh tingkat pasokan P) dan pengayaan P (di tiga tingkat pencoklatan) pada biomassa mesozooplankton yang ditransformasikan secara logaritma ditentukan dalam dua model LME terpisah yang memperhitungkan pengukuran berulang. Setiap tingkat pencoklatan atau pengayaan nutrisi dibandingkan dengan intersep model, yang mencerminkan kondisi referensi tanpa penambahan HF atau P. Kami mengadopsi pendekatan yang sama untuk total biovolume fitoplankton yang ditransformasikan secara logaritma.
Distribusi ukuran sel
Kami menguji untuk setiap kandang apakah distribusi ukuran sel fitoplankton menyimpang secara signifikan dari distribusi unimodal. Pada awal dan akhir percobaan, kami menyelidiki distribusi ukuran biovolume spesies menggunakan model aditif umum (GAM) (Wood, 2017 ). Kami menentukan untuk setiap kandang biovolume relatif spesies yang dikategorikan berdasarkan interval ukuran 1 log 2 μm 3 pada rentang 1–15 log 2 μm 3. Kami menormalkan biovolume relatif spesies dalam setiap kandang (yaitu, proporsi biovolume total), yang berkisar dari 1,1 × 10 −5 hingga 0,76, dengan menerapkan transformasi logit. Karena biovolume ditemukan bervariasi secara signifikan di seluruh gradien cahaya tetapi tidak nutrisi, kami memasang satu GAM per tingkat pencoklatan di awal dan akhir percobaan, menggunakan biovolume relatif spesies di seluruh tujuh kandang terlepas dari tingkat pengayaan P. Tingkat P ditetapkan sebagai efek acak untuk memperhitungkan setiap variasi yang bergantung pada nutrisi dalam distribusi ukuran sel. Semua plot diagnostik GAM (fungsi yang dinilai dalam paket R gratia ; Simpson, 2023 ) menunjukkan kesesuaian yang memuaskan dengan distribusi normal dari sisa deviasi, homogenitas sisa deviasi sepanjang prediktor linier, dan linearitas nilai yang diamati versus yang disesuaikan.
Untuk menguji jumlah mode di sepanjang gradien ukuran sel, kami menghitung turunan orde pertama GAM. Puncak yang signifikan dalam model GAM menghasilkan turunan positif yang signifikan di sepanjang bagian puncak yang menaik, diikuti oleh turunan negatif di sepanjang bagian yang menurun. Karena penyertaan efek acak untuk nutrisi tidak pernah memperbaiki GAM menurut kriteria informasi Akaike (AIC), kami merata-ratakan tujuh turunan per tingkat pencoklatan dan menghitung amplop kepercayaan GAM 95%. Semua analisis GAM dilakukan dengan paket mgcv di R (Wood, 2017 ).
Kekayaan spesies
Kami mengeksplorasi variasi dalam jumlah spesies fitoplankton sebagai respons terhadap PAR, SRP, dan biomassa mesozooplankton menggunakan model LME. Meskipun ada korelasi negatif yang signifikan antara PAR dan SRP, kami memasukkan interaksi antara PAR dan SRP dalam model. Waktu yang berlalu dimasukkan sebagai prediktor tetap karena jumlah spesies secara bertahap menurun selama percobaan. Semua prediktor distandarisasi dengan memusatkannya di sekitar nilai rata-rata dan membaginya dengan SD ( skor- z ). Model tersebut menyertakan intersepsi acak untuk penutup untuk memperhitungkan pengukuran berulang. Untuk menguji apakah waktu yang berlalu memiliki efek yang signifikan, kami menghitung uji rasio kemungkinan (likelihood ratio test/LRT) yang membandingkan hasil model yang menyertakan atau mengecualikan waktu yang berlalu sebagai variabel. Kami juga menguji efek biomassa mesozooplankton menggunakan metode yang sama.
Bahasa Indonesia: Untuk menilai variasi dalam distribusi ukuran fitoplankton, kami mengeksplorasi dalam model ada-tidaknya (PA) apakah ukuran sel spesies memiliki efek pada probabilitas bahwa spesies tertentu muncul pada setiap saat selama percobaan dan sepanjang gradien biomassa PAR, SRP, dan mesozooplankton. Secara khusus, kami menguji apakah pada tingkat cahaya dan nutrisi yang lebih rendah, probabilitas kemunculan spesies lebih tinggi untuk spesies bersel kecil daripada spesies yang lebih besar dan apakah kemunculan spesies bersel besar dikaitkan dengan tekanan penggembalaan yang lebih tinggi pada spesies bersel kecil. Spesies dipisahkan menjadi dua rentang ukuran untuk analisis ini, satu terdiri dari spesies bersel kecil (0–8 log 2 μm 3 ) dan satu terdiri dari spesies dengan ukuran sel sedang (8–15 log 2 μm 3 ).
Kami membangun model campuran linier tergeneralisasi (GLMM) menggunakan paket R lme4 (Bates et al., 2015 ). Kami menyertakan intersepsi acak untuk identitas spesies guna menangkap variasi dalam kemunculan spesies. Karena PA spesies dapat dijelaskan dengan distribusi binomial dengan nilai 0 (tidak ada) dan 1 (ada), model PA adalah
Seperti pada model PA, kami menggunakan LRT untuk menguji apakah respons fitoplankton terhadap tiga prediktor (PAR, SRP, zooplankton) bersifat khusus spesies dengan membandingkan hasil model biovolume dengan model alternatif terkait yang tidak menyertakan kemiringan acak. Kami kemudian menguji apakah ukuran sel memiliki efek pada biovolume relatif spesies di sepanjang prediktor dengan menghitung LRT yang membandingkan model biovolume dan model alternatif terkait yang tidak menyertakan interaksi antara ukuran sel dan masing-masing prediktor. Semua hasil LRT didukung oleh uji bootstrap parametrik dengan 999 simulasi.
Semua analisis dilakukan menggunakan R versi 4.2.2 (Tim Inti R, 2022 ).
HASIL
Kondisi lingkungan
Penambahan cDOM dalam bentuk HF meningkatkan redaman cahaya di dalam enklosur yang menerima cDOM (B dan C) dibandingkan dengan enklosur A yang bening (Gambar 1a–c ). Akibatnya, penurunan eksponensial PAR terhadap kedalaman dipertegas, sehingga mengurangi rata-rata kadar PAR di epilimnion (Gambar 1d–f ). Namun, seiring berjalannya waktu, redaman cahaya menurun di dalam enklosur yang menerima cDOM (B dan C), entah karena pemutihan foto cDOM atau mekanisme lain seperti flokulasi (Fonvielle et al., 2021 ). Rata-rata kadar PAR dan SRP di epilimnion berkorelasi negatif (Gambar 1d–i ), konsisten dengan hipotesis kami (H1) bahwa keterbatasan cahaya setelah penambahan cDOM mengurangi penyerapan nutrisi.
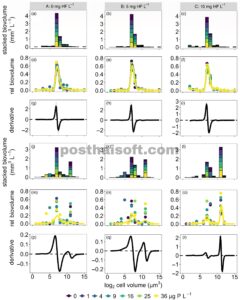
GAMBAR 1
Dinamika temporal koefisien atenuasi cahaya (a–c) dan radiasi aktif fotosintesis rata-rata (PAR) pada siang hari (d–f), fosfor reaktif terlarut (SRP) (g–i), nitrogen anorganik terlarut (DIN) (j–l), dan biomassa mesozooplankton (m–o) dalam kandang yang tidak menerima (A: 0 mg HF L −1 ; kolom kiri: a, d, g, j, m), menengah (B: 5 mg HF L −1 ; kolom tengah: b, e, h, k, n), atau tinggi (C: 10 mg HF L −1 ; kolom kanan: c, f, i, l, o) tingkat bahan organik terlarut berwarna dalam bentuk HuminFeed (HF). Pengayaan P eksperimental (penambahan 0, 1, 4, 9, 16, 25, dan 36 μg P L −1 ) direpresentasikan oleh gradien warna dari biru tua ke kuning.
Hubungan log–log antara PAR dan SRP mengindikasikan bahwa SRP menurun secara signifikan dengan peningkatan PAR (LME, slope ± SE (95% CI) = −0,26 ± 0,07 (−0,39; −0,13), p < 0,001). Suhu meningkat secara signifikan seiring waktu di semua kandang (LME, p < 0,001; Lampiran S1 : Gambar S1 ) dari 15,6 ± 0,1°C pada tanggal 5 Juni hingga 20,6 ± 0,1°C pada tanggal 21 Juli (rata-rata ± SD di semua kandang). Peningkatan ini tidak berbeda secara signifikan di antara jenis kandang ( p > 0,90; Lampiran S1 : Tabel S1 dan S2 ).
Biomassa Plankton
Biomassa mesozooplankton meningkat dengan cepat setelah permulaan percobaan (Gambar 1m–o ) tetapi secara signifikan lebih sedikit di dalam kandang B (LME, p < 0,001) dan C (LME, p < 0,001) dibandingkan di dalam kandang A (Lampiran S1 : Gambar S2a ). Biovolume fitoplankton menurun di dalam kandang yang menerima cDOM, di mana ketersediaan cahaya berkurang (LME, p < 0,001; Lampiran S1 : Gambar S3a,b ). Pengayaan nutrisi tidak berpengaruh pada biomassa zooplankton (LME, semua p > 0,50; Lampiran S1 : Gambar S2b ) atau biovolume fitoplankton (LME, semua p > 0,40; Lampiran S1 : Gambar S3c ). Dinamika di salah satu kandang bening (A4) sangat berbeda karena biomassa zooplankton jauh lebih rendah dibandingkan di kandang bening lainnya. Hal ini disebabkan oleh dominasi copepoda calanoid predator besar ( Heterocope appendiculata ) yang mengurangi kelimpahan spesies zooplankton herbivora dan dengan demikian mengurangi biomassa mesozooplankton secara keseluruhan.
Distribusi ukuran fitoplankton
Distribusi frekuensi spesies fitoplankton mencakup rentang ukuran yang luas (Lampiran S2 : Gambar S1 ), dari picoplankton (misalnya, Cyanodictyon spp., ~1 μm 3 ) hingga Dinophyceae terbesar ( Ceratium hirundinella , ~50.000 μm 3 ). Dalam hal biovolume, distribusi spesies sepanjang gradien ukuran sel kurang merata (Lampiran S2 : Gambar S2 ), karena total biovolume sebagian besar terdiri dari spesies dengan ukuran sel yang sama, menghasilkan distribusi berkelompok dengan puncak dan palung biovolume (Gambar 2 ). Sebelum badai yang disimulasikan, distribusi ukuran selalu unimodal (rata-rata 7,7 log 2 μm 3 atau 211 μm 3 ) dan didominasi oleh spesies bersel kecil (Gambar 2a–i ). Spesies dalam kategori ukuran 7 log 2 μm 3 (6–7 log 2 μm 3 sama dengan 64–128 μm 3 ) mendominasi komunitas, berkontribusi sekitar 60% terhadap total biovolume fitoplankton di semua kandang (Gambar 2d–f ). Varians yang dijelaskan oleh GAM pada awal percobaan adalah 83%, 92%, dan 95% di kandang A, B, dan C, masing-masing (Gambar 2d–f , Lampiran S2 : Tabel S1 ). Ukuran sel menjelaskan variasi signifikan dalam biovolume spesies di ketiga GAM (semua p < 0,001). Tidak ada efek pengayaan nutrisi yang dicatat (semua p > 0,10). Pola unimodal didukung secara statistik oleh turunan orde pertama GAM, yang secara signifikan positif (bagian puncak yang menaik) dan negatif (bagian puncak yang menurun), seperti yang ditunjukkan oleh rata-rata turunan di seluruh tingkat nutrisi (Gambar 2g–i , Lampiran S2 : Tabel S1 ).
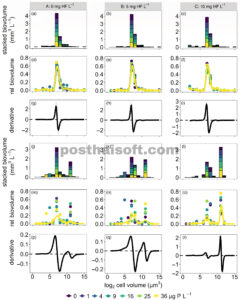
GAMBAR 2
Distribusi ukuran sel dari biovolume relatif spesies fitoplankton dalam kandang yang tidak menerima (A: 0 mg HF L −1 ; kolom kiri: a, d, g, j, m, p), menengah (B: 5 mg HF L −1 ; kolom tengah: b, e, h, k, n, q), atau tinggi (C: 10 mg HF L −1 ; kolom kanan: c, f, i, l, o, r) tingkat bahan organik terlarut berwarna sebelum simulasi peristiwa badai pada tanggal 5 Juni (a–i) dan pada akhir percobaan 6 minggu kemudian pada tanggal 21 Juli (j–r); jumlah biovolume relatif selama tujuh tingkat pengayaan nutrisi (penambahan 0, 1, 4, 9, 16, 25, dan 36 μg P L −1 ) per tingkat pencoklatan (a–c, j–l); model aditif umum untuk setiap tingkat pencoklatan pada biovolume relatif spesies yang ditransformasikan secara logit dalam masing-masing dari tujuh tingkat pengayaan P (d–f, m–o); rata-rata dan, dalam warna abu-abu, 95% CI (hampir tidak terlihat) dari turunan orde pertama di seluruh tingkat nutrisi (g–i, p–r).
Setelah penambahan cDOM dan nutrisi, pola bergeser dari unimodal ke bimodal karena biovolume relatif spesies yang lebih besar meningkat dan spesies bersel lebih kecil menurun secara bersamaan (Gambar 2j–r ). Varians yang dijelaskan oleh GAM pada akhir percobaan adalah 51%, 55%, dan 72% di kandang A, B, dan C, masing-masing (Gambar 2m–o , Lampiran S2 : Tabel S1 ). Seperti yang diamati pada awal percobaan, ukuran sel menjelaskan variasi signifikan dalam biovolume spesies di ketiga GAM (semua p < 0,001), sedangkan efek pengayaan nutrisi tidak tampak (semua p > 0,40). Pada akhir percobaan, distribusi ukuran bersifat bimodal di hampir semua enklosur (Gambar 2m–r , Lampiran S2 : Gambar S2 ), dengan komunitas didominasi oleh spesies dalam kategori ukuran 7 dan 11 log 2 μm 3 (masing-masing 64–128 μm 3 dan 1024–2048 μm 3 ). Namun, biovolume relatif rata-rata (±SD) spesies dalam kategori ukuran 11 log 2 μm 3 di enklosur C (47 ± 20%) melebihi enklosur B (28 ± 14%) dan A (24 ± 18%). Pola bimodal didukung secara statistik oleh turunan orde pertama GAM (Gambar 2p–r ), yang masing-masing secara signifikan positif (bagian puncak yang menaik) dan negatif (bagian puncak yang menurun).
Kekayaan spesies
Jumlah spesies fitoplankton menurun di semua kandang selama percobaan (Lampiran S3 : Gambar S1 ). Di semua kandang, rata-rata 39 ± 9% (±SD) spesies yang awalnya ada hilang antara hari pertama dan terakhir percobaan, dengan kerugian di kandang individu berkisar antara 18% dan 54%. Jumlah spesies meningkat secara signifikan dengan meningkatnya ketersediaan cahaya (LME, p < 0,001; Lampiran S3 : Gambar S2 , Tabel S1 ). Biomassa mesozooplankton tidak berhubungan secara signifikan dengan jumlah spesies fitoplankton (LRT, χ 2 = 0,96, p = 0,33). Demikian pula, tidak ada hubungan yang signifikan antara SRP dan jumlah spesies fitoplankton (LME, p = 0,79), juga interaksi antara PAR dan SRP tidak berhubungan secara signifikan dengan jumlah spesies (LME, p = 0,06; Lampiran S3 : Gambar S2 , Tabel S1 ). Menyertakan konsentrasi SRP sebagai tambahan waktu dalam model tidak menjelaskan lebih lanjut tentang variasi temporal dalam jumlah spesies di kandang A yang jelas (LRT, χ 2 < 0,1, p = 0,99; Lampiran S3 ). Oleh karena itu dan karena korelasi negatif dengan PAR, SRP tidak disertakan dalam model PA untuk meminimalkan jumlah variabel. Hal ini memungkinkan model untuk konvergen.
Pada nilai rata-rata prediktor terstandardisasi PAR, waktu berlalu, dan biomassa zooplankton (intersep, Tabel 1 , Gambar 3 ), probabilitas kemunculan spesies tidak berbeda ( p = 0,34) antara spesies besar (17% atau -1,60 pada skala logit) dan spesies kecil (20% atau -1,36 pada skala logit). Model PA mengungkapkan efek positif signifikan dari PAR ( p < 0,01, Gambar 3 , Tabel 1 ) pada probabilitas kemunculan spesies pada kedua rentang ukuran, sedangkan waktu berlalu memiliki efek negatif ( p < 0,001). Namun, rentang ukuran tampaknya memiliki efek pada kemunculan spesies di sepanjang gradien biomassa mesozooplankton (yaitu, tekanan penggembalaan). Interaksi antara rentang ukuran dan biomassa zooplankton signifikan ( p < 0,01), yang menunjukkan bahwa kemunculan spesies kecil menurun relatif terhadap yang lebih besar saat biomassa zooplankton meningkat. Keberadaan spesies fitoplankton besar meningkat seiring dengan meningkatnya biomassa zooplankton ( p < 0,05).
TABEL 1. Statistik model campuran linier umum ada–tidaknya (skala logit; lihat Persamaan 1 dalam Metode ), termasuk SE dan 95% CI bootstrap (999 simulasi) dari faktor-faktor tetap.

GAMBAR 3
Perkiraan probabilitas kemunculan spesies sebagai fungsi interaksi antara kisaran ukuran sel (spesies bersel kecil vs. bersel besar) dan radiasi aktif fotosintesis (PAR) (a), waktu yang berlalu (b), dan biomassa zooplankton (c) sebagai prediktor terstandarisasi.
Model biovolume
Fitoplankton merespons gradien PAR dengan cara yang spesifik terhadap spesies, seperti yang ditunjukkan oleh perbandingan kedua model biovolume termasuk kemiringan acak untuk PAR atau tidak (LRT, χ 2 = 84,1, p < 0,001). Ukuran sel memiliki efek signifikan pada biovolume relatif spesies di sepanjang gradien PAR (Gambar 4a , ukuran β ×PAR pada Tabel 2 ), seperti yang ditunjukkan oleh LRT (χ 2 = 4,3, p = 0,04) dan bootstrap parametrik (999 simulasi, p = 0,04). Dua puncak biovolume untuk spesies dominan (ukuran sel 7 log 2 μm 3 atau 128 μm 3 , dan 11 log 2 μm 3 atau 2048 μm 3 ; Gambar 2d–f,m–o ) yang ditunjukkan oleh garis kecocokan (Gambar 4a ) menggarisbawahi bahwa spesies bersel besar berkontribusi lebih banyak pada total biovolume komunitas saat PAR menurun karena pencoklatan. Sebaliknya, total biovolume klaster yang terdiri dari spesies yang lebih kecil (7 log 2 μm 3 atau 128 μm 3 ) menunjukkan sedikit respons terhadap PAR. Spesies dengan 3 sel log 2 μm 3 (atau 8 μm 3 ) berkontribusi secara signifikan lebih sedikit pada biovolume daripada spesies dengan sel yang lebih besar ( p < 0,001) dan cenderung meningkat dalam biovolume saat PAR meningkat (Gambar 4a ).
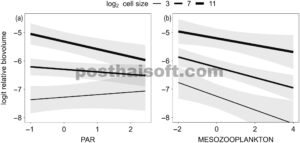
GAMBAR 4
Hubungan yang diprediksi antara ukuran sel dan biovolume fitoplankton relatif sepanjang gradien radiasi aktif fotosintesis (PAR) terstandarisasi (a) dan biomassa zooplankton (yaitu, tekanan penggembalaan yang mungkin) (b). Pita mewakili 95% CI. Tiga garis per plot menunjukkan spesies dengan ukuran sel 3, 7, dan 11 log 2 μm 3 , yang sesuai dengan 8, 128, dan 2048 μm 3 .
TABEL 2. Statistik dua model efek campuran linier (skala logit; lihat Persamaan 2 dalam Metode ) yang menggambarkan hubungan antara ukuran sel dan biovolume fitoplankton relatif sepanjang gradien radiasi aktif fotosintesis (PAR) terstandarisasi dan biomassa zooplankton (yaitu, tekanan penggembalaan yang diduga).
Model Faktor Memperkirakan Bahasa Inggris 95% CI nilai p
PAR β 0 -6.10 0.14 -6,34; -5,84 <0,001
β PAR -0,13 0,06 -0,24; -0,01 <0,05
ukuran β 0.64 0,09 0,46; 0,82 <0,001
ukuran β ×PAR -0,12 0,05 -0,22; -0,01 <0,05
Biomassa mesozooplankton β 0 -6,02 0.14 -6,27; -5,75 <0,001
kebun binatang beta -0,17 0,04 -0,25; -0,08 <0,001
ukuran β 0.66 0,09 0,48; 0,84 <0,001
β ukuran×kebun binatang 0,04 0,04 -0,04; 0,13 0.35
Catatan : 95% CI merujuk pada batas bawah dan atas 95% dari CI yang di-bootstrap (999 simulasi).
Fitoplankton juga merespons gradien biomassa zooplankton dalam mode spesifik spesies (LRT, χ 2 = 167,8, p < 0,001). Ukuran sel tidak memiliki efek signifikan pada biovolume relatif spesies di sepanjang gradien biomassa zooplankton (Gambar 4b , interaksi mesozooplankton:ukuran sel yang tidak signifikan, β ukuran×kebun binatang dalam Tabel 2 ) seperti yang ditunjukkan oleh LRT (χ 2 = 0,78, p = 0,38) dan bootstrap parametrik (999 simulasi, p = 0,40). Meskipun demikian, biovolume fitoplankton menurun secara signifikan saat biomassa zooplankton meningkat ( p < 0,001).
Ukuran sel tidak mempunyai efek signifikan pada biovolume relatif spesies sepanjang gradien SRP (Lampiran S4 : Gambar S1a ; LRT, χ 2 = 3,68, p = 0,06; bootstrap parametrik, 999 simulasi, p = 0,07), maupun seiring waktu (Lampiran S4 : Gambar S1b ; LRT, χ 2 = 1,30, p = 0,25; bootstrap parametrik, 999 simulasi, p = 0,28).
DISKUSI
Hasil kami yang menunjukkan efek merugikan yang jelas dari pencoklatan danau pada kekayaan spesies fitoplankton dan kemungkinan kemunculan spesies mendukung hipotesis pertama kami, yang menyatakan bahwa jumlah spesies fitoplankton akan berkurang seiring dengan meningkatnya limpasan daratan yang disebabkan oleh badai. Hasil ini sejalan dengan hasil dari percobaan penutupan skala kecil sebelumnya (Rasconi et al., 2015 ; Urrutia-Cordero et al., 2017 ) dan tampaknya terutama berasal dari berkurangnya produksi primer akibat keterbatasan cahaya oleh cDOM (Cooney et al., 2018 ; Solomon et al., 2015 ). Selain tingkat iradiasi yang berkurang, pergeseran spektrum cahaya bawah air mungkin telah memainkan peran dalam menyebabkan efek ini pada kekayaan dan kejadian spesies karena penyerapan preferensial PAR gelombang pendek oleh cDOM dapat mengganggu koeksistensi spesies karena partisi relung sepanjang spektrum PAR, yang dimungkinkan oleh kompleks pemanenan cahaya yang berbeda (Burson et al., 2019 ; Luimstra et al., 2020 ; Stomp et al., 2004 ). Untuk mendukung hipotesis ini, kekayaan fitoplankton memang menurun dalam komunitas laut alami yang terpapar cahaya merah dibandingkan dengan cahaya putih (Hintz et al., 2021 ). Meskipun bukan bukti konklusif bahwa partisi spektral memungkinkan koeksistensi spesies (Hintz et al., 2021 ), mekanisme ini, yang dimediasi oleh pencoklatan, kemungkinan memiliki pengaruh pada kejadian dan kekayaan spesies dalam percobaan kami.
Browning juga dapat secara tidak langsung memengaruhi komunitas fitoplankton, terutama dengan mengubah ketersediaan nutrisi, seperti yang ditunjukkan oleh peningkatan SRP dan konsentrasi nitrogen anorganik terlarut (DIN) di kandang kami yang menerima cDOM. Secara khusus, spesies yang dicirikan oleh tingkat penyerapan nutrisi yang tinggi dapat mengalahkan yang lain dengan memanfaatkan denyut nutrisi yang menyertai masukan cDOM (Sommer, 1984 ). Efek nutrisi tersebut melemah ketika keterbatasan cahaya menjadi sangat besar (Olson et al., 2020 ), seperti dalam penelitian kami. Namun, terlepas dari kepentingan relatif dari efek langsung versus tidak langsung, hasil kami menunjukkan bahwa kondisi cahaya yang berubah karena browning menyebabkan pergeseran penting dalam komunitas fitoplankton jika presipitasi dan limpasan meningkat di masa mendatang, seperti yang diprediksi (IPCC, 2023 ).
Hasil paling mencolok dari analisis kami terhadap komunitas fitoplankton dalam berbagai kondisi lingkungan adalah pengelompokan spesies dalam dua kelas ukuran berbeda sepanjang gradien ukuran sel. Distribusi bimodal (atau bahkan multimodal) seperti itu telah diamati dalam komunitas yang berkisar dari kumbang (Scheffer & Van Nes, 2006 ) hingga burung (Thibault et al., 2011 ) dan mamalia (Holling, 1992 ), dan dari pohon (D’Andrea et al., 2020 ) hingga fitoplankton (Downing et al., 2014 ; Segura et al., 2011 , 2013 ; Vergnon et al., 2009 , 2012 ). Ini menimbulkan pertanyaan apakah pola tersebut didorong oleh proses ekologi umum atau tidak. Kemungkinan pendorongnya adalah menstabilkan perbedaan relung (yaitu, partisi relung) dan mekanisme penyetaraan yang mengurangi perbedaan kebugaran di antara spesies yang bersaing (yaitu, netralitas; Adler et al., 2007 ; Chesson, 2000 ). Keduanya juga dapat bertindak bersama-sama (Downing et al., 2014 ; Segura et al., 2011 , 2013 ; Vergnon et al., 2009 , 2012 ), sebagaimana diartikulasikan dalam konsep yang dikenal sebagai netralitas yang muncul atau kesamaan yang terorganisasi sendiri (Holt, 2006 ; Scheffer et al., 2018 ; Scheffer & Van Nes, 2006 ). Dengan demikian, spesies dapat hidup berdampingan jika perbedaan antara atau di antara klaster cukup besar untuk membatasi persaingan, dan pada saat yang sama cukup mirip dalam klaster untuk mencegah pengecualian kompetitif. Kedua gaya tersebut dapat berkontribusi pada pergeseran dari distribusi ukuran sel unimodal ke bimodal yang muncul selama percobaan kami, yang mendukung gagasan tentang netralitas yang muncul, sedangkan paradoks Hutchinson muncul, sebagian, karena fokusnya yang unik pada perbedaan relung. Kesimpulan ini juga sesuai dengan hasil dari percobaan laboratorium yang menilai hasil kompetitif pada pasangan spesies sianobakteri penghuni versus spesies invasif yang berbeda dalam ukuran sel atau koloni, yang menunjukkan bahwa meskipun perbedaan ukuran tidak cukup untuk memprediksi koeksistensi spesies, perbedaan relung dan kebugaran meningkat seiring dengan perbedaan ukuran (Gallego et al., 2019 ).
Meskipun muncul sebagai pola umum dalam percobaan kami, pengelompokan yang kami amati terjadi secara berbeda di seluruh perlakuan eksperimental. Secara khusus, pengelompokan sel berukuran lebih kecil dominan dalam air jernih, sedangkan pengelompokan yang terdiri dari sel-sel yang lebih besar dianggap lebih penting pada tingkat pencoklatan yang tinggi. Perbedaan ini bertentangan dengan harapan kami menurut Hipotesis 2, yang menyatakan bahwa distribusi ukuran spesies dalam kondisi cahaya rendah dan ketersediaan nutrisi tinggi akan bergeser ke arah sel-sel kecil karena sifat penggunaan cahaya yang berskala dengan ukuran sel lebih menyukai spesies bersel kecil dalam cahaya redup (Edwards et al., 2015 ; Schwaderer et al., 2011 ). Beberapa proses dapat menyebabkan hasil yang tidak diharapkan.
Pertama, karena kuota nutrisi maksimum ( Q max ) meningkat lebih kuat dengan ukuran sel daripada kuota minimum ( Q min ), spesies besar memiliki kapasitas penyimpanan yang lebih besar ( Q max / Q min ) (Hillebrand et al., 2022 ; Litchman et al., 2009 ), memfasilitasi penyerapan P mewah (Solovchenko et al., 2019 ). Hal ini memberi mereka keunggulan kompetitif dalam kondisi nutrisi yang berfluktuasi karena mereka dapat memperoleh manfaat dari kumpulan nutrisi seluler yang dibangun lebih awal untuk mempertahankan pertumbuhan selama paparan cDOM ketika penyerapan SRP dan DIN tampak terganggu pada tingkat cahaya rendah dalam percobaan kami.
Kedua, ukuran sel mengatur perolehan sumber daya, mengalihkan fungsi trofik dari spesies autotrofik kecil ke spesies miksotrofik menengah ke spesies heterotrofik besar (Ward & Follows, 2016 ). Meskipun distribusi ukuran bersifat bimodal di hampir semua kandang kami, kemungkinan besar pencoklatan oleh cDOM memperburuk perkembangan spesies miksotrofik besar, seperti yang dilaporkan dalam studi kandang pencoklatan lainnya (misalnya, Urrutia-Cordero et al., 2017 ).
Ketiga, terlepas dari pentingnya ukuran sel sebagai sifat utama (Finkel et al., 2010 ; Irwin et al., 2006 ; Key et al., 2010 ), sifat spesies lain seperti motilitas, daya apung, atau pembentukan koloni (Clegg et al., 2003 ; Litchman & Klausmeier, 2008 ) juga dapat memengaruhi perolehan sumber daya dan karenanya distribusi ukuran sel fitoplankton. Misalnya, koloni sianobakteri menghindari peningkatan self-shading dengan peningkatan ukuran dengan mengurangi konsentrasi pigmen seluler atau kepadatan sel dalam koloni (Agustí & Phlips, 1992 ). Ini akan menjadi sangat penting ketika peningkatan ukuran koloni memperkuat penghindaran predator, seperti yang terlihat oleh peningkatan 10 kali lipat dalam diameter koloni rata-rata oleh Microcystis aeruginosa yang terpapar tekanan penggembalaan oleh flagellata Ochromonas sp. (Yang & Kong, 2012 ).
Terakhir, plastisitas ciri spesies yang berkaitan dengan penggunaan sumber daya mungkin memainkan peran, khususnya kemampuan spesies untuk beraklimatisasi terhadap perubahan kondisi cahaya (Dubinsky & Stambler, 2009 ; Guislain et al., 2019 ). Di sini, komposisi spektral mungkin juga penting, selain tingkat iradiasi yang berfluktuasi (Hintz et al., 2022 ), dengan aklimatisasi kromatik diprediksi bermanfaat di lingkungan tempat cahaya merah dan hijau dari spektrum PAR mendominasi (Sanfilippo et al., 2019 ). Cahaya hijau biasanya mendominasi di danau seperti Danau Stechlin, sementara penyerapan cahaya yang kuat oleh cDOM, khususnya dalam rentang gelombang pendek, menggerakkan spektrum ke arah panjang gelombang yang lebih panjang (cahaya merah). Meskipun aklimatisasi kromatik sebagian besar melibatkan penyesuaian kromofor (Kehoe & Gutu, 2006 ; Richardson, 2022 ; Sanfilippo et al., 2019 ), morfologi sel juga dapat berubah, seperti yang dijelaskan untuk cyanobacterium berfilamen, Fremyella diplosiphon , di mana sel-sel silindris dan lebih kecil yang tumbuh di bawah cahaya hijau menjadi lebih besar dan lebih bulat saat terkena cahaya merah. Alasan yang mendasarinya tidak diketahui (Gutu & Kehoe, 2012 ), tetapi fenomena tersebut menyiratkan bahwa beberapa sel yang lebih besar mungkin memiliki keunggulan kompetitif dibandingkan sel lain di bawah cahaya yang bergeser ke merah akibat pencoklatan danau.
Hasil kami juga memberikan wawasan tentang pentingnya ukuran sel pada struktur dominasi (kemerataan) komunitas dan menyoroti kebutuhan untuk menentukan distribusi sifat dalam komunitas untuk memprediksi respons komunitas terhadap perubahan lingkungan (Hillebrand et al., 2008 ; Norberg, 2004 ; Soininen et al., 2012 ). Memang, efek PAR yang bergantung pada ukuran yang kami temukan dalam analisis biovolume kami, tetapi tidak pada kemunculan spesies, kontras dengan pengaruh yang tampak bergantung pada ukuran dari penggembalaan mesozooplankton pada kemungkinan kemunculan spesies, tetapi tidak pada biovolume. Berbeda dengan Hipotesis 3 kami (yang menyatakan bahwa sel-sel besar akan meningkat jumlahnya pada tingkat cahaya dan nutrisi yang tinggi karena akses yang cukup ke kedua sumber daya dan mortalitas penggembalaan yang lebih rendah), perbedaan ini kemungkinan besar disebabkan oleh kecenderungan spesies langka dengan biovolume rendah untuk tidak terdeteksi pada tingkat cahaya rendah. Selain itu, peran mungkin dimainkan oleh kerentanan spesies kecil yang lebih besar terhadap penggembalaan tanpa mengubah distribusi ukuran sel dari biovolume relatif spesies dalam komunitas.
Secara keseluruhan, temuan kami menawarkan dukungan yang beragam untuk hipotesis awal kami, yang mengungkap dinamika kompleks terkait ukuran dalam komunitas fitoplankton yang dipengaruhi oleh pencoklatan danau. Hipotesis 1, yang memprediksi penurunan kekayaan spesies dengan peningkatan limpasan daratan, didukung karena kemungkinan kemunculan spesies menurun di bawah pencoklatan. Sebaliknya, Hipotesis 2 tidak didukung. Alih-alih mendukung spesies bersel kecil di bawah cahaya rendah dan ketersediaan nutrisi tinggi, seperti yang kami hipotesiskan, pencoklatan menyebabkan dominasi sel yang lebih besar yang lebih kuat. Ini menunjukkan bahwa sifat-sifat selain efisiensi penggunaan cahaya penting dalam memastikan keberhasilan spesies yang lebih besar dalam kondisi ini. Sifat-sifat seperti penyimpanan nutrisi atau miksotrofi dapat berperan dalam hal ini. Berdasarkan Hipotesis 3, kami mengantisipasi peningkatan kelimpahan sel besar di bawah cahaya tinggi dan tingkat nutrisi karena mortalitas penggembalaan yang lebih rendah. Namun, hasil kami menunjukkan bahwa, meskipun kemunculan spesies yang lebih kecil memang lebih rentan terhadap penggembalaan, efeknya tidak cukup kuat untuk secara signifikan mengubah distribusi ukuran sel spesies dalam komunitas.
Kesimpulannya, hasil percobaan kami yang dilakukan di kandang besar yang dirancang untuk meniru kondisi lingkungan yang realistis menunjukkan keunggulan kompetitif yang jelas dari spesies fitoplankton yang lebih besar daripada yang lebih kecil di bawah ketersediaan cahaya yang berkurang yang disebabkan oleh pencoklatan danau. Ini menggarisbawahi bahwa ukuran sel adalah sifat spesies yang sangat penting yang memengaruhi struktur dan dinamika komunitas fitoplankton setelah peristiwa badai yang membawa cDOM ke danau air jernih. Terlebih lagi, pengelompokan spesies yang diamati dalam kelas ukuran yang berbeda sepanjang gradien ukuran sel menyiratkan bahwa perbedaan ukuran di antara spesies mungkin sama pentingnya dengan ukuran spesies itu sendiri untuk memahami dinamika fitoplankton. Mengingat bahwa pergeseran dalam distribusi ukuran sel memiliki implikasi untuk struktur jaring makanan dan siklus biogeokimia, hasil kami dengan demikian menyoroti pentingnya menentukan struktur ukuran fitoplankton sebagai elemen penting untuk memperkirakan komunitas danau dan dinamika ekosistem dalam menanggapi perubahan lingkungan.
KONTRIBUSI PENULIS
Alexis LN Guislain menyusun penelitian dan menganalisis data. Mark O. Gessner, Anne Lyche Solheim, Stella A. Berger, Jens C. Nejstgaard, Ute Mischke, dan Hans-Peter Grossart merancang percobaan, yang dikoordinasikan oleh Stella A. Berger dan Jens C. Nejstgaard. Jens C. Nejstgaard dan Stella A. Berger merancang, membangun, dan menguji pengaturan teknis yang memungkinkan pengisian dan pencampuran percobaan dalam skala besar. Semua penulis mengumpulkan data. Ute Mischke dan Birger Skjelbred mengidentifikasi dan menghitung fitoplankton dan menentukan biomassanya. Erik Sperfeld mengidentifikasi dan menghitung zooplankton dan menentukan biomassanya. Alexis LN Guislain menulis naskah dengan kontribusi utama dari Mark O. Gessner, Jens C. Nejstgaard, Jan Köhler, Erik Sperfeld, Hans-Peter Grossart, Anne Lyche Solheim, dan Stella A. Berger. Naskah disetujui oleh semua penulis.
UCAPAN TERIMA KASIH
Kami sangat berterima kasih kepada A. Penske, M. Lentz, G. Idoate Santaolalla, A. Boiché, M. Sachtleben, M. Schnittger, S. Pinnow, E. Mach, R. Roßberg, U. Mallok, M. Degebrodt, M. Papke, E. Huth, U. Beyer, C. Kasprzak, G. Mohr, S. Beeske, K. Görden, C. Stratmann, J. Klein, K. Lörsch, M. Zamzow, M. Røst Kile, L. Tveiten, H. Christie, D. Giling, L. Minguez, S. Stephan, J. Fonvielle, T. Walles, L. Ganzert, P. Casper, S. van den Wyngaert, M. Belyaeva, A. Sepulveda-Jauregui, K. Martinez Cruz, M. Saebelfeld, T. Miki, N. Pansch, H. Ma, W. Eckert, S. Hilt, G. Singer, H. Gundersen, S. Haande, A. Ballot, S. Jannicke Moe, T. Hveem Hansson, A. Jechow, T. Hornick, dan F. Hölker atas berbagai kontribusinya pada pekerjaan lapangan dan laboratorium sebelum dan selama percobaan penutup. Pekerjaan ini dimulai sebagai bagian dari proyek MARS (Managing Aquatic Ecosystems and Water Resources under Multiple Stress) yang diberikan kepada MO Gessner dan A. Lyche Solheim oleh Komisi Eropa di bawah Program Kerangka ke-7 (hibah no. 603378) dan proyek ILES (Illuminating Lake Ecosystems) yang diberikan kepada MO Gessner dan F. Hölker oleh Leibniz Association (no. SAW-2015-IGB-1), dan didukung oleh Kementerian Pendidikan dan Penelitian Federal Jerman (BMBF) dalam Proyek Kolaboratif BIBS (Bridging in Biodiversity Science, no. 01LC1501) yang diberikan kepada MO Gessner dan H.-P. Grossart, dan hibah infrastruktur oleh BMBF (no. 033L041B) dan hibah Fasilitas Inti oleh Yayasan Penelitian Jerman (DFG, no. GE 1775/2-1), keduanya diberikan kepada MO Gessner. Dana tambahan selama tahap analisis data dan penulisan naskah disediakan oleh Komisi Eropa (EU H2020-INFRAIA) melalui proyek AQUACOSM (no. 731065) yang diberikan kepada JC Nejstgaard, SA Berger, dan MO Gessner, dan AQUACOSM-plus (no. 871081) kepada JC Nejstgaard dan SA Berger, serta melalui proyek CONNECT yang diberikan kepada SA Berger dan S. Wollrab oleh Leibniz Association (no. K45/2017). Kami berterima kasih kepada dua pengulas anonim atas komentar konstruktif mereka pada versi naskah sebelumnya. Pendanaan Open Access diaktifkan dan diselenggarakan oleh Projekt DEAL.
PERNYATAAN KONFLIK KEPENTINGAN
Penulis menyatakan tidak ada konflik kepentingan.
