Abstrak
Bidang transplantasi organ memerlukan pendekatan baru untuk mengganti dan meregenerasi jaringan karena kurangnya metode transplantasi yang memadai. Bioprinting berbasis ekstrusi tiga dimensi (3D) adalah pendekatan pembuatan prototipe cepat yang dapat merekayasa perancah 3D untuk aplikasi regenerasi jaringan. Dalam proses ini, konstruksi berbasis sel cetak 3D, yang terdiri dari biomaterial, faktor pertumbuhan, dan sel, dibentuk dengan ekstrusi biotinta dari nosel. Namun, ekstrusi memberikan tekanan geser pada sel, yang sering kali menyebabkan kerusakan sel atau pecahnya membran. Untuk mengatasi keterbatasan ini, di sini, kami mengembangkan dan mengoptimalkan pendekatan bioprinting 3D dengan mengevaluasi efek parameter bioprinting 3D berbasis ekstrusi utama—viskositas biotinta, ukuran nosel, bentuk, dan kecepatan pencetakan—pada viabilitas sel. Hasil kami mengungkapkan bahwa sel yang dicetak dalam biotinta dengan viskositas lebih tinggi, dengan nosel silinder yang lebih kecil, menunjukkan viabilitas yang lebih rendah karena paparannya terhadap tekanan geser yang tinggi. Kecepatan aliran translasi memiliki dampak yang bergantung pada sel, karena jenis sel yang berbeda memiliki kepekaan yang berbeda terhadap besarnya dan durasi tegangan geser di dalam nosel. Secara keseluruhan, mengevaluasi parameter ini dapat memfasilitasi pengembangan konstruksi biocetak resolusi tinggi 3D untuk aplikasi regenerasi jaringan, menawarkan alternatif yang lebih efisien untuk metode fabrikasi tradisional, yang sering kali padat karya, mahal, dan berulang.
1. PENDAHULUAN
Transplantasi organ telah menjadi landasan pengobatan untuk kegagalan organ stadium akhir, menyelamatkan dan memperpanjang hidup pasien yang menderita gangguan kegagalan organ. Meskipun ada peningkatan dalam teknologi bedah dan pengawetan organ, transplantasi organ masih menimbulkan kesulitan yang signifikan. Peningkatan jumlah pasien dalam daftar tunggu transplantasi karena kurangnya organ yang memadai untuk memenuhi permintaan merupakan tantangan besar. 1 – 3 Selain itu, variasi genetik antara donor dan penerima, 4 respons imun, 5 dan infeksi 6 meningkatkan kemungkinan penolakan.
Kemajuan terbaru dalam bidang rekayasa jaringan dan pengobatan regeneratif membuka jalan baru untuk mengganti dan meregenerasi jaringan dan organ. 7 , 8 Salah satu pendekatan pengobatan regeneratif yang paling umum melibatkan konstruksi perancah rekayasa jaringan dengan menggabungkan polimer alami, 9 , 10 polimer sintetis, 11 – 14 bahan keramik 15 – 17 , sel induk, 18 , 19 dan faktor pertumbuhan. 20 Konstruksi ini telah dikembangkan melalui berbagai metode fabrikasi, seperti pemintalan listrik, 21 , 22 pemisahan fase, 23 , 24 pengeringan beku, 25 , 26 dan perakitan sendiri. 27 – 29 Meskipun demikian, pendekatan ini telah menunjukkan keterbatasan dalam menghasilkan perancah multifungsi dan multi-material dengan geometri yang kompleks dan terkendali, jaringan pori, dan sifat biologis. 30 – 32 Oleh karena itu, solusi alternatif sangat penting untuk mengatasi keterbatasan metode fabrikasi saat ini.
Strategi bioprinting tiga dimensi (3D), termasuk berbasis tetesan, 33 , 34 stereolitografi, 35 , 36 dan ekstrusi, 37 – 39 telah menunjukkan keunggulan dibandingkan metode tradisional untuk menghasilkan perancah dengan cara yang cepat, tepat, dan terkendali. 40 Proses ini didasarkan pada penggunaan metode berbantuan komputer untuk memungkinkan pembuatan pola spasial sel dan/atau biomaterial secara otomatis dan simultan. 41 , 42 Secara khusus, strategi bioprinting 3D berbasis ekstrusi merupakan salah satu modalitas pertama yang dikembangkan dan sekarang dapat dikatakan paling banyak digunakan untuk menghasilkan konstruksi jaringan 3D. Biotinta diendapkan ke substrat melalui ekstrusi pneumatik, piston, atau penggerak sekrup. 43 – 45
Selama proses ini, cedera sel dapat bersumber dari berbagai bujukan atau rangsangan seperti tegangan geser, 44 , 46 tegangan termal, 47 , 48 dan tegangan radiasi. 45 , 49 Persentase cedera sel bergantung pada kekuatan dan durasi rangsangan. Jika tegangan yang diberikan melebihi kapasitas beban sel tunggal, kerusakan sel yang ireversibel akan terjadi, yang mengakibatkan kematian sel yang tidak terduga. 45 , 50 Dalam kasus bioprinting 3D berbasis ekstrusi, tegangan geser tinggi di dalam nosel sering kali menyebabkan pecahnya membran sel dan kerusakan/kematian sel berikutnya. 45 , 49 Selain pengaruh besarnya tegangan geser pada kerusakan sel, durasi tegangan geser yang diberikan pada sel juga penting, yang menunjukkan efek akumulatif tegangan geser pada kerusakan sel. 45
Dalam studi ini, kami mengembangkan dan mengoptimalkan pendekatan bioprinting 3D dengan mengevaluasi peran parameter bioprinting 3D berbasis ekstrusi utama dalam kelangsungan hidup sel. Untuk tujuan ini, kami menilai dampak viskositas biotinta, ukuran dan bentuk nosel, dan kecepatan cetak pada kelangsungan hidup sel pasca-cetak. Hasil kami menunjukkan bahwa parameter ini saling berhubungan dan bergantung satu sama lain, yang menunjukkan kompleksitas proses bioprinting 3D. Metodologi yang kami usulkan menyediakan dasar untuk mengembangkan standar untuk proses bioprinting 3D dengan memberikan pedoman untuk mempercepat proses pemilihan parameter untuk aplikasi bioprinting. Secara keseluruhan, pendekatan ini akan memajukan efisiensi pembuatan konstruksi bioprinting 3D dengan fidelitas tinggi untuk aplikasi regenerasi jaringan.
2 BAHAN DAN METODE
2.1 Kultur sel
Bahasa Indonesia: Sel Human Embryonic Kidney-293T (HEK-293T) (American Type Culture Collection: CRL-3216, Manassas, VA, AS) dan Normal Human Knee Articular Chondrocytes (NHAC-kn) (Lonza, Walkersville, MD, AS) dikultur dalam Dulbecco’s Modified Eagle Medium (DMEM) (Thermo Fisher Scientific, Waltham, MA, AS) yang dilengkapi dengan 10% (v/v) Fetal Bovine Serum (FBS) dan 1% (v/v) larutan Penicillin–Streptomycin (P/S).
2.2 Persiapan Biotinta
Awalnya, larutan sel disiapkan dengan cara mensuspensikan kembali 5 × 105 sel dalam 1 mL DMEM (ditambah dengan 10% (v/v) FBS dan 1% (v/v) larutan P/S) dan 9 mL air deionisasi pada suhu 37°C. Selanjutnya, bubuk gelatin dilarutkan pada suhu 37°C selama 30 menit dalam larutan sel untuk menghasilkan biotinta pada konsentrasi akhir 10% (b/v), 15% (b/v), dan 20% (b/v).
2.3 Reologi
Sifat reologi biotinta pada konsentrasi larutan gelatin 10% (b/v) ditentukan menggunakan rheometer MCR702 (Anton Paar, Ashland, VA, AS) dengan sistem pengukuran Couette celah ganda DG26.7. Demikian pula, sifat reologi biotinta pada konsentrasi larutan gelatin 15% (b/v) dan 20% (b/v) ditentukan menggunakan rheometer MCR302 (Anton Paar, Ashland, VA, AS) yang dipasangi pelat paralel baja tahan karat berdiameter 25 mm sebagai sistem pengukuran yang diatur pada celah 1 mm. Sebelum setiap pengujian, tinta disimpan secara isotermal pada suhu 35°C selama 5 menit dengan sistem Peltier yang terdiri dari pelat bawah dan penutup. Sapuan frekuensi osilasi dikumpulkan pada regangan 125%, dari frekuensi 100 rad/s hingga 1 rad/s.
2.4 Biocetak 3D
Biotinta ditempatkan ke dalam kartrid cetak yang disterilkan ultraviolet (UV) dari 3D-Bioplotter (EnvisionTec GmbH, Gladbeck, Jerman). Kartrid dimuat ke dalam printer dan diseimbangkan ke suhu 35°C selama 45 menit dalam kompartemen yang dipanaskan sebelum mencetak. Biotinta diekstrusi melalui nosel sepanjang 12,5 mm ke pelat kultur sel 6-sumur, menghasilkan filamen kontinu satu lapis berukuran 20 mm × 20 mm dengan pola pengisian bujursangkar seperti yang dirancang menggunakan perangkat lunak Perfactory RP (EnvisionTEC, Dearborn, MI, AS) (Gambar 1 dan S1 ). Untuk memastikan kesetiaan pencetakan 3D, kami melakukan proses berikut untuk menghasilkan filamen kontinu dan seragam. Kartrid larutan gelatin dimasukkan ke dalam printer dan diatur ke suhu 35°C. Bahan tersebut diekstrusi ke dalam cawan Petri selama durasi tertentu pada tekanan yang telah ditentukan (misalnya, 0,3 bar selama 10 detik) dan kemudian ditimbang pada neraca mikro. Berdasarkan pengukuran berat tersebut, fluks volume bahan dan kecepatan aliran dihitung untuk setiap desain eksperimen. Analisis regresi linier digunakan untuk setiap eksperimen, dan berdasarkan itu, tekanan dan kecepatan aliran diidentifikasi dan diuji untuk menghasilkan filamen kontinu dan seragam yang dicetak 3D (Gambar S2 ).
2.5 Pengujian sel hidup/mati
Filamen bermuatan sel diwarnai dengan LIVE/DEAD Viability/Cytotoxicity Assay Kit (Invitrogen, Waltham, MA, AS) berdasarkan petunjuk pabrik untuk menentukan viabilitas sel. Secara khusus, larutan kerja kalsein-AM dan etidium homodimer-1 dibuat dalam larutan penyangga fosfat (PBS) pada konsentrasi masing-masing 2 dan 4 μmol/L. Selanjutnya, 500 μL larutan dioleskan ke setiap konstruksi cetak 3D bermuatan sel, konstruksi noncetak (kontrol), dan konstruksi tanpa sel, dan diinkubasi pada suhu ruangan selama 45 menit. Kemudian, filamen bermuatan sel, kontrol, dan tanpa sel hasil cetak 3D dicuci dua kali selama 5 menit masing-masing dengan 1 mL PBS, diikuti dengan pencitraan di bawah mikroskop otomatis.
2.6 Analisis gambar throughput tinggi
Pencitraan sel hidup (hijau) dan mati (merah) dalam filamen dilakukan dengan lensa 4x dari Mikroskop Otomatis BioTek Lionheart LX (Agilent, Santa Clara, CA, AS). Beberapa titik dijahit bersama untuk menghasilkan citra komposit dari seluruh struktur, yang mencakup area seluas 21 mm × 21 mm. Sel hidup (hijau) dan mati (merah) di setiap sumur dihitung menggunakan Perangkat Lunak Pembaca dan Pencitra Mikroplat Agilent BioTek Gen 5 Versi 3.14. Viabilitas sel dalam struktur yang dicetak dihitung sebagai rasio sel hidup (hijau) terhadap jumlah sel total di setiap gambar dan dinormalisasi oleh viabilitas sel bioink yang tidak dicetak (kontrol) yang tidak diekstrusi melalui nosel jarum suntik. Dalam percobaan ini, filamen tanpa sel digunakan sebagai kontrol negatif untuk mengukur tingkat sinyal latar belakang yang tidak spesifik. Untuk setiap percobaan, pencitraan filamen tanpa sel dilakukan untuk memastikan bahwa setiap sinyal yang diamati dapat dikaitkan secara khusus dengan kondisi percobaan dan bukan kebisingan latar belakang (Gambar S3 ).
2.7 Analisis statistik
Analisis data statistik dilakukan menggunakan analisis varians satu arah (ANOVA) dan uji pasca Tukey untuk lebih dari dua variabel. Nilai p signifikan jika p < 0,05; hasilnya dinyatakan sebagai nilai rata-rata plus atau minus satu kesalahan standar. Setiap percobaan diulang secara independen tiga kali ( N = 3), dengan 12 sampel ( n = 12) yang disiapkan per kondisi untuk memastikan analisis statistik yang kuat dan konsistensi. N dan n ditunjukkan pada keterangan gambar.
3 HASIL
Bahasa Indonesia: Untuk menetapkan kondisi optimal untuk bioprinting 3D, meminimalkan kebutuhan untuk upaya berulang, bervariasi, dan melelahkan untuk mencapai konstruksi bioprinted 3D resolusi tinggi yang sukses, kami awalnya mengembangkan dan mengoptimalkan parameter bioprinting 3D berbasis ekstrusi utama. Biotinta cetak 3D yang terdiri dari sel dan larutan gelatin pada konsentrasi akhir 10% (b/v), 15% (b/v), dan 20% (b/v), dievaluasi untuk kelangsungan hidup sel mereka melalui penyetelan konsentrasi gelatin, bentuk dan ukuran nosel, dan kecepatan aliran ekstrusi (Gambar 1a dan S1 ). Dalam kondisi ini, biotinta diekstrusi menggunakan bioplotter 3D yang membentuk struktur 20 mm × 20 mm satu lapis, sarat sel (Gambar 1b ), yang diukur pada throughput tinggi untuk kelangsungan hidup sel melalui mikroskopi (Gambar 1c ).

Representasi skematis dari proses bioprinting 3D. (a) Biotinta cetak 3D yang terdiri dari sel dan larutan gelatin dievaluasi untuk viabilitas selnya melalui pengaturan konsentrasi gelatin, bentuk dan ukuran nosel, serta kecepatan aliran ekstrusi. (b) Biotinta dimasukkan dan diekstrusi melalui bioprinter 3D sehingga menghasilkan pembentukan struktur bermuatan sel cetak 3D. (c) Pengukuran viabilitas sel dari struktur cetak 3D melalui mikroskopi.
Sebelum melakukan percobaan viabilitas sel, penting untuk memastikan bahwa kami akan menghasilkan konstruksi cetak 3D dengan fidelitas tinggi (Gambar S2 ) dengan menyetel parameter cetak 3D. Untuk mencapainya, kami menghitung kecepatan aliran material yang diekstrusi pada berbagai peningkatan tekanan (0,1–1,7 bar, atau 10–170 kPa). Secara khusus, massa material dengan kepadatan
diekstrusi selama rentang interval waktu pendek (1–5 detik) pada tekanan tertentu diukur. Volume material yang diekstrusi untuk setiap cetakan 3D dihitung berdasarkan persamaan
Selanjutnya kecepatan aliran dihitung berdasarkan persamaan
, Di mana
pada setiap kenaikan tekanan ditentukan. Pada Gambar 2 , regresi linier dalam grafik menunjukkan pedoman untuk mengidentifikasi kecepatan translasi pada tekanan yang sesuai untuk menghasilkan filamen yang kontinu dan seragam. Berdasarkan analisis ini, kami mengevaluasi bagaimana viskositas tinta pada konsentrasi (10% (w/v), 15% (w/v), dan 20% (w/v)) mengendalikan jumlah material yang diekstrusi pada tekanan yang berbeda. Kami menemukan bahwa pada kecepatan aliran 50 mm/s, gelatin yang diekstrusi pada konsentrasi 10% (w/v) dicetak pada 0,1 bar, 15% (w/v) dicetak pada 0,6 bar, dan 20% (w/v) dicetak pada 1,6 bar (Gambar 2a ). Berdasarkan analisis regresi linier, kami mengidentifikasi bahwa ekstrusi gelatin 15% (b/v) melalui nosel kerucut dan silinder memerlukan 0,1 bar dan 1,8 bar, masing-masing, pada 100 mm/s (Gambar 2b ). Berikutnya, kami mengevaluasi kondisi pencetakan 3D untuk gelatin 15% (b/v) dengan menyetel diameter nosel. Dalam analisis ini, regresi linier menunjukkan bahwa pada kecepatan aliran 70 mm/s, tekanan yang diperlukan adalah 0,3 bar, 0,5 bar, 0,7 bar, dan 1,5 bar untuk diameter nosel masing-masing 0,51 mm, 0,41 mm, 0,34 mm, dan 0,26 mm (Gambar 2c ). Akhirnya, untuk memeriksa bagaimana kecepatan aliran memengaruhi pencetakan, model regresi linier yang diukur sebelumnya digunakan untuk menghitung tekanan yang diperlukan untuk mencapai kecepatan aliran 25 mm/s, 50 mm/s, 75 mm/s, dan 100 mm/s. Selama proses ini, konsentrasi gelatin (15% (b/v)) dan ukuran nosel (0,34 mm) tetap konstan (Gambar 2d ). Selama pekerjaan ini, kecepatan translasi nosel diatur agar sesuai dengan kecepatan aliran tinta yang diantisipasi melalui nosel untuk mencapai filamen yang kontinu dan seragam. Di sini, kecepatan cetak mengacu pada kecepatan aliran translasi dan terhitung. Nilai terhitung untuk setiap kondisi yang diuji didefinisikan dan dirangkum dalam Tabel 1 .
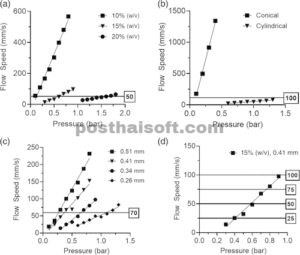
Penetapan parameter bioprinting 3D berdasarkan perkiraan kecepatan aliran. (a) Plot menggambarkan regresi linier dari kecepatan aliran ekstrusi terukur (mm/dtk) untuk tinta gelatin pada konsentrasi 10% (w/v), 15% (w/v), dan 20% (w/v) yang diekstrusi pada rentang tekanan 0 bar–2 bar melalui nosel silinder. (b) Evaluasi kecepatan aliran ekstrusi (mm/dtk) tinta gelatin (15% (w/v)) yang diekstrusi pada rentang tekanan 0 bar–2 bar melalui nosel berdiameter 0,26 mm, 0,34 mm, 0,41 mm, dan 0,51 mm pada suhu 35 °C. (c) Perbandingan kecepatan aliran ekstrusi untuk gelatin 15% (w/v) yang diekstrusi melalui nosel kerucut dan silinder pada suhu 35 °C. (d) Prediksi tekanan yang dibutuhkan (bar) untuk mencapai kecepatan aliran ekstrusi 25 mm/s, 50 mm/s, 75 mm/s, dan 100 mm/s untuk tinta gelatin (15% (b/v)) yang diekstrusi melalui nosel silinder 0,34 mm pada suhu 35°C.
Untuk mencapai proses bio-fabrikasi yang dapat direproduksi dan dikarakterisasi sepenuhnya untuk struktur gelatin biocetak 3D, kemampuan cetak biotinta pada konsentrasi 10% (b/v), 15% (b/v), dan 20% (b/v) dikarakterisasi dengan melakukan pengukuran reologi. Hasil kami menunjukkan bahwa viskositas meningkat dengan meningkatnya konsentrasi gelatin terlepas dari keberadaan sel (Gambar 3a,b dan S2 ). Misalnya, pada 10 rad/s, viskositasnya adalah 0,04 Pa·s, 0,8 Pa·s, dan 4 Pa·s untuk biotinta gelatin pada konsentrasi 10% (b/v), 15% (b/v), dan 20% (b/v), masing-masing. Selain itu, keberadaan sel meningkatkan indeks konsistensi aliran ( K ) sambil mengurangi indeks perilaku aliran ( n ) (Tabel 2 ), yang menunjukkan bahwa keberadaan sel meningkatkan perilaku penipisan geser.
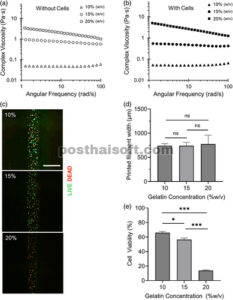
Kehadiran sel mengubah viskositas kompleks dari biotinta gelatin. Grafik menggambarkan viskositas kompleks (Pa·s) dari tinta gelatin pada berbagai konsentrasi: 10% (w/v), 15% (w/v), dan 20% (w/v). Sapuan frekuensi menurun dilakukan pada frekuensi sudut yang berkisar dari 100 rad/s hingga 1 rad/s pada (a) tinta gelatin tanpa sel dan (b) tinta gelatin dengan 5 × 105 sel /mL. (c) Gambar mikroskop fluoresensi representatif dari sel HEK-293T yang dicetak dalam tinta gelatin 10% (w/v), 15% (w/v), dan 20% (w/v). (d) Lebar filamen cetak yang dihasilkan oleh 10% (w/v), 15% (w/v), dan 20% (w/v) biotinta dan (e) persentase kelangsungan hidup relatif yang dinormalisasi dari sel yang dicetak dengan biotinta gelatin pada konsentrasi 10% (w/v), 15% (w/v), dan 20% (w/v). Sel hidup (Hijau) dan sel mati (Merah) (skala batang: 1000 μm). Semua percobaan dilakukan pada 35°C menggunakan nosel silinder dengan diameter 0,34 mm dan kecepatan cetak 50 mm/s. Data dinyatakan sebagai nilai rata-rata plus atau minus satu kesalahan standar untuk N = 3 dan n = 12 untuk setiap kondisi. Tanda bintang (*) menunjukkan nilai p dari p < 0,05; (**) menunjukkan nilai p dari p < 0,01; (***) menunjukkan nilai p dari p < 0,001; dan ns menunjukkan tidak ada hubungan yang signifikan secara statistik.
Berikutnya, kami mengevaluasi dampak viskositas gelatin pada lebar filamen dan viabilitas sel. Menurut Tabel 1 , berbagai konsentrasi gelatin diekstrusi melalui nosel silinder 0,34 mm pada laju alir 50 mm/s dan menghasilkan filamen kontinu dan seragam dengan lebar 750 ± 35 μm (Gambar 3c,d dan S2 ). Hal ini menunjukkan bahwa metode regresi linier yang digunakan dalam penelitian kami memungkinkan pembuatan filamen gelatin dengan kesetiaan dan akurasi yang tinggi. Berikutnya, dalam kondisi tersebut, kami mengevaluasi tegangan geser yang mungkin dialami sel. Tegangan geser dihitung berdasarkan persamaan
, di mana P adalah tekanan cetak yang sesuai, D adalah diameter nosel, dan L adalah panjang nosel. Hasil kami menunjukkan bahwa biotinta viskositas tinggi pada konsentrasi 20% (b/v) menyebabkan sel terpapar pada tekanan geser yang lebih tinggi (Tabel 3 ) dan menunjukkan viabilitas sel yang lebih rendah. Secara khusus, sel dalam biotinta gelatin 20% (b/v) menunjukkan penurunan viabilitas lima kali lipat dibandingkan dengan kondisi lain, sementara hanya perubahan yang lebih kecil yang diamati antara gelatin 10% (b/v) dan 15% (b/v) (Gambar 3e ).
Berikutnya, kami memperluas studi kami untuk menyelidiki bagaimana bentuk dan ukuran nosel mengatur viabilitas sel dalam biotinta pada konsentrasi gelatin 15% (b/v). Kami juga mengukur lebar filamen untuk mengevaluasi sejauh mana filamen menyebar ke substrat selama pencetakan. Filamen bermuatan sel yang dicetak menggunakan nosel kerucut dua kali lebih lebar daripada yang dicetak dengan nosel silinder (Gambar 4a,b,d,e ). Selain itu, analisis tegangan geser kami menunjukkan bahwa sel-sel dalam nosel silinder terkena tegangan geser yang lebih tinggi dibandingkan dengan kerucut (Tabel 3 ). Kami selanjutnya memeriksa apakah bentuk nosel silinder dan kerucut mempengaruhi viabilitas sel HEK-293T dan NHAC-kn. Seperti yang diharapkan, hasil kami menunjukkan bahwa viabilitas sel untuk sel HEK-293T dan NHAC-kn yang dicetak dengan nosel silinder menurun masing-masing dua kali lipat dan tiga kali lipat, dibandingkan dengan nosel kerucut (Gambar 4c,f ). Berikutnya, kami mengevaluasi efek diameter nosel silinder pada viabilitas sel HEK-293T dan NHAC-kn. Biotinta gelatin pada konsentrasi 15% (b/v) diekstrusi melalui nosel silinder dengan diameter dalam 0,51 mm, 0,41 mm, 0,34 mm, dan 0,26 mm pada kecepatan cetak 70 mm/dtk. Sel-sel tersebut secara proporsional terpapar pada tingkat tegangan geser yang lebih tinggi saat diameter nosel menurun (Tabel 3 ). Konstruksi bermuatan sel HEK-293T yang dicetak dengan nosel berdiameter 0,26 mm menghasilkan lebar filamen terkecil (Gambar 5a,b ) dan menunjukkan viabilitas sel 1,5 kali lebih rendah dibandingkan dengan konstruksi yang dicetak dengan nosel berdiameter 0,51 mm (Gambar 5c ). Demikian pula, konstruksi bermuatan sel NHAC-kn yang dicetak dengan nosel 0,26 mm membentuk filamen yang dua kali lebih sempit daripada yang dicetak dengan nosel 0,51 mm (Gambar 5d,e ). Dalam kondisi yang sama, hasil kami menunjukkan bahwa viabilitas sel menurun hingga 3,5 kali lipat (Gambar 5f ), yang menunjukkan bahwa sel yang dikeluarkan melalui nosel kecil terpapar tekanan mekanis tinggi, yang berpotensi menyebabkan kematian sel.
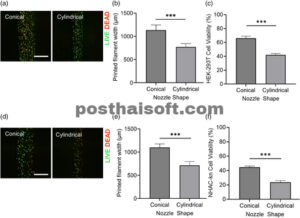
Bentuk nosel mengontrol viabilitas sel selama pencetakan. (a) Gambar mikroskop fluoresensi representatif dari struktur bermuatan sel HEK-293T yang dicetak dengan nosel kerucut dan silinder. Sel hidup (Hijau) dan sel mati (Merah) (batang skala: 1000 μm). (b) Lebar filamen cetak yang dihasilkan oleh nosel kerucut dan silinder (c) Persentase viabilitas sel yang dinormalkan relatif. (d) Gambar mikroskop fluoresensi representatif dari struktur bermuatan sel NHAC-kn yang dicetak dengan nosel kerucut dan silinder. Sel hidup (Hijau) dan sel mati (Merah) (batang skala: 1000 μm). (e) Lebar filamen cetak yang dihasilkan oleh nosel kerucut dan silinder (f) Persentase viabilitas sel yang dinormalkan relatif. Semua percobaan dilakukan menggunakan 15% (b/v) gelatin pada suhu 35°C melalui nosel 0,26 mm dan kecepatan cetak 100 mm/dtk. Data dinyatakan sebagai nilai rata-rata plus atau minus satu standar error pada N = 3 dan n = 12 untuk setiap kondisi. Tanda bintang (*) menunjukkan nilai p sebesar p < 0,05; (**) menunjukkan nilai p sebesar p < 0,01; (***) menunjukkan nilai p sebesar p < 0,001; dan ns menunjukkan tidak ada hubungan yang signifikan secara statistik.
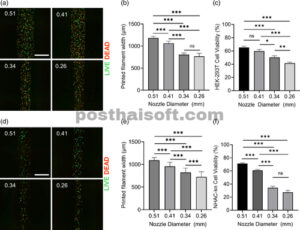
Diameter nosel mengatur viabilitas sel selama pencetakan. (a) Gambar mikroskop fluoresensi representatif dari struktur cetakan sel HEK-293T menggunakan nosel 0,51 mm, 0,41 mm, 0,34 mm, dan 0,26 mm. Sel hidup (Hijau) dan Sel mati (Merah) (skala batang: 1000 μm). (b) Lebar filamen cetakan yang dihasilkan oleh diameter nosel 0,51 mm, 0,41 mm, 0,34 mm, dan 0,26 mm. (c) Persentase viabilitas sel HEK-293T yang dinormalisasi relatif. (d) Gambar mikroskop fluoresensi representatif dari struktur bermuatan sel NHAC-kn yang dicetak dengan nosel 0,51 mm, 0,41 mm, 0,34 mm, dan 0,26 mm. Sel hidup (Hijau) dan Sel mati (Merah) (skala batang: 1000 μm). (e) Lebar filamen yang dicetak, dan (f) Persentase viabilitas sel NHAC-kn yang dinormalisasi secara relatif. Semua percobaan dilakukan menggunakan gelatin 15% (b/v) pada suhu 35°C dengan kecepatan cetak 70 mm/s. Data dinyatakan sebagai nilai rata-rata plus atau minus satu standar error pada N = 3 dan n = 12 untuk setiap kondisi. Tanda bintang (*) menunjukkan nilai p < 0,05; (**) menunjukkan nilai p < 0,01; (***) menunjukkan nilai p < 0,001; dan ns menunjukkan tidak ada hubungan yang signifikan secara statistik.
Parameter terakhir yang diuji dalam percobaan optimasi kami adalah kecepatan aliran. Biotinta gelatin pada konsentrasi 15% (b/v) diekstrusi melalui nosel silinder 0,34 mm pada kecepatan aliran 25 mm/s, 50 mm/s, 75 mm/s, dan 100 mm/s. Meskipun kecepatan tercepat (100 mm/s) empat kali lebih tinggi daripada kecepatan paling lambat (25 mm/s) dan memaparkan sel pada tegangan geser 2,5 kali lebih besar, tidak ada perbedaan signifikan secara statistik yang diamati dalam viabilitas sel HEK-293T rata-rata di seluruh kondisi ini (Gambar 6a,b ). Sebaliknya, data kami menunjukkan bahwa viabilitas sel NHAC-kn menurun seiring dengan peningkatan kecepatan aliran. Khususnya, sel NHAC-kn yang dicetak pada 100 mm/s memiliki pengurangan viabilitas sel 1,5 kali lipat dibandingkan dengan yang dicetak pada 25 mm/s, yang menunjukkan bahwa viabilitas sel dikontrol oleh kecepatan aliran (Gambar 6c,d ). Secara keseluruhan, data ini menunjukkan bahwa kecepatan aliran mengendalikan viabilitas sel secara berbeda tergantung pada jenis sel.
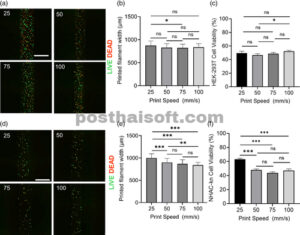
Kecepatan cetak translasi memengaruhi viabilitas sel selama proses pencetakan. (a) Gambar mikroskop fluoresensi representatif dari struktur bermuatan sel HEK-293T yang dicetak pada 25 mm/s, 50 mm/s, 75 mm/s, dan 100 mm/s. Sel hidup (Hijau) dan sel mati (Merah) (skala batang: 1000 μm). (b) Lebar filamen yang dicetak. (c) Persentase viabilitas sel HEK-293T yang dicetak pada kecepatan translasi 25 mm/s, 50 mm/s, 75 mm/s, dan 100 mm/s. (d) Gambar mikroskop fluoresensi representatif dari struktur bermuatan sel NHAC-kn yang dicetak pada 25 mm/s, 50 mm/s, 75 mm/s, dan 100 mm/s. Sel hidup (Hijau) dan sel mati (Merah) (skala batang: 1000 μm). (e) Lebar filamen yang dicetak. (f) Persentase viabilitas sel NHAC-kn yang dicetak pada kecepatan translasi 25 mm/s, 50 mm/s, 75 mm/s, dan 100 mm/s. Semua percobaan dilakukan menggunakan gelatin 15% (b/v) pada suhu 35°C dengan nosel silinder berdiameter 0,34 mm. Data dinyatakan sebagai nilai rata-rata plus atau minus satu standar error dengan N = 3 dan n = 12 untuk setiap kondisi. Tanda bintang (*) menunjukkan nilai p sebesar p < 0,05; (**) menunjukkan nilai p sebesar p < 0,01; (***) menunjukkan nilai p sebesar p < 0,001; dan ns menunjukkan tidak ada hubungan yang signifikan secara statistik.
4 DISKUSI
Mengembangkan konstruksi biocetak 3D beresolusi tinggi dengan fidelitas tinggi untuk aplikasi rekayasa jaringan sering kali merupakan proses yang melelahkan, mahal, berulang, dan sangat menuntut. 51 Tantangan utama melibatkan pemaparan sel terhadap kondisi yang merusak, seperti tegangan geser tinggi selama ekstrusi, yang sering memengaruhi kelangsungan hidup sel, sehingga menghasilkan konstruksi jaringan cetak 3D yang tidak berfungsi. Meskipun beberapa penelitian telah melaporkan peran tekanan, kecepatan, dan komposisi matriks dalam pencetakan 3D, 52 perannya dalam menghasilkan konstruksi biocetak 3D dengan fidelitas tinggi dan kelangsungan hidup sel belum dieksplorasi secara menyeluruh. Untuk mengatasi hal ini, kami bertujuan untuk menilai bagaimana parameter tersebut memengaruhi kelangsungan hidup sel selama pencetakan berbasis ekstrusi. Temuan ini akhirnya memberikan pedoman untuk merekayasa struktur sel cetak 3D fidelitas tinggi secara efisien untuk pengobatan regeneratif.
Kami menguji empat variabel secara independen untuk menilai bagaimana parameter pencetakan yang berbeda memengaruhi kelangsungan hidup sel selama proses pencetakan. Awalnya, kami memeriksa efek konsentrasi gelatin pada viabilitas sel. Kami memilih gelatin, hidrogel pengencer geser yang banyak digunakan dalam aplikasi rekayasa jaringan dan bioprinting 3D dengan biokompatibilitas yang baik, biodegradabilitas, dan mekanisme ikatan silang yang mudah. 45 , 53 Data reologi kami menunjukkan bahwa konsentrasi gelatin memengaruhi ekstrusi material dari nosel, yang menggambarkan bahwa konsentrasi gelatin yang lebih tinggi menyebabkan viabilitas sel yang lebih rendah. Selain itu, kami menghitung indeks konsistensi aliran ( K ) dan indeks perilaku aliran ( n ) untuk tinta gelatin dengan dan tanpa sel untuk memberikan wawasan tambahan tentang perilaku reologi fluida. 54 – 56 Nilai K yang lebih tinggi menunjukkan peningkatan viskositas, sedangkan nilai n kurang dari 1 menunjukkan fluida pengencer geser, dengan nilai yang lebih rendah mencerminkan efek pengencer geser yang lebih substansial. Data kami menunjukkan bahwa penambahan sel cenderung meningkatkan viskositas biotinta dan meningkatkan sifat pengenceran gesernya, yang mengonfirmasi bahwa perubahan viskositas yang diamati terutama disebabkan oleh penggabungan sel daripada pengenceran. Pengamatan tersebut sejalan dengan studi komputasional sebelumnya, 57 , 58 yang menunjukkan bahwa biotinta kental secara inheren memberikan tekanan geser yang tinggi pada sel, yang berdampak negatif pada kelangsungan hidup mereka. Meskipun, dalam studi saat ini, kami berfokus terutama pada efek viskositas gelatin pada kelangsungan hidup sel, sifat lain dari biotinta, seperti tekanan luluh dan tiksotropi, harus dieksplorasi lebih lanjut untuk merancang skema pencetakan dengan berbagai biomaterial. 59
Selain itu, penelitian kami mengevaluasi efek bentuk dan ukuran nosel pada kesetiaan dan akurasi filamen biocetak 3D. Analisis regresi linier memungkinkan kami menghasilkan filamen cetak 3D dengan kesetiaan dan akurasi tinggi dalam arah x , y , dan z . Misalnya, hasil kami dari 10 filamen cetak menunjukkan bahwa tinggi rata-rata adalah 244,03 ± 9,51 μm (dengan toleransi 3,90%) dan lebarnya adalah 750 ± 35 μm untuk biotinta (15% (b/v) gelatin) yang diekstrusi dari nosel 0,34 mm pada kecepatan cetak 50 mm/s. Pengukuran ini menunjukkan bahwa pendekatan kami dapat diterapkan dalam penelitian mendatang untuk menghasilkan konstruksi multilapis biocetak 3D dengan kesetiaan dan akurasi tinggi.
Selain itu, kami menilai bagaimana bentuk dan ukuran nosel mengendalikan viabilitas sel dengan menghindari keterbatasan penyumbatan nosel, gelasi tertunda, fidelitas pencetakan rendah, dan akurasi yang ditunjukkan oleh biotinta gelatin rendah (10% (b/v)) atau tinggi (20% (b/v)) pada suhu 35°C (data tidak ditampilkan). Meskipun penyesuaian suhu nosel dan substrat akan mengatasi keterbatasan tersebut, 60 , 61 parameter suhu akan meningkatkan kompleksitas evaluasi bentuk dan ukuran nosel pada viabilitas sel. Dengan demikian, biotinta konsentrasi gelatin 15% (b/v) telah mencapai keseimbangan terbaik antara resolusi, retensi bentuk, dan penyumbatan minimal pada suhu 35 °C dan digunakan untuk mengevaluasi efek bentuk dan ukuran nosel pada viabilitas sel. Secara khusus, hasil kami menunjukkan bahwa sel yang diekstrusi melalui nosel tumpul, seperti nosel silinder yang umum digunakan dalam bioprinting 3D, menunjukkan viabilitas yang lebih rendah dibandingkan dengan sel yang diekstrusi melalui nosel meruncing (kerucut). Hal ini terkait dengan fakta bahwa bentuk nosel memengaruhi distribusi tegangan geser. Secara khusus, seperti dilaporkan dalam penelitian sebelumnya, 57 , 58 dalam kasus bioprinting 3D dengan nosel kerucut, tegangan geser menyebar ke area yang lebih luas dengan nilai maksimum yang lebih rendah. Akibatnya, sel-sel terkena gaya yang terdistribusi secara merata, mengurangi kematian sel. Demikian pula, laju aliran yang lebih tinggi dalam nosel besar menyebabkan peningkatan kecepatan aliran, yang menghasilkan tegangan geser maksimal yang lebih rendah. Dalam penelitian ini, kami menggunakan berbagai jenis sel untuk mengevaluasi efek ukuran dan bentuk nosel pada viabilitas sel. Kami awalnya menggunakan sel HEK-293T untuk mengevaluasi efek parameter bioprinting 3D pada viabilitas sel. Secara umum, sel HEK-293T menunjukkan perbanyakan cepat, pemeliharaan rendah, dan reproduktifitas tinggi. Namun, mereka memiliki beberapa kelemahan karena mereka tidak merangkum struktur dan fungsi sel yang berasal dari lokasi anatomi yang berbeda. 62 , 63 Untuk tujuan ini, kami memperluas penelitian kami untuk menyelidiki peran parameter pencetakan 3D pada sel NHAC-kn, garis sel spesifik yang berasal dari jaringan anulus fibrosus manusia pada diskus intervertebralis. 64 , 65 Mengevaluasi parameter biocetak 3D tersebut pada viabilitas sel NHAC-kn dapat berfungsi sebagai landasan untuk menghasilkan struktur cetak 3D spesifik jaringan, yang dapat digunakan sebagai strategi terapi potensial untuk regenerasi diskus.
Studi kami menunjukkan bahwa kedua populasi sel menunjukkan perilaku yang serupa, yang menunjukkan bahwa bentuk dan ukuran nosel mengendalikan viabilitas sel secara independen dari jenis sel. Namun, kecepatan cetak memengaruhi viabilitas sel NHAC-kn dan HEK-293T secara berbeda. Secara khusus, kecepatan cetak tidak berpengaruh pada viabilitas sel HEK-293T, sedangkan viabilitas sel NHAC-kn menurun secara signifikan pada kecepatan cetak yang lebih tinggi. Studi sebelumnya menunjukkan bahwa tidak hanya besarnya tegangan geser tetapi juga waktu pemaparan sel pada besaran tersebut menentukan tingkat kerusakan sel. 43 , 57 , 66 , 67 Sementara kecepatan cetak yang lebih tinggi meningkatkan tegangan geser, mereka juga mengurangi durasi pemaparan. Perbedaan sensitivitas tegangan antara kedua jenis sel dapat menunjukkan bahwa sel HEK-293T lebih sensitif terhadap durasi tegangan geser, sementara sel NHAC-kn lebih dipengaruhi oleh besarnya tegangan geser.
5 KESIMPULAN
Studi ini secara keseluruhan menilai dampak dari empat parameter bioprinting 3D utama – viskositas tinta, bentuk dan ukuran nosel, dan kecepatan cetak – pada kelangsungan hidup sel. Kami menunjukkan bahwa parameter ini menyebabkan kerusakan sel dan kematian sebagai akibat dari paparan tekanan geser. Kematian sel sangat bergantung pada sensitivitas sel terhadap besarnya dan durasi tekanan geser yang dialami, yang menunjukkan bahwa tekanan geser merupakan faktor utama yang perlu dipertimbangkan. 45 , 53 , 58 Pendekatan ini sangat penting untuk mengisolasi kontribusi setiap parameter dalam proses pencetakan, sehingga menghindari kompleksitas yang timbul dari beberapa parameter yang berinteraksi selama bioprinting 3D. Studi masa depan akan membahas efek multifaktorial dari parameter ini pada kelangsungan hidup sel selama proses bioprinting secara lebih komprehensif. Secara keseluruhan, penelitian kami mengevaluasi parameter ini dan menetapkan metodologi yang dapat membuka jalan bagi pembuatan perancah multiseluler cetak 3D dengan geometri kompleks, serta akan menjadi dasar bagi pendekatan pemodelan eksperimental dan prediktif di masa mendatang melalui pembelajaran mesin 68 untuk proses biocetak 3D, yang pada akhirnya memajukan perancah biocetak 3D untuk rekayasa dan regenerasi jaringan.
KONTRIBUSI PENULIS
Sophie Lipshutz: Konseptualisasi; investigasi; metodologi; validasi; analisis formal; perangkat lunak; penulisan – tinjauan dan penyuntingan; penulisan – draf asli; kurasi data. Yoontae Kim: Konseptualisasi; metodologi; validasi; analisis formal; perangkat lunak; kurasi data; penulisan – tinjauan dan penyuntingan. Micaila Curtis: Konseptualisasi; investigasi; metodologi; validasi; analisis formal; perangkat lunak; kurasi data. Leanne Friedrich: Konseptualisasi; penulisan – tinjauan dan penyuntingan; metodologi. Stella Alimperti: Konseptualisasi; investigasi; perolehan dana; penulisan – draf asli; penulisan – tinjauan dan penyuntingan; sumber daya; administrasi proyek; supervisi; metodologi; validasi; visualisasi; analisis formal; kurasi data.
UCAPAN TERIMA KASIH
Kami berterima kasih kepada Dr. Xiran Zhang atas bantuan dan dukungannya dalam studi karakterisasi reologi bionk yang dilakukan di Institute of Soft Matter. Peralatan, instrumen, atau material komersial tertentu diidentifikasi dalam makalah ini untuk menentukan prosedur eksperimen secara memadai. Identifikasi tersebut tidak dimaksudkan untuk menyiratkan rekomendasi atau dukungan oleh National Institute of Standards and Technology, juga tidak dimaksudkan untuk menyiratkan bahwa material atau peralatan yang diidentifikasi tentu merupakan yang terbaik yang tersedia.
INFORMASI PENDANAAN
Pekerjaan ini didukung, sebagian, oleh hibah dari National Institutes of Health (NIH) (R01DE031046 dan R21CA294025) dan oleh Georgetown University Startup Funds untuk Alimperti (Penerima: 91252) dan Toulmin Award.
PERNYATAAN KONFLIK KEPENTINGAN
Para penulis menyatakan bahwa mereka tidak memiliki benturan kepentingan.
