ABSTRAK
Pada gangguan neurometabolik yang dapat diobati, diagnosis dini dan inisiasi pengobatan yang cepat adalah kunci untuk meningkatkan kelangsungan hidup dan hasil. Varian biallelik pada SLC5A6 menyebabkan defisiensi multivitamin transporter yang bergantung pada natrium (OMIM # 618973), yang dapat diobati dengan asam pantotenat dosis tinggi, biotin, dan asam alfa lipoat. Sejauh ini, onsetnya terjadi setelah lahir pada semua pasien yang dilaporkan. Tinjauan pencitraan prenatal menunjukkan ventrikulomegali pada usia kehamilan 32 minggu. Setelah lahir, bayi tersebut menunjukkan regresi perkembangan. Pada usia 6 bulan, ia mengalami syok metabolik akut akibat infeksi saluran kemih. Analisis eksom cepat mengidentifikasi varian patogen heterozigot majemuk pada SLC5A6 dan mengonfirmasi diagnosis defisiensi multivitamin transporter yang bergantung pada natrium. Setelah bayi tersebut memulai pengobatan dengan biotin dosis tinggi dan asam pantotenat, kami mencatat peningkatan dramatis pada gejala hematologi, kulit, jantung, dan gastrointestinal. Meskipun bayi tersebut tidak menunjukkan regresi lebih lanjut, ia terus mengalami disabilitas psikomotor yang signifikan. Tinjauan atas temuan selama kehamilan menunjukkan bahwa bayi tersebut sudah mengalami pembesaran ventrikel pada akhir kehamilan, dan neuroimaging pada hari ke-12 kelahiran menunjukkan tanda-tanda kegagalan energi pada akhir kehamilan. Tinjauan kami terhadap pasien yang dilaporkan sebelumnya menunjukkan tidak ada korelasi genotipe-fenotipe yang jelas, tetapi terdapat sedikit variabilitas intrafamilial dalam timbulnya penyakit. Pengamatan saat ini, untuk pertama kalinya, memberikan bukti klinis tentang timbulnya defisiensi transporter multivitamin yang bergantung pada natrium pada janin. Risiko kekambuhan yang tinggi dan variabilitas intrafamilial yang rendah dalam timbulnya penyakit menunjukkan bahwa identifikasi dan perawatan prenatal pada kelompok berisiko tinggi mungkin penting.
1 Pendahuluan
Gangguan neurometabolik merupakan sekelompok gangguan genetik yang bermanifestasi dengan berbagai gejala neurologis. Di antara sekitar 1500 gangguan metabolik yang diketahui, terapi telah diidentifikasi untuk lebih dari 300 kondisi (Ferreira et al. 2021 ; Monaco et al. 2022 ). Defisiensi transporter multivitamin yang bergantung pada natrium (OMIM # 618973) merupakan gangguan neurometabolik prototipe yang disebabkan oleh varian kehilangan fungsi biallelik pada SLC5A6 (Subramanian et al. 2017 ). Transporter multivitamin dikodekan oleh SLC5A6 dan diekspresikan dalam sawar darah-otak dan saluran gastrointestinal. Ia memainkan peran penting dalam penyerapan nutrisi jejak yang penting untuk produksi energi dalam mitokondria di sistem saraf pusat (Uchida et al. 2015 ).
Aspek yang paling signifikan secara klinis dari kelainan neurometabolik ini adalah bahwa kelainan ini dapat diobati dengan asam pantotenat dosis tinggi, biotin, dan asam alfa-lipoat (Subramanian et al. 2017 ), yang menekankan pentingnya diagnosis dini dan permulaan pengobatan. Pada pasien yang dilaporkan sejauh ini, usia pada manifestasi pertama penyakit ini berkisar dari periode neonatal hingga dewasa muda (Byrne et al. 2019 ; Hauth et al. 2022 ; Holling et al. 2022 ; Mansour-Hendili et al. 2024 ; Montomoli et al. 2023 ; Rupasinghe and Onyeador 2023 ; Schwantje et al. 2019 ; Subramanian et al. 2017 ; Van Vyve et al. 2024 ). Strategi untuk diagnosis molekuler dini dan bukti untuk waktu intervensi terapeutik yang optimal masih ditunggu.
2 Laporan Klinis
Propositus diketahui memiliki ventrikulomegali pada usia kehamilan 32 minggu. Tidak ada riwayat keluarga dengan kelainan metabolik bawaan. Pasien lahir pada usia kehamilan 37 minggu sebagai anak ketiga dari orang tua non-konsanguinitas yang sehat. Saat lahir, berat badannya 2918 g (−1,0 SD), panjangnya 47,0 cm (−0,2 SD), dan lingkar kepala 36,5 cm (+2,2 SD). Skor Apgarnya adalah 7, 6, dan 9 pada menit ke-1, ke-5, dan ke-10, berturut-turut. Darah tali pusatnya menunjukkan pH 7,366. Ia hipotonik saat lahir dan memerlukan ventilasi mekanis selama 5 hari. Kadar piruvat dan laktat serum berada dalam batas normal. Pencitraan resonansi magnetik otak pada hari ke-12 setelah lahir menunjukkan kelainan sinyal yang luas pada substansia alba, mielinisasi yang tertunda, ventrikel lateral yang membesar, dan kista subependimal (Gambar 1 ). Hasil tes respons batang otak pendengaran otomatis normal. Setelah keluar dari rumah sakit, bayi menunjukkan kemunduran progresif dalam perkembangan psikomotorik. Meskipun ia mampu menyusu saat lahir, hal itu menjadi sulit setelah berusia 3 bulan, dan ia harus mulai diberi makan lewat selang. Respons terhadap cahaya dan suara menurun dan akhirnya menghilang.
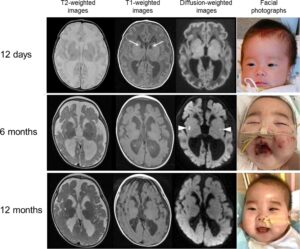
Pada usia 6 bulan, ia mengalami krisis metabolik akut dengan syok jantung akibat infeksi saluran kemih. Ia diresusitasi dengan perawatan medis maksimal dan diintubasi serta ditempatkan pada ventilasi mekanis di unit perawatan intensif. Hasil uji laboratorium dirangkum dalam Informasi Pendukung. Singkatnya, analisis gas darah vena menunjukkan asidosis metabolik berat dengan pH 7,053 (kisaran normal: 7,35–7,45), bikarbonat 4,8 mmol/L (kisaran normal: -2,3 hingga 2,7), dan kelebihan basa -24,1 mmol/L (kisaran normal: 22–26 mmol/L). Ekokardiografi menunjukkan hipertrofi ventrikel kiri dengan fraksi ejeksi berkurang sebesar 40% (kisaran normal > 60%). Uji laboratorium menunjukkan anemia berat dengan konsentrasi hemoglobin 5,5 g/dL, yang memerlukan transfusi sel darah merah berulang. Kadar piruvat dan laktat meningkat dalam serum dan cairan serebrospinal. Terdapat hiperamonemia, trombositopenia, anemia normositik, hipogamaglobulinemia, dan asidosis tubulus ginjal. Pencitraan resonansi magnetik otak menunjukkan hilangnya materi putih dan agenesis korpus kalosum, hipomielinasi, dan atrofi serebral global. Terdapat difusi terbatas bilateral pada aspek lateral putamen, yang mengingatkan pada tanda radiografi klasik penyakit mitokondria, termasuk ensefalopati Leigh. Spektroskopi resonansi magnetik menunjukkan tidak adanya puncak laktat dan rasio N-asetil aspartat terhadap kreatin yang rendah. Uji respons kondisi stabil pendengaran tidak menunjukkan kelainan pada kedua sisi.
Berdasarkan diagnosis dugaan penyakit mitokondria, pengobatan dimulai dengan suplementasi beberapa nutrisi dan vitamin (100 mg vitamin B1, 100 mg vitamin B2, 100 mg piridoksin, 1 mg B12, 1000 mg vitamin C, 100 mg vitamin E, 10 mg koenzim Q10, dan 150 mg/kg/hari l -karnitin), tanpa perbaikan klinis. Bayi tersebut juga menerima antibiotik dan imunoglobulin intravena untuk pneumonia aspirasi, selulitis, dan bakteremia Staphylococcus aureus yang resistan terhadap metisilin . Ia selanjutnya mengalami dermatitis dengan erosi di aksila, ekstremitas, bibir, rongga mulut, dan daerah perianal. Ruam memburuk meskipun pengobatan dengan steroid topikal dan antibiotik telah dimulai.
Sementara itu, pengurutan eksom berbasis trio dilakukan seperti yang dijelaskan sebelumnya [Takenouchi et al. 2015 ]. Analisis mengidentifikasi varian heterozigot majemuk dari SLC5A6 : NM_021095.4: c.1828 del, p.(Asp610ThrfsTer42) pada alel maternal, dan NM_021095.4: c.455A>C, p.(Gln152Pro) pada alel paternal. Kedua varian tersebut tidak teridentifikasi pada 3552 individu Jepang yang sehat (Tadaka et al. 2019 ) dan tidak dilaporkan dalam basis data genomik publik yang besar (Genome Aggregation Database; gnomAD, http://gnomad.broadinstitute.org/ ). Mengenai varian missense pada alel paternal, beberapa alat prediksi in silico menunjukkan patogenisitasnya: “merugikan” oleh SIFT (menyortir tidak toleran dari toleran) (Ng dan Henikoff 2003 ), “penyebab penyakit” oleh MutationTaster (Schwarz et al. 2010 ), skor phred Combined Annotation Dependent Depletion sebesar 24,6 (skor > 20 dianggap mewakili patogenisitas) (Kircher et al. 2014 ), dan skor PROVEAN sebesar -4,81 (skor ≤ -2,5 dianggap menunjukkan “merugikan”) (Choi dan Chan 2015 ). Menurut pedoman American College of Medical Genetics untuk interpretasi varian, varian tersebut diklasifikasikan sebagai “patogen” karena kriteria PVS1, PM2, dan PM3 terpenuhi (Richards et al. 2015 ).
Diagnosis molekuler defisiensi multivitamin transporter dependen natrium (OMIM# # 618973) dikonfirmasi pada hari ke-14 penerimaan. Berdasarkan hal ini, pada hari ke-20 penerimaan, bayi tersebut memulai pengobatan dengan 5 mg biotin dan 250 mg asam pantotenat. Dalam beberapa hari, ia menunjukkan perbaikan dramatis: ia menunjukkan resolusi lengkap dari ruam kulit, penyakit refluks gastroesofageal, disfungsi miokard, anemia dependen transfusi, dan asidosis laktat baik dalam darah maupun cairan serebrospinal. Setelah sebulan pengobatan, waktu terjaganya meningkat dan ia mulai tersenyum dan menangis (ia tidak responsif terhadap belaian dan menunjukkan sedikit ekspresi emosional sebelum pengobatan). Orangtuanya diberi konseling genetik mengenai risiko kekambuhan (25%) dari kelainan resesif autosomal ini.
Selama tindak lanjut jangka panjang, pasien terus menunjukkan perbaikan dalam perkembangan psikomotoriknya, tetapi masih tertunda secara signifikan. Pada usia 2 tahun 4 bulan, berat badannya 8920 g (−2,8 SD), panjang badan 74,6 cm (−4,6 SD), dan lingkar kepala 45,7 cm (−2,1 SD). Ia tidak mampu menjaga kepalanya tetap stabil atau berguling sendiri. Ia tetap diberi makan lewat selang karena disfagia. Tidak ada perbaikan pada atrofi optik bilateralnya. Ia tersenyum dan merespons suara, dengan gerakan anggota tubuh aktif terhadap rangsangan eksternal. Tidak ada kemunduran perkembangan setelah dimulainya pengobatan.
Sembilan bulan setelah dimulainya pengobatan (pada usia 12 bulan), pencitraan resonansi magnetik otaknya menunjukkan sisa hipomielinasi, tetapi tidak ada perkembangan atrofi serebral atau sinyal abnormal di ganglia basal (Gambar 1 ).
3 Diskusi
Di sini, kami mendokumentasikan perjalanan klinis dini yang terperinci dari seorang bayi dengan defisiensi multivitamin transporter yang bergantung pada natrium akibat varian biallelik pada SLC5A6 . Bayi tersebut mengalami syok metabolik akut dalam kondisi infeksi pada usia 6 bulan. Diagnosis molekuler yang cepat dan inisiasi biotin dosis tinggi dan asam pantotenat membalikkan banyak, jika tidak semua, gejalanya. Dalam retrospeksi, pasien sudah mengalami pembesaran ventrikel pada akhir kehamilan (32 minggu kehamilan), dan neuroimaging pada hari ke-12 setelah lahir menunjukkan tanda-tanda kegagalan energi pada tahap akhir kehamilan, yaitu, atrofi serebral global dengan defek pada ganglia basal. Pengamatan saat ini, untuk pertama kalinya, memberikan bukti klinis dari timbulnya defisiensi multivitamin transporter yang bergantung pada natrium pada janin.
Kami meninjau karakteristik klinis dan genetik dari pasien yang dilaporkan dengan defisiensi transporter multivitamin yang bergantung pada natrium karena mutasi biallelik pada SLC5A6 dan menyajikannya dalam bentuk tabel (Tabel 1 ). Gejala yang muncul sangat bervariasi, dengan pasien dengan onset dini di bawah usia 18 bulan yang datang dengan masalah akut, multisistem, dan nonspesifik. Membuat diagnosis klinis yang akurat dalam kelompok ini tampaknya sangat menantang; oleh karena itu diperlukan sekuensing genom dan eksom yang cepat. Mengenai usia saat onset, tidak ada korelasi genotipe-fenotipe yang jelas telah diamati, tetapi tampaknya ada sedikit variabilitas intrafamilial. Hal ini menunjukkan bahwa dalam kasus familial, identifikasi dan pencegahan yang ditargetkan pada kelompok berisiko tinggi mungkin memiliki signifikansi klinis yang besar.
| Kasus # | Usia saat timbulnya penyakit | Varian SLC5A6 | Gejala | DD/ID | Perlakuan | Tanggapan | Referensi |
|---|---|---|---|---|---|---|---|
| 1 | 1 bulan | R94X/R123L | G, H, M | Hadiah | Biotin, asam pantotenat, asam α-lipoat | Bagus | Subramanian dan kawan-kawan ( 2017 ) |
| 2 | 10 bulan | V141fs/Q622fs | G, C | Hadiah | Biotin, asam pantotenat | Bagus | Schwantje dan kawan-kawan ( 2019 ) |
| 3 | 14 bulan | V141fs/R400T | G, C, M | Hadiah | Tidak direkam | Meninggal pada usia 2 tahun 7 bulan | Byrne dan kawan-kawan ( 2019 ) |
| 4 | 12 bulan | G, H, M | Hadiah | Biotin, dexpanthenol, asam α-lipoat | Bagus | ||
| 5 sebuah | 13 tahun 6 bulan | S429G (homoseksual) | M | Absen | Biotin, asam pantotenat, asam lipoat | Bagus | Holling dan kawan-kawan ( 2022 ) |
| 6 sebuah | 10 tahun | M | Absen | Biotin, asam pantotenat, asam lipoat | Bagus | ||
| 7 sebuah | 6 tahun 9 bulan | M | Absen | Biotin, asam pantotenat, asam lipoat | Tidak berubah | ||
| 8 | 8 tahun 5 bulan | R94X/Y162C | C, Pria | Absen | Biotin, asam pantotenat, asam lipoat | Bagus | |
| 9 | 11 tahun | S429G (homoseksual) | M | Absen | Biotin, asam lipoat | Bagus | |
| 11 | 6 bulan | L566fs (homoseksual) | G, S, C | Hadiah | Tidak direkam | Meninggal pada usia 3 tahun | Montomoli dan kawan-kawan ( 2023 ) |
| 12 | 1 tahun | G, S, C, M, V | Hadiah | Biotin, asam pantotenat, asam lipoat | Tidak berubah | ||
| 13 | 1 tahun | G, H, S | Hadiah | Tidak direkam | Meninggal pada usia 1 tahun 5 bulan | ||
| 14 | 4 bulan | P437L (manusia) | G, H, C | Absen | Biotin, asam pantotenat | Bagus | Van Vyve dkk. ( 2024 ) |
| 15 | 1 tahun 1 bulan | L364V (homoseksual) | G, H, S, V | Hadiah | Biotin, dexpanthenol, asam α-lipoat | Bagus | Rupasinghe dan Onyeador ( 2023 ) |
| 16 | “Segera setelah lahir” | Q622fs/c.1005 + 1G>A | G, S | Absen | Biotin, asam pantotenat, asam lipoat | Bagus | Hauth dan kawan-kawan ( 2022 ) |
| 17 bulan | 4 tahun | sekitar 460-19T>G (homoseksual) | G, C, M, V | Hadiah | Tidak direkam | — | Mansour-Hendili dkk. ( 2024 ) |
| 18 bulan | 4 tahun | G, M, V | Hadiah | Biotin, asam pantotenat, asam lipoat | — | ||
| 19 | 4 tahun | G, M, V | Absen | Tidak direkam | Meninggal pada usia 7 tahun | ||
| 20 | 3 tahun | G, M, V | Absen | Biotin, asam pantotenat, asam lipoat | — | ||
| Pasien saat ini | Sebelum melahirkan | R610fs/Q152P | G, H, S, C, M, V | Hadiah | Biotin, asam pantotenat, karnitin, vitamin B1, B6, B12 | Bagus | Laporan saat ini |
Singkatan: C, masalah jantung; DD, keterlambatan perkembangan; G, gejala gastrointestinal; H, masalah hematologi; ID, cacat intelektual; M, gerakan abnormal; S, masalah kulit; V, gangguan penglihatan. a Saudara kandung. b Saudara kandung.
Dari sudut pandang pilihan terapi praktis, semakin diakui bahwa pada gangguan neurometabolik yang dapat muncul selama periode infantil, terapi pascanatal standar mungkin sudah terlambat dan perawatan prenatal mungkin diperlukan. Hal ini baru-baru ini diilustrasikan dengan baik dalam keluarga dengan penyakit Pompe dengan kematian berulang bahkan setelah pemberian terapi pascanatal standar. Inisiasi terapi penggantian enzim pada usia kehamilan 24 minggu dalam rahim melalui vena umbilikalis menghasilkan hasil yang baik (Cohen et al. 2022 ). Pengamatan saat ini bahwa propositus menunjukkan bukti prenatal cedera otak dapat membenarkan perawatan prenatal jika anak/janin berikutnya terpengaruh.
Sebagai kesimpulan, bayi dengan defisiensi multivitamin transporter yang bergantung pada natrium pada awal perkembangan janin merespons pemberian biotin dan asam pantotenat dosis tinggi pascanatal dengan keberhasilan yang terbatas. Mengingat risiko kekambuhan yang tinggi dan variabilitas intrafamilial yang rendah pada awal perkembangan penyakit, intervensi terapeutik prenatal mungkin perlu dipertimbangkan pada bayi berisiko tinggi.