ABSTRAK
Dalam 12 tahun sejak Dudgeon et al . (2006) meninjau tekanan utama pada ekosistem air tawar, krisis keanekaragaman hayati di danau, waduk, sungai, aliran air dan lahan basah dunia telah semakin dalam. Sementara danau, waduk dan sungai hanya menutupi 2,3% dari permukaan Bumi, ekosistem ini menampung setidaknya 9,5% dari spesies hewan yang dideskripsikan di Bumi. Lebih jauh lagi, dengan menggunakan Indeks Planet Hidup dari World Wide Fund for Nature, penurunan populasi air tawar (83% antara tahun 1970 dan 2014) terus melampaui penurunan kontemporer dalam sistem laut atau darat. Antroposen telah membawa banyak ancaman baru dan beragam yang secara tidak proporsional berdampak pada sistem air tawar. Kami mendokumentasikan 12 ancaman yang muncul terhadap keanekaragaman hayati air tawar yang sepenuhnya baru sejak 2006 atau telah meningkat sejak saat itu: ( i ) perubahan iklim; ( ii ) perdagangan elektronik dan invasi; ( iii ) penyakit menular; ( iv ) ledakan alga berbahaya; ( v ) perluasan pembangkit listrik tenaga air; ( vi ) munculnya kontaminan; ( vii ) rekayasa nanomaterial; ( viii ) polusi mikroplastik; (i x ) cahaya dan kebisingan; ( x ) salinitas air tawar; ( xi ) penurunan kalsium; dan ( xii ) stresor kumulatif. Efek dibuktikan untuk amfibi, ikan, invertebrata, mikroba, tanaman, kura-kura dan burung air, dengan potensi perubahan tingkat ekosistem melalui proses bawah-atas dan atas-bawah. Dalam masa depan kita yang sangat tidak pasti, efek bersih dari ancaman ini menimbulkan kekhawatiran serius bagi ekosistem air tawar. Namun, kami juga menyoroti peluang untuk keuntungan konservasi sebagai hasil dari alat manajemen baru (misalnya aliran lingkungan, DNA lingkungan) dan tindakan berorientasi konservasi tertentu (misalnya pemindahan bendungan, kebijakan perlindungan habitat, relokasi spesies yang dikelola) yang telah dipenuhi dengan berbagai tingkat keberhasilan. Ke depannya, kami menganjurkan pendekatan hibrida yang mengelola air tawar sebagai ekosistem penting untuk mendukung kehidupan manusia serta hotspot penting keanekaragaman hayati dan fungsi ekologi. Upaya untuk membalikkan tren global dalam degradasi air tawar sekarang bergantung pada penjembatani kesenjangan besar antara aspirasi ahli biologi konservasi dan laju percepatan kepunahan spesies.
I. PENDAHULUAN
Sudah lebih dari satu dekade sejak Dudgeon et al . ( 2006 ) menerbitkan tinjauan penting mereka tentang stresor ekologi yang bertanggung jawab atas penurunan keanekaragaman hayati air tawar global. Makalah berwibawa ini telah dikutip lebih dari 1800 kali, menempatkannya di antara 1% makalah yang paling banyak dikutip di bidang Biologi dan Biokimia (Web of Science®). Dudgeon et al . ( 2006 ) mengidentifikasi ‘eksploitasi berlebihan’, ‘polusi air’, ‘modifikasi aliran’, ‘perusakan atau degradasi habitat’ dan ‘invasi oleh spesies eksotis’ sebagai lima penyebab utama penurunan populasi dan pengurangan jangkauan organisme air tawar di seluruh dunia. Namun, selama dekade terakhir, dan saat kita maju ke zaman yang sekarang disebut sebagai ‘Antroposen’ (Crutzen, 2006 ), ancaman-ancaman ini telah meningkat dan/atau berkembang, dan ancaman-ancaman baru atau yang sebelumnya tidak dikenal telah menjadi lebih jelas. Skala hilangnya keanekaragaman hayati di perairan tawar saat ini begitu cepat sehingga kita menganggapnya sebagai tragedi tak kasat mata – tersembunyi di bawah permukaan air (Richter et al ., 1997 ) – yang kurang menarik perhatian publik, politik, atau ilmiah (Cooke et al ., 2016 ). Oleh karena itu, sudah saatnya untuk meninjau kembali pertanyaan: ancaman baru mana yang menimbulkan tantangan terbesar bagi konservasi keanekaragaman hayati air tawar, dan di mana peluang untuk melakukan intervensi?
Tinjauan umum ini mengidentifikasi ancaman-ancaman yang muncul ini dan memperbarui pengetahuan kita tentang tantangan-tantangan yang terus berlanjut terhadap konservasi air tawar, dengan memberikan perhatian khusus pada isu-isu yang mungkin memiliki efek global yang tidak diinginkan. Cakupannya meliputi: ( i ) ancaman yang diidentifikasi oleh pendapat ahli dan didukung oleh literatur primer; ( ii ) ancaman yang bervariasi dalam besaran, luas geografis dan/atau frekuensi di seluruh dunia; dan ( iii ) ancaman yang sepenuhnya baru sejak 2006 (lihat Bagian V.7 ), atau isu-isu yang diketahui sebelumnya dengan lintasan yang memerlukan pertimbangan baru (lihat Bagian V.9 ). Kami mulai dengan mendeskripsikan status keanekaragaman hayati air tawar global dan perubahan-perubahan yang diidentifikasi sejak Dudgeon et al . ( 2006 ). Dua belas ancaman yang muncul dibahas dan dicontohkan menggunakan berbagai kelompok taksonomi dengan contoh-contoh mitigasi yang disediakan jika memungkinkan. Kami menutup dengan diskusi tentang risiko dan manfaat dari berbagai alat konservasi, akhirnya mendeskripsikan area-area optimisme konservasi yang dapat berkontribusi pada Antroposen yang ‘baik’ (Bennett et al ., 2016 ) untuk keanekaragaman hayati air tawar.
II. KEANEKARAGAMAN HAYATI AIR TAWAR: KRISIS YANG SEMAKIN DALAM
Perairan tawar hanya mencakup 0,01% dari air di Bumi, dengan danau, waduk, dan sungai yang mencakup sekitar 2,3% (dan lahan basah air tawar mencakup sekitar 5,4–6,8%) dari luas permukaan daratan global, tidak termasuk lapisan es besar (Lehner & Döll, 2004 ). Inventarisasi global awal – Penilaian Keanekaragaman Hayati Hewan Air Tawar (FABA) (Balian et al ., 2008 ) – mengungkapkan bahwa ekosistem ini menampung hampir 9,5% spesies hewan yang dideskripsikan di Bumi, termasuk sepertiga vertebrata; ekosistem lahan basah yang sangat beragam hayati tidak termasuk dalam FABA. Meskipun area dan produksi total lingkungan laut jauh lebih besar, kekayaan spesies ikan laut dan air tawar (Actinopterygii) serupa (masing-masing 14736 dan 15149 spesies), dengan semua spesies air asin berasal dari nenek moyang air tawar (Carrete Vega & Wiens, 2012 ).
Yang mengkhawatirkan, indikator-indikator mengungkap penurunan populasi yang cepat dan risiko kepunahan yang besar pada organisme air tawar. Indeks Planet Hidup (LPI) World Wide Fund for Nature (WWF) (Collen et al ., 2009 ) mengungkapkan bahwa indeks untuk populasi spesies air tawar turun lebih tajam dari tahun 1970 hingga 2012 daripada indeks untuk populasi laut atau terestrial (lihat Gambar 1 ) (WWF, 2016 ). LPI untuk vertebrata air tawar telah menurun sebesar 81% (kisaran 68-89%) relatif terhadap penurunan indeks sebesar 38 dan 36% untuk daratan dan laut, masing-masing; pada tahun 2014, nilai ini untuk ekosistem air tawar telah meningkat menjadi 83% (WWF, 2018). Ini merupakan penurunan indeks tahunan sebesar 3,9% untuk populasi air tawar yang dipantau, yang mendekati empat kali lebih besar daripada populasi terestrial (1,1%). Dalam analisis ini, semua 881 spesies air tawar (dan 3324 populasi) yang digunakan untuk menghitung LPI adalah vertebrata, dengan bias taksonomi dan biogeografis yang dapat dideteksi di seluruh set data yang tersedia. Bagaimana tren LPI yang dilaporkan berhubungan dengan keanekaragaman hayati yang lebih luas sebagian besar masih belum diketahui (Collen et al ., 2009 ). Meskipun demikian, data lain, seperti Daftar Merah International Union for Conservation of Nature (IUCN), mengonfirmasi tingginya proporsi spesies yang terancam di antara vertebrata yang terkait dengan air tawar (Ricciardi & Rasmussen, 1999 ; Collen et al ., 2014 ). Misalnya, hampir 40% ikan air tawar Eropa dan Amerika Utara berisiko (Kottelat & Freyhof, 2007 ; Jelks et al ., 2008 ). Meskipun kurang tercatat secara komprehensif dibandingkan vertebrata, invertebrata air tawar juga bernasib lebih buruk dibandingkan dengan invertebrata darat (Taylor et al ., 2007 ; Clausnitzer et al ., 2009 ; Cumberlidge et al ., 2009 ).
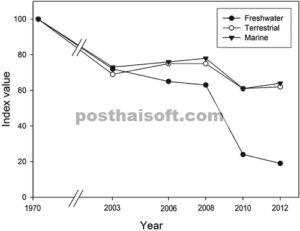
Living Planet Index (LPI) World Wide Fund for Nature (WWF) 2016 menunjukkan data tren populasi untuk ‘keranjang’ kolektif vertebrata di wilayah air tawar (lingkaran hitam), terestrial (lingkaran putih) dan laut (segitiga hitam), yang mengungkapkan penurunan indeks yang luar biasa di antara spesies air tawar. Penurunan indeks ini relatif terhadap nilai patokan 100 pada tahun 1970. Tanggal yang diberikan di sini merujuk pada tahun-tahun di mana estimasi kelimpahan dibuat, karena laporan LPI biasanya merujuk pada data dari empat tahun sebelumnya (misalnya LPI 2016 didasarkan pada data 2012). Nilai indeks 2012 sebesar 19 untuk populasi air tawar memiliki batas keyakinan berkisar antara 11 hingga 32; nilai 62 untuk populasi terestrial memiliki batas dari 49 hingga 79; dan nilai 64 untuk populasi laut memiliki batas dari 52 hingga 80 (WWF, 2016 ).
Meskipun banyak taksa air tawar mengalami lintasan menurun, literatur konservasi masih bias terhadap organisme terestrial, dengan kurang dari 20% makalah terbaru membahas spesies akuatik (Di Marco et al ., 2017 ). Ini bermasalah setidaknya karena tiga alasan. Pertama, indikator keanekaragaman hayati terestrial merupakan pengganti yang buruk untuk air tawar (Darwall et al ., 2011 ). Kedua, sementara beberapa solusi utama untuk masalah konservasi air tawar bergantung pada pengelolaan di antarmuka terestrial-air tawar (misalnya pengurangan limpasan pertanian), banyak upaya konservasi berbasis lahan untuk keanekaragaman hayati air tawar memerlukan implementasi pada rentang spasial yang luas di skala saluran, riparian, atau daerah tangkapan air (Darwall et al ., 2011 ). Misalnya, 84% rentang megafauna air tawar yang terancam berada di luar kawasan lindung yang ada (Carrizo et al ., 2017 ). Akhirnya, ekosistem air tawar merupakan titik-titik panas yang terancam punah sebagai akibat dari konvergensi antara kekayaan hayati dan berbagai bentuk eksploitasi air tawar manusia yang tidak hanya dihasilkan oleh tindakan berbasis daratan. Memproyeksikan isu-isu ini ke depan menunjukkan bahwa risiko kepunahan air tawar akan tetap tinggi selama beberapa dekade mendatang, terlepas dari tindakan yang diambil sekarang, karena ‘utang’ yang timbul dari populasi dengan viabilitas rendah yang sedang dalam proses menyusut menuju kepunahan (Strayer & Dudgeon, 2010 ). Tekanan antropogenik pada ekosistem air tawar juga tidak akan segera mereda, mengingat ancaman yang diulas di sini, khususnya rencana ambisius untuk pengembangan infrastruktur air secara global (lihat Bagian V.5 ) serta melalui perluasan tekanan populasi dan meningkatnya kebutuhan untuk penggunaan air domestik dan produksi pangan (Mekonnen & Hoekstra, 2016 ).
III. ANCAMAN YANG BERKELANJUTAN TERHADAP KEANEKARAGAMAN HAYATI AIR TAWAR
Degradasi habitat adalah penyebab utama dan terus-menerus dari penurunan populasi dalam sistem air tawar (Dudgeon et al ., 2006 ; WWF, 2018 ). Sementara ancaman ini ada di mana-mana sebagai risiko terhadap keanekaragaman hayati di hampir semua bioma dan tipe ekosistem air tawar di Bumi, kemungkinan akan bertambah atau diperburuk ketika ancaman baru muncul (lihat Bagian V.12 ). Misalnya, sementara polusi air sudah mapan dalam degradasi ekosistem air tawar (Cope, 1966 ), polutan dan proses yang terlibat berubah dengan cepat (lihat Bagian V.6 ). Permukaan bumi di bawah pengelolaan lahan dengan risiko polusi tinggi (misalnya zona perkotaan, lahan pertanian) meningkat seiring dengan bertambahnya populasi manusia global (Martinuzzi et al ., 2014 ).
Degradasi habitat melalui modifikasi aliran adalah ancaman persisten lainnya terhadap keanekaragaman hayati air tawar global (lihat Bagian V.5 ) (Dudgeon et al ., 2006 ). Ribuan bendungan direncanakan atau sedang dibangun di seluruh dunia (Zarfl et al ., 2015 ), dengan sedikit atau tanpa pertimbangan konsekuensi ekologisnya (Winemiller et al ., 2016 ). Ekosistem air tawar berisiko mengalami satu atau lebih efek yang telah dipelajari dengan baik dari modifikasi aliran yang disebabkan oleh bendungan (misalnya debit berkurang, migrasi ikan terganggu, konektivitas sungai-dataran banjir menurun) (Juracek, 2015 ). Selain itu, dengan mengurangi kelimpahan dan keanekaragaman hayati ikan, bendungan menimbulkan ancaman terhadap ekonomi berbasis ikan dan ketahanan pangan individu yang bergantung pada ikan (Orr et al ., 2012 ). Mereka juga dapat menciptakan atau memperburuk ancaman penyakit menular dengan meningkatkan peluang penularan parasit yang berhubungan dengan air (misalnya Steinmann et al ., 2006 ). Selain itu, perubahan iklim diperkirakan akan mengubah hidroklimat dan meningkatkan permukaan air laut (lihat Bagian V.1 ), dengan dampak sosial ekonomi dan ekologi yang berpotensi membahayakan manusia dan ekosistem di wilayah pesisir (lihat Bagian V.10).
Eksploitasi berlebihan organisme untuk konsumsi (terutama ikan, invertebrata air tertentu) adalah pendorong utama lain dari hilangnya keanekaragaman hayati air tawar (Dudgeon et al ., 2006 ; WWF, 2018 ; He et al ., 2017 ), yang telah lama diketahui (Allan et al ., 2005 ; Pikitch et al ., 2005 ) dan di beberapa daerah dibatasi (Buszkiewicz et al ., 2016 ). Eksploitasi berlebihan mencakup panen yang ditargetkan dan kematian melalui tangkapan sampingan. Meskipun pernah dianggap sebagai masalah utama perikanan laut (Alverson et al ., 1994 ), tangkapan sampingan juga memengaruhi berbagai taksa air tawar (Raby et al ., 2011 ). Meskipun besarnya dan luasnya eksploitasi lebih besar di sistem laut dibandingkan di perairan tawar (Arthington et al ., 2016 ), ada beberapa contoh utama di mana eksploitasi berlebihan terhadap ikan air tawar terus berlanjut sebagai ancaman air tawar yang berkelanjutan (lihat Dudgeon et al ., 2006 ).
Pendorong signifikan lainnya dari penurunan keanekaragaman hayati air tawar adalah spesies invasif dan penyakit (Dudgeon et al ., 2006 ; WWF, 2018 ). Dalam meta-analisis global dari 151 publikasi dan 733 kasus terpisah dari serangan spesies invasif dalam ekosistem perairan dari tahun 1994 hingga 2014, Gallardo et al . ( 2016 ) mendokumentasikan efek negatif yang kuat pada kelimpahan makrofita, zooplankton, dan ikan. Dalam dunia yang mengglobal di mana orang, material, dan informasi bergerak terus-menerus (lihat Bagian V.2 ), spesies invasif sangat mengancam dalam ekosistem air tawar. Mereka, seperti pulau-pulau, secara historis terisolasi tetapi semakin terhubung melalui tindakan manusia yang memfasilitasi penyebaran dan transportasi spesies invasif (Gherardi, 2007 ). Meningkatnya konektivitas juga memfasilitasi penularan patogen dan penyakit baru (lihat Bagian V.3 ), dengan implikasi bagi kesejahteraan manusia dan konservasi satwa liar.
IV. MEMPERKIRAKAN HAL-HAL YANG DAPAT DIPERKIRAKAN
Meskipun menantang, memprediksi dampak ancaman terhadap air tawar membantu identifikasi kesenjangan dalam pengetahuan dan kebijakan (Sutherland et al ., 2007 ), sambil mendorong pengambilan keputusan yang terinformasi. Dengan ‘meramalkan yang dapat diramalkan’, praktisi dapat memprioritaskan penelitian, merencanakan secara strategis, dan mengelola risiko untuk memungkinkan pengelolaan dan konservasi air tawar yang lebih baik. Sementara ada tinjauan ‘ancaman yang muncul’ untuk sistem terestrial (misalnya Estrada et al ., 2017 ) dan laut (misalnya Harvell et al ., 1999 ), tinjauan tersebut sering kali bersifat khusus habitat atau isu (misalnya Calmon et al ., 2011 ), dan kami tidak mengetahui adanya publikasi terbaru untuk keanekaragaman hayati air tawar. Oleh karena itu, sintesis stresor air tawar global ini dimaksudkan untuk membantu mengidentifikasi ancaman yang muncul dan menginformasikan prediksi, pengambilan keputusan pengelolaan, mitigasi, dan tindakan konservasi.
V. ANCAMAN YANG MUNCUL
Meskipun tidak menyeluruh, 12 ancaman yang mendesak dan muncul terhadap keanekaragaman hayati air tawar telah diidentifikasi berdasarkan pendapat para ahli dan literatur primer pendukung. Ancaman-ancaman ini bervariasi dalam hal jangkauan geografis, tingkat keparahan dampak, dan tingkat pemahaman (lihat Tabel 1 ).
Tabel 1. Karakteristik ancaman yang muncul terhadap keanekaragaman hayati air tawar: jangkauan geografisnya (dan wilayah fokus); tingkat keparahan dampaknya; contoh perubahan ekologis yang menyertainya; tingkat pemahaman kita; dan opsi potensial untuk mengurangi dampak ancaman. Untuk tingkat keparahan ancaman, kategorinya adalah parah (merah), sedang (kuning) atau tidak jelas (abu-abu) dan didasarkan pada hubungan dengan kepunahan spesies air tawar yang ditunjukkan dalam literatur. Tingkat pemahaman meliputi buruk (merah), cukup (kuning) atau baik (hijau) dan didasarkan pada kesenjangan pengetahuan yang teridentifikasi dan tantangan penelitian yang ada atau hal yang tidak diketahui. Referensi yang relevan disajikan di bagian ancaman yang sesuai (lihat Bagian V. )

(1) Perubahan iklim
Meskipun contoh kepunahan atau kerusakan spesies yang terkait dengan perubahan iklim masih jarang (Durance & Ormerod, 2007 , 2010 ), perubahan iklim berpotensi mengancam ∼50% spesies ikan air tawar global (Darwall & Freyhof, 2015 ). Respons ekologis terhadap pemanasan rata-rata hanya ∼1°C sudah tampak jelas. Dari 31 proses ekologi yang mendukung fungsi ekosistem air tawar dari gen hingga populasi, 23 telah dipengaruhi oleh perubahan iklim, termasuk pengurangan ukuran tubuh, pergeseran distribusi, perubahan fenologi, mekarnya alga dan desinkronisasi interaksi interspesifik (Scheffers et al ., 2016 ).
Ancaman air tawar yang terus-menerus akibat perubahan iklim meliputi peningkatan suhu air, perubahan debit, dan interaksi antara faktor-faktor tersebut dan pemicu stres lainnya (lihat Bagian V.12 ) (Ficke, Myrick & Hansen, 2007 ; Heino, Virkkala & Toivonen, 2009 ; IPCC, 2014 ). Meningkatnya suhu air tawar dapat mengubah distribusi spesies (Parmesan, 2006 ), wabah penyakit (Hermoso, 2017 ), fenologi (Krabbenhoft, Platania & Turner, 2014 ) dan kelangsungan hidup (Bassar et al ., 2016 ). Perubahan rezim aliran bervariasi secara geografis, namun variasi dalam presipitasi tahunan, peristiwa badai, banjir dan kekeringan diprediksi akan meningkat di Eropa utara, membahayakan moluska dan spesies lainnya (Hastie et al ., 2003 ), sementara di wilayah yang lebih kering seperti Australia, curah hujan dan aliran sungai diantisipasi akan menurun, mengancam burung air dan spesies lainnya (Pittock, Hansen & Abell, 2008 ).
Peristiwa ekstrem diantisipasi menjadi lebih umum (IPCC, 2014 ), dengan tingkat perubahan dan ketidakpastian melebihi apa yang dapat diakomodasi oleh evolusi spesies (Brook, Sodhi & Bradshaw, 2008 ; Loarie et al ., 2009 ). Selain pemanasan, penurunan cepat dalam suhu air (disebut ‘guncangan dingin’) mungkin juga terjadi di beberapa lokasi. Misalnya, peristiwa guncangan dingin 2010 di Bolivia menyebabkan kematian massal ikan di Amazon (Szekeres et al ., 2016 ). Saat ini, lebih dari setengah sungai di dunia dicirikan oleh peristiwa pengeringan berkala, tetapi peningkatan frekuensi dan intensitas kekeringan (Milly et al ., 2002 ) akan menyebabkan banyak sungai abadi beralih menjadi sungai intermiten (Datry, Fritz & Leigh, 2016 ). Sifat fisik dan kimia air tawar juga berubah, misalnya waktu pembentukan dan pemecahan es bergeser dalam skala global (Magnuson et al ., 2000 ). Perubahan stratifikasi danau kemungkinan akan memperbesar hipoksia hipolimnetik dan memengaruhi produktivitas danau (Kraemer et al ., 2015 ), membatasi ketersediaan habitat pelagis bagi banyak spesies (Ficke et al ., 2007 ). Meningkatnya suhu air dan konsentrasi CO2 diperkirakan akan lebih mendukung sianobakteri daripada alga eukariotik, sehingga sangat penting untuk membatasi masukan nutrisi guna mengurangi ledakan populasi yang berbahaya (Visser et al ., 2016 ) (lihat Bagian V.4 ).
Perubahan iklim juga diantisipasi akan memperkuat banyak masalah yang muncul yang diidentifikasi di sini [misalnya spesies invasif (Rahel & Olden, 2008 ), patogen (Marcogliese, 2008 ), eutrofikasi (Elliott, 2012 ), tenaga air (Knouft & Ficklin, 2017 ), salinitas (Henman & Poulter, 2008 ), meskipun dalam beberapa kasus dapat berfungsi untuk mengurangi ancaman tertentu]. Untuk mengantisipasi pergeseran curah hujan dan suhu, manusia selanjutnya mengubah rezim aliran dengan membangun bendungan dan proyek rekayasa ‘keras’ untuk melindungi dari banjir, meningkatkan penyimpanan air dan meningkatkan kapasitas irigasi (Palmer et al ., 2008 ). Komitmen pemerintah global untuk mengurangi emisi gas rumah kaca (GRK) (yang akan dibangun berdasarkan perjanjian Paris 2015), memperluas kawasan perlindungan air tawar (Pittock et al ., 2008 ) dan memulihkan habitat untuk menyediakan tempat perlindungan bagi adaptasi termal (Heino et al ., 2009 ) sangat penting untuk mengurangi dampak perubahan iklim terhadap keanekaragaman hayati air tawar.
(2) E-commerce dan invasi
Spesies invasif merupakan ancaman utama bagi keanekaragaman hayati air tawar, dan cara-cara pengenalan spesies dapat berkembang lebih jauh di masa mendatang (Rahel & Olden, 2008 ). Perdagangan global dan pergerakan organisme hidup yang terkait merupakan jalur utama invasi biologis yang sudah berlangsung lama (Levine & D’Antonio, 2003 ; Perrings et al ., 2005 ), tetapi vektor yang berkembang (mekanisme transportasi) dan rute perdagangan (jalur geografis antara wilayah sumber dan penerima) menimbulkan tantangan konservasi yang baru muncul. Secara khusus, lonjakan terkini dalam perdagangan elektronik global (e-commerce) yang terkait dengan penjualan spesies invasif baru melalui internet (misalnya Walters et al ., 2006 ; Humair et al ., 2015 ) dapat memperluas potensi hubungan di antara mitra dagang yang mapan dan yang baru muncul, seiring dengan perubahan dalam sikap masyarakat terhadap hewan peliharaan yang tidak biasa (Prokop & Randler, 2018 ) dan spesies non-asli (Humair, Kueffer & Siegrist, 2014 ). Toko ‘fisik’ besar dan kecil secara tradisional memainkan peran penting dalam perdagangan hewan peliharaan, akuarium, dan hortikultura (Reichard & White, 2001 ; Padilla & Williams, 2004 ), yang sering kali berpuncak pada pemilik hewan peliharaan yang melepaskan organisme yang tidak diinginkan ke badan air alami (Gertzen, Familiar & Leung, 2008 ). Menariknya, beberapa ikan yang paling populer dijual juga merupakan ikan yang paling mungkin tumbuh di alam liar (Duggan, Rixon & MacIsaac, 2006 ). Penghobi, kolektor, dan pembiak perorangan kini dapat dengan mudah berpartisipasi dalam pasar spesies di Internet (Tissot et al ., 2010 ). Kegiatan yang sebagian besar tidak diatur ini menantang manajemen, kebijakan, dan strategi pendidikan saat ini yang bertujuan untuk mengatasi jalur perdagangan ikan hidup (Strecker, Campbell & Olden, 2011 ).
Evaluasi terkini telah menyoroti peran penting e-commerce dalam perdagangan tumbuhan dan hewan non-asli. Gulma air dijual secara internasional melalui Internet di beberapa kawasan (Kay & Hoyle, 2001 ; Walters et al ., 2006 ; Martin & Coetzee, 2011 ), dan spesies tumbuhan yang lebih invasif daripada yang tidak invasif tersedia di situs web lelang daring utama (Humair et al ., 2015 ). Gambaran umum yang luas mengidentifikasi e-commerce sebagai kontributor signifikan terhadap risiko biosekuriti tingkat nasional (misalnya Parrott & Roy, 2009 ; Derraik & Phillips, 2010 ). Di kota-kota besar Brasil seperti São Paulo dan Rio de Janeiro, ikan non-asli dari Amazon, Australia, Asia Tenggara, dan Afrika dijual tanpa batasan yang jelas (Magalhães, 2015 ) . Perubahan lingkungan global juga dapat mengintensifkan dan menggeser rute geografis perdagangan e-commerce. ( 2012 ) menunjukkan bagaimana perubahan iklim dan pembatasan air dapat meningkatkan permintaan spesies hortikultura yang beradaptasi dengan lingkungan hangat dan kering. Hasil akhirnya adalah terciptanya cara penyebaran jarak jauh yang baru (Lenda et al ., 2014 ).
Mengelola risiko e-commerce merupakan tantangan. Rangkaian mekanisme untuk melakukan transaksi beragam, termasuk situs web ritel standar, situs lelang, bisnis lokal, iklan yang dicari, portal online, dan forum obrolan (NISC, 2012 ). Media sosial semakin memperumit lanskap, khususnya melalui ritel informal (Magalhães et al ., 2017 ). Perayap web telah digunakan untuk memantau Internet untuk penjualan hewan dan tumbuhan ilegal (Sonricker Hansen et al ., 2012 ); demikian pula, otoritas penegakan hukum dapat menggunakan alat-alat Internet seperti algoritma pembelajaran mesin untuk mengidentifikasi penjual spesies invasif yang dilarang (Di Minin et al ., 2018 ). Alat-alat lain yang berfokus pada akuntabilitas dapat berupaya untuk mendidik pembeli, misalnya dengan label peringatan online atau pop-up ketika spesies invasif akan dibeli. Meningkatkan penjangkauan dan pendidikan untuk meningkatkan kesadaran pembeli dan penjual tentang spesies invasif tetap menjadi yang terpenting.
(3) Penyakit menular
Air tawar sering kali menjadi fokus penularan patogen manusia dan satwa liar (Johnson & Paull, 2011 ; Okamura & Feist, 2011 ). Karena pentingnya air bagi kelangsungan hidup sebagian besar bentuk kehidupan, ekosistem air tawar sering kali berfungsi sebagai hotspot interaksi multispesies yang andal namun terkonsentrasi. Media akuatik juga memfasilitasi kelangsungan hidup banyak tahap infeksi parasit (dengan mencegah pengeringan) serta kemungkinan kontak dengan inang potensial, baik secara langsung maupun tidak langsung melalui konsumsi. Siklus hidup bifasik beberapa taksa air tawar (misalnya serangga akuatik, amfibi) juga menghubungkan infeksi lintas ekoton. Akibatnya, banyak mikroparasit (misalnya virus, jamur, protozoa, bakteri) dan makroparasit (misalnya cacing pipih, cacing gelang, cacing pita, artropoda) bergantung pada inang air tawar untuk penularan (Marcogliese, 2008 ; Johnson & Paull, 2011 ). Banyak penyakit menular baru merupakan spesies invasif, dan beberapa ditularkan oleh taksa non-asli.
Dalam beberapa kasus, infeksi dapat secara dramatis mempengaruhi keanekaragaman hayati air tawar. Penyakit yang diperkenalkan (misalnya wabah udang karang dan penyakit berputar salmonid), misalnya, telah menghancurkan taksa asli (misalnya udang karang Eropa dan salmonid Amerika Utara, masing-masing) (Hoffman, 1990 ; Holdich & Reeve, 1991 ). Penyebaran global chytridimycosis yang disebabkan oleh patogen jamur Batrachochytrium dendrobatidis (Bd) telah dikaitkan dengan pemusnahan atau kepunahan 200 spesies katak dan kodok (Rödder et al ., 2009 ). Chytrid invasif kedua yang baru-baru ini ditemukan ( B. salamandrivorans ) diperkirakan akan menjadi masalah yang sama bagi spesies salamander di Eropa dan Amerika Utara (Feldmeier et al ., 2016 ). Secara kolektif, epizootik ini memiliki efek tingkat komunitas dan ekosistem yang signifikan. Sebagai contoh, wabah udang karang secara tidak langsung meningkatkan populasi makrofita dan moluska (Alderman et al ., 1984 ), penyakit berputar menyebabkan perubahan pola makan pada beruang dan burung (Koel et al ., 2005 ), dan Bd mengubah pertumbuhan alga dan siklus nutrisi di sungai tropis (Whiles et al ., 2013 ).
Namun, kepentingan relatif penyakit menular dalam mengancam keanekaragaman hayati air tawar masih belum dipahami secara lengkap (Daszak, Cunningham & Hyatt, 2000 ). Johnson & Paull ( 2011 ) menyajikan bukti peningkatan kejadian penyakit terkait air pada amfibi, ikan air tawar, dan udang karang selama 40 tahun sebelumnya (1970–2009). Untuk amfibi, ada peningkatan lebih dari empat kali lipat dalam penelitian dan laporan terkait penyakit pada Bd, ranavirus, dan infeksi oleh cacing pipih, dengan infeksi ranavirus juga dikaitkan dengan kematian kura-kura (Johnson et al ., 2008 ). Ikan memiliki volume penelitian tertinggi dan keanekaragaman patogen terluas; infeksi virus seperti septikemia hemoragik virus dan anemia salmon menular telah menyebar dari lingkungan laut dan akuakultur, masing-masing (Murray, Smith & Stagg, 2002 ). Penyakit yang muncul, seperti penyakit ginjal proliferatif (PKD), mencerminkan suhu yang lebih hangat (Okamura et al ., 2011 ), dan pada tahun 2016, PKD menyebabkan matinya 10.000 ikan di Sungai Yellowstone setelah peristiwa pemanasan yang tidak biasa. Untuk udang karang, sindrom bintik putih dan penyakit porselen telah menyebabkan penurunan populasi, sering kali terkait dengan akuakultur, di samping efek wabah udang karang yang sedang berlangsung (Edgerton et al ., 2004 ).
Pemantauan penyakit sering kali memerlukan informasi lebih dari sekadar keberadaan atau kelimpahan parasit. Banyak laporan tentang infeksi air tawar yang muncul terkait dengan setidaknya satu spesies invasif, intensifikasi akuakultur, limpasan nutrisi dan polutan atau perubahan struktur jaring makanan (Daszak et al ., 2000 ; Johnson & Paull, 2011 ). Perubahan kebijakan dan pengawasan yang lebih baik telah dianjurkan untuk mengurangi kemungkinan masuknya patogen dan memaksimalkan peluang untuk pengendalian – dengan potensi yang cukup besar untuk menginformasikan manajemen penyakit manusia (misalnya malaria, schistosomiasis, giardiasis, demam West Nile) (Steinmann et al ., 2006 ). Jika infeksi melibatkan satwa liar dan inang manusia, atau memiliki kesamaan dalam pengendalian penularan, manajemen air tawar untuk membatasi eutrofikasi, mempertahankan tingkat trofik yang lebih tinggi (misalnya predator) dan mencegah spesies invasif dapat membantu mengatur infeksi di berbagai taksa inang.
(4) Mekarnya alga yang berbahaya
Alga air tawar menempati posisi trofik yang penting, menyediakan energi dan nutrisi untuk jaring makanan akuatik yang terhubung. Secara berkala, dan bisa dibilang lebih sering, spesies alga dipilih oleh kekuatan lingkungan (bawah ke atas) atau ekologi (atas ke bawah) yang memungkinkan akumulasi biomassa. Kondisi akumulasi biomassa spesies alga ini disebut bloom alga berbahaya (HAB). Sering dipandang sebagai organisme fisiologis sederhana, penyelidikan terhadap pembentukan HAB (D’Alelio et al ., 2016 ) mengungkapkan bahwa organisme ini dapat menempati sejumlah besar relung, dan relung ini terbuka untuk spesies asli yang berada dalam konsentrasi rendah di perairan alami serta untuk spesies invasif, dengan keduanya berkontribusi pada HAB.
Perubahan global telah meningkatkan peluang bagi spesies alga untuk menjadi lazim secara ekologis, berkontribusi pada peningkatan HAB baru-baru ini, dan mencakup pemanasan iklim (Elliott, 2012 ; Huisman et al ., 2018 ), intensifikasi hidrologi (di mana daerah kering menjadi lebih kering dan daerah basah menjadi lebih basah, dengan peningkatan frekuensi kejadian presipitasi intens bahkan di daerah di mana presipitasi menurun) (Huntington, 2006 ; Trenberth, 2011 ), eutrofikasi (Downing, 2014 ) dan brownifikasi (Kritzberg & Ekström, 2012 ). Perubahan fisik ini di permukaan air (misalnya suhu yang tinggi dan konstan) meningkatkan pertumbuhan alga yang berpotensi berbahaya (Paerl & Huisman, 2009 ), dan menyediakan stratifikasi kolom air yang diperlukan bagi prokariota fotosintetik untuk mendominasi dan mengekspresikan toksisitas (Burford et al ., 2016 ). Lebih jauh lagi, perubahan kimia di permukaan air dapat memilih spesies yang mampu mengeksploitasi matriks anorganik-organik yang diubah dari besi dan fosfor (Kritzberg & Ekström, 2012 ), yang secara signifikan mempengaruhi spesiasi alga dominan, distribusi dominasi produsen primer (pelagis versus bentik) dan kualitas air secara keseluruhan melalui produksi dan pelepasan racun terpilih (misalnya mikrokistin) (Ekvall et al ., 2013 ). Efek kumulatif dari perubahan global ini menghasilkan kompleksitas dan ketidakpastian yang lebih besar dalam kemampuan kita untuk memprediksi besarnya, frekuensi dan durasi kejadian HAB.
Setelah terbentuk, HAB mengancam keanekaragaman hayati air tawar. Beberapa mengakibatkan kematian ikan – baik secara tidak langsung dengan mengurangi ketersediaan oksigen terlarut, atau secara langsung melalui produksi toksin. Spesies bloom menciptakan kondisi fisiologis yang merugikan bagi pesaing mereka, mengubah aliran energi atau nutrisi melalui jaring makanan saat mereka menghasilkan senyawa alelopati atau toksik yang mengurangi pertumbuhan, kelangsungan hidup, dan reproduksi pada organisme lain atau mencemari jaring makanan. Misalnya, transfer trofik sianotoksin, kelompok toksin air tawar yang paling banyak dipelajari, ke konsumen sekunder dan tersier menyebabkan gangguan fisiologis dan perilaku (Ferrão-Filho & Kozlowsky-Suzuki, 2011 ). Manusia juga dapat terpapar sianotoksin melalui penghirupan toksin aerosol, konsumsi air danau atau konsumsi ikan (Caller et al ., 2009 ). Satu racun lingkungan yang telah memperoleh perhatian besar adalah asam amino β-N-methylamino-L-alanine (BMAA) (Brand et al ., 2010 ; Merel et al ., 2013 ). BMAA adalah neurotoksin yang telah diidentifikasi sebagai senyawa yang sedang berkembang karena perannya dalam penyakit neurodegeneratif (misalnya amiotrofik lateral sklerosis dan penyakit Alzheimer) (Banack et al ., 2015 ). Biosintesis BMAA dianggap sebagai sifat yang ada di mana-mana yang dimiliki oleh sebagian besar genus sianobakteri (Cox et al ., 2005 ) dan dapat terakumulasi dalam jaring makanan akuatik yang dipenuhi oleh sianoHAB (Brand et al ., 2010 ; Jiao et al ., 2014 ). Meskipun terdapat temuan ini, kurangnya protokol universal untuk mengukur BMAA dan ambiguitas seputar produksi BMAA oleh cyanobacteria menciptakan ketidakpastian besar seputar topik ini (Faassen, 2014 ).
Surveilans diperlukan untuk memantau kejadian penyakit terkait HAB (Backer et al ., 2015 ). Agenda penelitian nasional dan internasional yang terkoordinasi harus mengembangkan kebijakan dan sistem manajemen HAB yang efektif (Creed et al ., 2016 ). Langkah-langkah pencegahan mencakup satu atau beberapa hal berikut: mengurangi atau menghilangkan beban nutrisi eksternal (Paerl, Hall & Calandrino, 2011 ); mengangin-anginkan sedimen danau (Prepas et al ., 1997 ); atau secara kimia menangani sedimen danau untuk menekan daur ulang nutrisi internal (Molot et al ., 2014 ). Langkah-langkah mitigasi mencakup pengendalian kimia (misalnya algisida atau flokulan), pengendalian fisik (misalnya meningkatkan aliran untuk mengurangi waktu tinggal air dan menghilangkan sianobakteri) dan pengendalian biologis (misalnya memperkenalkan organisme yang mengonsumsi spesies HAB) (Rastogi, Madamwar & Incharoensakdi, 2015 ). Pada akhirnya, pengelolaan risiko HAB memerlukan analisis menyeluruh terhadap efektivitas dan kepatuhan seluruh sistem manajemen, termasuk pengendalian keras yang mencegah tekanan dan dampak, serta pengendalian lunak yang memungkinkan, memfasilitasi, atau melacak efektivitas pengendalian keras.
(5) Perluasan tenaga hidro
Hampir setengah (48%) dari volume sungai global diubah oleh regulasi aliran dan/atau fragmentasi (Grill et al ., 2015 ). Saat ini ada 3700 bendungan tenaga air utama yang direncanakan atau sedang dibangun, sebagian besar di negara-negara dengan ekonomi berkembang (Zarfl et al ., 2015 ; Winemiller et al ., 2016 ). Penyelesaian akan menyebabkan 93% dari semua volume sungai dipengaruhi oleh regulasi aliran dan/atau fragmentasi (Grill et al ., 2015 ), menambah efek akumulasi bendungan yang ada pada debit, suhu, zat terlarut, transportasi sedimen dan migrasi ikan (Reidy Liermann et al ., 2012 ; Pelicice, Pompeu & Agostinho, 2015 ). Konstruksi bendungan tenaga air membahayakan keanekaragaman hayati air tawar karena bendungan memodifikasi aliran alami dan rezim termal dan mengurangi konektivitas sungai-dataran banjir, produktivitas perairan dan akses ikan ke habitat pemijahan dan pembibitan (Freeman, Pringle & Jackson, 2007 ; Juracek, 2015 ). Bahkan ketika proyek tenaga air melibatkan struktur jalur ikan untuk meningkatkan pergerakan melalui bendungan, struktur seperti itu mungkin tidak efektif (Pompeu, Agostinho & Pelicice, 2012 ) atau bahkan berfungsi sebagai perangkap ekologi (Pelicice & Agostinho, 2008 ). Meskipun sudut pandang yang berkembang mengenai keberlanjutan pembangkit listrik tenaga air besar (LHP), telah terjadi peningkatan besar dalam dukungan untuk pengembangan pembangkit listrik tenaga air kecil (SHP) secara luas. Puluhan ribu SHP beroperasi atau sedang dibangun (11 SHP untuk setiap LHP) dan jumlah ini diperkirakan akan tiga kali lipat jika semua kapasitas pembangkitan potensial dikembangkan (Couto & Olden, 2018 ). Didorong oleh insentif politik dan ekonomi yang besar dalam beberapa dekade terakhir, pertumbuhan SHP telah jauh melampaui ilmu ekologi yang tersedia.
Kekhawatiran terkait yang utama adalah penuaan waduk. Ketidakseimbangan sedimen yang terkait dengan operasi bendungan dan masukan anak sungai menyebabkan waduk ‘menua’ melalui sedimentasi, erosi garis pantai, dan degradasi saluran setelah periode waktu (misalnya 50 tahun) yang bervariasi secara regional (Juracek, 2015 ). Sedimentasi memecah habitat perairan, merusak kesehatan dan kelangsungan hidup ikan, menurunkan produksi ikan, menurunkan produksi primer dan mengurangi kapasitas penyimpanan. Akses tepi air yang berubah merusak kemampuan waduk untuk mendukung kebutuhan manusia lainnya (misalnya pengendalian banjir, pasokan air, navigasi) (Chapman et al ., 2014 ; Juracek, 2015 ). Banyak bendungan sungai besar mencapai usia 50+ tahun karena dibangun pada pertengahan abad kedua puluh ketika kondisi politik dan ekonomi mendukung pembangunan bendungan (Avakyan & Iakovleva, 1998 ).
Panen ikan dan ketahanan pangan masyarakat yang bergantung pada sungai juga dapat terganggu oleh tenaga air, termasuk proyek-proyek yang diusulkan di sistem sungai besar seperti Amazon (Winemiller et al ., 2016 ) dan Mekong (Orr et al ., 2012 ; Ziv et al ., 2012 ) – cekungan dengan keanekaragaman hayati ikan yang tinggi yang secara historis memiliki tenaga air yang terbatas. Di Amazon, di mana sekarang terdapat 154 bendungan tenaga air besar, penyelesaian semua 277 bendungan yang diusulkan hanya akan menyisakan tiga anak sungai yang mengalir bebas dan dengan demikian mengancam keanekaragaman hayati ikan, ekonomi berbasis ikan, dan ketahanan pangan (Pelicice et al ., 2015 ). Mekong bagian bawah, perikanan tangkap pedalaman terbesar di dunia, juga terancam oleh pembangunan bendungan di sepanjang batang utama sungai (Ziv et al ., 2012 ; Winemiller et al ., 2016 ). Selain itu, membanjiri lahan untuk membuat waduk meningkatkan metilasi merkuri dan perpindahannya ke ikan, yang juga memengaruhi ketahanan pangan bagi masyarakat (Bodaly et al ., 2007 ). Waduk, terutama di daerah tropis dan subtropis, merupakan sumber utama emisi GRK (Deemer et al ., 2016 ) – tenaga air menawarkan sumber energi terbarukan tetapi tidak netral terhadap iklim.
Mengalihkan ketahanan pangan penduduk pedesaan dari protein akuatik ke protein yang berasal dari ternak dan berbasis daratan menghadirkan tantangan sosial ekonomi yang cukup besar, termasuk kebutuhan akan lahan dan air tambahan untuk operasi peternakan (Orr et al ., 2012 ). Interaksi potensial antara pengembangan tenaga air dan pemicu stres air tawar lainnya (misalnya perubahan iklim, perubahan tutupan lahan) (Hermoso, 2017 ), dan dampak terkait pada ekosistem dan populasi manusia, masih belum jelas. Saat ini, proyek tenaga air umumnya dinilai berdasarkan lokasi tertentu yang tidak memperhitungkan interaksi tersebut atau potensi tradeoff lingkungan-sosial ekonomi (Orr et al ., 2012 ; Winemiller et al ., 2016 ). Oleh karena itu, ada kebutuhan untuk penilaian tenaga air komprehensif yang mensintesis berbagai dampak potensial.
(6) Kontaminan yang muncul
Air permukaan menerima polusi dari pembuangan sumber titik seperti pertambangan, pertanian dan akuakultur, produksi pulp dan kertas, produksi minyak dan gas, dan limpasan perkotaan. Masing-masing dapat merusak keanekaragaman hayati air tawar secara tidak langsung melalui dampak pada habitat atau melalui toksisitas langsung. Namun, karena perjanjian lingkungan seperti Konvensi Stockholm (2001), produksi dan penggunaan bahan kimia global telah bergeser dari senyawa yang persisten, bioakumulatif, dan beracun, seperti insektisida diklorodifeniltrikloroetana (DDT), ke pestisida dan bahan kimia industri dengan waktu tinggal lingkungan yang lebih pendek dan toksisitas yang lebih rendah. Selain itu, dengan peningkatan pengolahan air limbah di seluruh sektor (misalnya limbah kota) (Holeton, Chambers & Grace, 2011 ), fokus di negara-negara maju kurang pada penanganan toksisitas akut (misalnya amonia) dan lebih pada penilaian dan mitigasi efek jangka panjang dari kontaminan lama dan kontaminan yang baru muncul. Yang terakhir adalah istilah yang luas dan mencakup semua yang mencakup zat-zat yang lebih baru atau kontaminan yang diketahui yang memiliki kekhawatiran yang lebih baru dan termasuk, tetapi tidak terbatas pada, bahan farmasi aktif, obat-obatan terlarang, aditif produk perawatan pribadi, pestisida yang lebih baru, pengganggu endokrin, nanomaterial (lihat Bagian V.7 ) dan mikroplastik (lihat Bagian V.8 ); semua telah menarik perhatian luas karena aktivitas biologis dan/atau stabilitas (atau pseudo-persistensi) yang tidak terduga atau tidak diketahui di lingkungan perairan. Sebagai contoh, survei sungai yang terkena dampak air limbah menunjukkan keberadaan global obat-obatan seperti antibiotik, antivirus dan antidepresan, dengan antibiotik menjadi yang paling sering terdeteksi (Hughes, Kay & Brown, 2013 ). Namun, efek dari senyawa-senyawa individual ini dan campurannya pada populasi dan komunitas perairan, serta fungsi ekosistem, masih kurang dipelajari.
Bahan kimia pengganggu endokrin dan, lebih khusus lagi, tiruan estrogen relatif dipahami dengan baik berkenaan dengan dampaknya pada beberapa spesies akuatik (Sumpter & Jobling, 2013 ). Di seluruh taksa, ikan paling rentan terhadap hormon alami dan sintetis yang terdapat dalam limbah kota, dengan dampak mulai dari produksi vitelogenin dan perkembangan interseks pada jantan (Jobling et al ., 2002 ) hingga berkurangnya kelimpahan (Kidd et al ., 2007 ). Baru-baru ini, dampak tingkat individu – khususnya interseks – telah dikaitkan dengan dampak transgenerasional pada keturunan (Schwindt et al ., 2014 ), berkurangnya kebugaran (Harris et al ., 2011 ) dan potensi penurunan keragaman genetik (Hamilton et al ., 2016 ). Meskipun bahan kimia ini berisiko rendah bagi taksa tingkat trofik yang lebih rendah, ada potensi efek yang dimediasi oleh jaring makanan pada konsumen primer melalui berkurangnya tekanan pemangsaan setelah penurunan kelimpahan ikan (Kidd et al ., 2014 ). Risiko yang menyertainya terhadap ekosistem belum jelas.
Senyawa antimikroba, termasuk antibiotik dan aditif produk perawatan pribadi, ditemukan dalam air limbah kota dan limpasan pertanian. Tidak mengherankan bahwa bahan kimia yang dirancang untuk membunuh mikroorganisme pada manusia juga akan memengaruhi komunitas mikroba alami (Barra Caracciolo, Topp & Grenni, 2015 ). Namun, tidak terduga bahwa kontaminan ini (misalnya triclosan) dapat memengaruhi keanekaragaman alga dan perifiton, serta beberapa konsumen primer (Nietch et al ., 2013 ). Studi yang lebih baru mengungkapkan efek kontaminan baru lainnya (misalnya antiinflamasi, antidepresan) pada komunitas alga (Bácsi et al ., 2016 ; Richmond et al ., 2016 ). Selain memengaruhi kelimpahan dan komposisi spesies, senyawa antimikroba juga dapat memengaruhi fungsi ekosistem akuatik (Nietch et al ., 2013 ), tetapi implikasi keanekaragaman hayati hilir masih bersifat spekulatif.
Mitigasi potensial kontaminan yang muncul mencakup penanganan lanjutan terhadap air limbah kota dan pengurangan sumber. Meskipun konsentrasi yang keluar terkadang dikurangi (misalnya asetaminofen, estrogen) dengan proses penanganan yang lebih maju – dan dengan manfaat selanjutnya di hilir (Hicks et al ., 2017 ) – beberapa kontaminan yang muncul (karbazepin, triklosan, dan diklofenak) lebih membandel dan memerlukan pengembangan intervensi baru (misalnya Bean et al ., 2016 ). Pengurangan sumber efektif dan diperlukan untuk beberapa kontaminan yang muncul mengingat kurangnya opsi penanganan, dan keuntungan sedang dibuat (misalnya mengurangi penggunaan antibiotik dalam produksi ternak dan mikrobead dalam kosmetik di beberapa yurisdiksi). Pengurangan dalam penggunaan farmasi manusia tidak mungkin terjadi, tetapi keuntungan hilir dan perlindungan keanekaragaman hayati yang lebih baik dapat terjadi melalui pembuangan obat-obatan yang tidak digunakan yang lebih baik dan pengolahan air limbah yang canggih.
(7) Nanomaterial hasil rekayasa
Nanomaterial rekayasa (ENM) adalah material buatan (rentang ukuran 1–100 nm) yang digunakan dalam banyak aplikasi industri, klinis, dan konsumen (Stone et al ., 2010 ). ENM memiliki rasio luas permukaan terhadap volume yang sangat tinggi dan sering kali menunjukkan sifat fisik dan kimia yang unik dibandingkan dengan material konvensional. Sementara karakteristik ini membuatnya diinginkan dalam banyak aplikasi (Lee, Mahendra & Alvarez, 2010 ; Tong et al ., 2014 ), mereka juga dapat membuat bioaktivitas ENM sulit diprediksi. Jumlah besar menemukan jalannya ke perairan tawar, tetapi keterbatasan analitis (von der Kammer et al ., 2012 ) berarti bahwa estimasi beban saat ini terutama didasarkan pada model (Gottschalk, Sun & Nowack, 2013 ; Sun et al ., 2014 ; Dale et al ., 2015 ). Di sungai, konsentrasi yang diprediksi untuk ENM umum berada dalam kisaran ng/l (atau lebih rendah), dengan beberapa formulasi mungkin mencapai μg/l (Gottschalk et al ., 2013 ). Banyak formulasi rentan terhadap agregasi dan presipitasi di perairan alami, yang berarti bahwa organisme epifauna dan infauna akan terpapar pada konsentrasi ENM yang besarnya lebih tinggi daripada spesies pelagis dalam sistem yang sama (Selck et al ., 2016 ). Perkiraan spesifik konsentrasi sedimen air tawar tidak tersedia, tetapi untuk air permukaan secara umum kemungkinan berada dalam kisaran μg/kg dan akan meningkat dengan pertumbuhan industri nanoteknologi yang berkelanjutan (Gottschalk et al ., 2013 ).
Beban lingkungan yang diprediksi umumnya jauh di bawah ambang batas toksisitas untuk ENM umum (Coll et al ., 2016 ), tetapi data pada spesies pelagis terlalu terwakili, sehingga risiko keseluruhan mungkin jauh lebih tinggi (Selck et al ., 2016 ). Tidak jarang untuk mengamati toksisitas akut minimal dari ENM murni (yaitu seperti yang diproduksi) pada ikan air tawar dan krustasea pada konsentrasi paparan yang realistis, tetapi sensitivitas dapat bervariasi berdasarkan urutan besarnya di seluruh spesies dan tahap kehidupan (Callaghan & MacCormack, 2017 ). Dengan ukuran sebagai pengklasifikasi utama, ENM dapat terdiri dari berbagai bahan organik, anorganik atau komposit, sehingga generalisasi tentang keamanan globalnya untuk organisme air tawar sulit dilakukan (Coll et al ., 2016 ).
Bahan inti sering ‘difungsionalisasikan’ dengan pelapis permukaan agar sesuai dengan aplikasi tertentu, dan mengubah pelapis ini dapat meningkatkan bioavailabilitas dan/atau bioaktivitas ENM hingga beberapa kali lipat (Osborne et al ., 2013 ). Banyak industri nanoteknologi yang sedang berkembang memanfaatkan ‘penyesuaian’ ini untuk menciptakan produk generasi berikutnya dengan potensi efek signifikan pada air tawar. Nano-farmasi adalah area pertumbuhan yang intens, dan pengenalan obat-obatan yang mendukung ENM atau sistem pengiriman obat ke dalam air tawar memerlukan pertimbangan yang cermat (Berkner, Schwirn & Voelker, 2016 ). Aplikasi pertanian, termasuk pupuk, herbisida, dan pestisida (Wang et al ., 2016 ), juga menjadi perhatian. Sementara peningkatan dalam penargetan dan kemanjuran atas bahan kimia konvensional dapat sangat mengurangi total massa produk yang diterapkan, peningkatan potensi dan sifat unik terkait ENM dari produk-produk ini dapat menimbulkan masalah baru setelah akhirnya mencapai air tawar. Misalnya, formulasi yang dirancang khusus untuk membawa agen bioaktif dapat meningkatkan ketersediaan dan toksisitas kontaminan lingkungan yang ada dengan bertindak sebagai ‘kuda Troya’ (Boncel et al ., 2015 ).
Sebuah hambatan utama untuk memahami risiko ENM yang muncul adalah kurangnya teknologi deteksi dan karakterisasi yang memadai (von der Kammer et al ., 2012 ; Coll et al ., 2016 ). Model saat ini memerlukan masukan yang lebih rinci untuk memperkirakan beban ENM secara akurat dan untuk memprediksi risiko pada ekosistem air tawar. Variasi dalam struktur ENM (misalnya bahan inti yang sama dengan lapisan yang berbeda) dan parameter utama seperti kimia air, pelapukan ENM, kinetika pelarutan dan agregasi dapat sangat memengaruhi nasib partikel dan bioaktivitas (Peijnenburg et al ., 2015 ) dan tidak diperhitungkan dalam model saat ini. Sebagian besar data bioaktivitas yang tersedia lagi-lagi berasal dari studi akut pada spesies pelagis, dan masih ada ketidakpastian yang cukup besar tentang risiko jangka panjang bahkan dari ENM yang paling umum (misalnya titanium dioksida, seng oksida, perak). Variabilitas tambahan dalam rentang sensitivitas yang dilaporkan dan tidak adanya tren dalam mekanisme toksisitas di seluruh taksa (Gottschalk et al ., 2013 ) menggarisbawahi perlunya kehati-hatian saat mengembangkan strategi untuk mengelola penggunaan dan pembuangan ENM baru.
(8) Polusi mikroplastik
Secara global, produksi plastik tahunan telah mencapai lebih dari 400 juta ton (Geyer, Jambeck & Law, 2017 ) untuk produk yang dirancang agar murah dan sekali pakai. Daripada terurai secara biologis, plastik dipecah oleh gaya mekanis dan radiasi ultraviolet (UV) menjadi fragmen yang lebih kecil (Barnes et al ., 2009 ) yang disebut ‘mikroplastik’ (partikel plastik <5 mm). Mikroplastik meliputi mikrobead (partikel yang ditambahkan ke kosmetik), nurdle (pelet kecil yang digunakan untuk memproduksi plastik lain), fragmen (bagian dari potongan yang lebih besar) dan serat mikro (dari pakaian sintetis) (Browne et al ., 2011 ). Di lingkungan laut, mikroplastik memiliki dampak lingkungan yang negatif, seperti kontaminan yang terkonsentrasi (Rios, Moore & Jones, 2007 ) dan konsumsi oleh hewan, yang mengurangi kebugaran dan meningkatkan mortalitas (Sigler, 2014 ; Provencher, Bond & Mallory, 2015 ). Meskipun data tentang konsentrasi mikroplastik air tawar terbatas, polusi mikroplastik di ekosistem air tawar sekarang sedang dilaporkan (diulas dalam Eerkes-Medrano, Thompson & Aldridge, 2015 ), termasuk Laurentian Great Lakes (Eriksen et al ., 2013 ), St. Lawrence (Castañeda et al ., 2014 ), Danube (Lechner et al ., 2014 ) dan sistem sungai lainnya yang membentuk saluran plastik antara daratan dan laut. Dalam beberapa tahun, konsentrasi mikroplastik di Sungai Danube dapat melebihi konsentrasi ikan larva planktonik (Lechner et al ., 2014 ). Polutan mikroplastik bervariasi di antara sistem air tawar, tetapi serat mikro sering kali mencakup >75% dari serpihan plastik (Ballent et al ., 2016 ; Vermaire et al ., 2017 ). Berasal dari pencucian pakaian sintetis (Browne et al ., 2011 ), pelepasan serat mikro ini sulit dikendalikan dalam pengolahan air limbah kota yang ada, tetapi filter pada mesin cuci dapat menjadi pilihan. Mikroplastik juga mengendap di sedimen perairan dan habitat dasar laut (Castañeda et al ., 2014 ; Ballent et al ., 2016 ; Vermaire et al ., 2017 ), sehingga mengekspos organisme dasar laut.
Mikroplastik dicerna oleh organisme air tawar termasuk burung (Holland, Mallory & Shutler, 2016 ), ikan (Campbell, Williamson & Hall, 2017 ), dan invertebrata (Windsor et al ., 2019 ). Ekstrapolasi dari temuan laut akan menunjukkan risiko yang muncul bagi organisme air tawar (Sigler, 2014 ; Provencher et al ., 2015 ). Pengelolaan polusi mikroplastik yang lebih baik di air tawar memerlukan pemahaman yang lebih jelas tentang: ( i ) sumber, tempat penampungan, dan aliran; ( ii ) faktor yang mengendalikan variasi spasio-temporal dalam konsentrasi mikroplastik; ( iii ) data tentang kontaminan yang diangkut bersama; dan ( iv ) rute penyerapan dan efek pada organisme air tawar (Wagner et al ., 2014 ). Undang-undang untuk mengendalikan mikroplastik telah diterapkan di beberapa negara (Amerika Serikat: Microbead-Free Waters Act, 2015 ; Kanada: Microbeads in Toiletries Regulations, 2016 ), tetapi ini biasanya hanya mewakili sebagian kecil dari total polusi plastik (Ballent et al ., 2016 ; Vermaire et al ., 2017 ). Karena produksi dan konsumsi plastik meningkat tanpa kontrol yang lebih baik, konsentrasi plastik di air tawar cenderung meningkat. Oleh karena itu, pemahaman yang lebih baik tentang nasib dan dampaknya menjadi prioritas. Singkatnya, ilmu yang mendukung mitigasi kontaminan yang muncul seperti mikroplastik dan ENM tertinggal dari farmasi dan produk perawatan pribadi. Penelitian lebih lanjut diperlukan untuk mengetahui dampak, jika ada, dari bahan-bahan ini terhadap ekosistem air tawar.
(9) Cahaya dan kebisingan
Peradaban kontemporer bergantung pada listrik dan mesin pembakaran – yang sering kali menjadi sumber cahaya (Longcore & Rich, 2004 ) dan kebisingan (Kight & Swaddle, 2011 ). Meskipun terdokumentasi dengan baik dalam sistem terestrial, sebagian besar penelitian akuatik berfokus pada kelautan dengan upaya yang relatif sedikit di perairan tawar meskipun jaringan jalan yang terang, pembangunan perkotaan, dan infrastruktur industri sering kali berlokasi di sepanjang sungai dan danau (Gaston et al ., 2014 ).
Polusi cahaya semakin dianggap sebagai pemicu stres yang berbahaya bagi keanekaragaman hayati air tawar (Hölker et al ., 2010 ). Studi awal mengungkapkan bahwa cahaya buatan mengubah migrasi vertikal diel dari zooplankton Daphnia (Moore et al ., 2000 ), yang berpotensi mengubah interaksi mereka dengan ikan. Baru-baru ini, Hölker et al . ( 2015 ) mengungkapkan bahwa bahkan komunitas mikroba dapat dipengaruhi oleh cahaya buatan di malam hari (ALAN), yang berpotensi mengubah sistem air tawar menjadi penyerap karbon nokturnal. Cahaya juga mengubah perilaku organisme yang sering kali sangat selaras dengan siklus sirkadian dan, misalnya, ALAN dapat memediasi interaksi antara udang karang sinyal invasif ( Pacifastacus leniusculus ) dan spesies asli (J. Thomas et al ., 2016a ). Untuk ikan, Foster et al . ( 2016 ) mengungkapkan bagaimana polusi cahaya meningkatkan pengeluaran energi dari ikan bass mulut kecil ( Micropterus dolomieu ) yang bersarang selama periode pengasuhan induk. Penerangan jalan juga menunda penyebaran pada ikan salmon Atlantik muda ( Salmo salar ), dan efek ini meningkat seiring dengan intensitas pencahayaan (Riley et al ., 2013 , 2015 ). Sementara sebagian besar penelitian difokuskan pada individu, potensi perubahan tingkat sistem terlihat jelas mengingat pentingnya cahaya sebagai isyarat untuk proses seperti pergerakan invertebrata dan makan oleh ikan yang mencari makan dengan cara hanyut.
Dampak kebisingan di air tawar pertama kali terungkap pada burung air yang terganggu oleh pesawat terbang dan perahu (Ortega, 2012 ), tetapi Zhang et al . ( 2013 ) kemudian menunjukkan bahwa kebisingan dari truk mengganggu burung sendok berwajah hitam ( Platalea minor ) yang terancam punah di lahan basah Sungai Pearl di Tiongkok. Kebisingan perahu motor dapat mengurangi tingkat berjemur di antara kura-kura air tawar (Jain-Schlaepfer et al ., 2017 ), menurunkan suhu tubuh dan memengaruhi asimilasi energi. Kebisingan lalu lintas dan pesawat terbang juga telah memengaruhi anuran (Tennessen, Parks & Langkilde, 2014 ), misalnya, menghambat kemampuan katak untuk berkomunikasi (misalnya mengubah frekuensi spektral yang digunakan dan frekuensi panggilan) selama perkembangbiakan (Kruger & Du Preez, 2016 ). Menariknya, Bleach et al . ( 2015 ) mengungkapkan bahwa kebisingan yang dihasilkan oleh kodok tebu invasif ( Rhinella marina ) menghambat perilaku memanggil katak asli Australia. Penelitian terbaru mengungkapkan bahwa kebisingan perahu meningkatkan hormon stres kortisol (Wysocki, Dittami & Ladich, 2006 ) dan meningkatkan pengeluaran metabolisme (Graham & Cooke, 2008 ) sekaligus mengurangi kinerja mencari makan (Purser & Radford, 2011 ) dan perilaku antipredator (Simpson, Purser & Radford, 2015 ) pada ikan air tawar. Bagaimana gangguan ini meningkat ke efek tingkat ekosistem tidak diketahui, meskipun kebisingan dapat mengubah bagaimana invertebrata penghuni sedimen memengaruhi sifat ekosistem (Solan et al ., 2016 ).
Untuk pengelolaan di masa mendatang, kami sarankan agar ada peluang untuk mengidentifikasi jenis cahaya, rezim pencahayaan, atau spektrum tertentu yang tidak terlalu merusak keanekaragaman hayati perairan. Pendidikan bagi masyarakat dan pemerintah daerah sebagai pengelola rezim pencahayaan (misalnya di jalan raya, dermaga, jembatan) juga akan membuahkan hasil. Mitigasi polusi suara mungkin paling baik dikembangkan untuk perahu dan telah mengambil bentuk pembatasan motor (misalnya zona tanpa motor pembakaran atau zona kecepatan) serta inovasi dalam desain motor yang mengurangi keluaran kebisingan. Namun, masih banyak yang harus dilakukan untuk mengurangi bentuk kebisingan lainnya.
(10) Salinisasi air tawar
Studi regional menunjukkan bahwa salinitas air tawar terjadi pada tingkat dan skala yang belum pernah terjadi sebelumnya (Herbert et al ., 2015 ), tetapi belum ada sintesis global dari masalah ini. Ancaman yang ditimbulkan oleh salinitas jauh dari baru, tetapi diperkirakan akan meningkat dengan perubahan iklim. Perkiraan menunjukkan bahwa 1,5 × 108 ha hutan dan lahan basah terkena garam di seluruh dunia (Wicke et al ., 2011 ), dan 1,5 × 107 ha lahan gambut air tawar rentan terhadap kenaikan permukaan laut (Henman & Poulter, 2008 ). Pembersihan vegetasi memungkinkan aksesi curah hujan yang lebih besar ke air tanah melalui zona pengisian ulang. Ketidakseimbangan ini meningkatkan tekanan hidrostatik di akuifer dataran rendah, meningkatkan pembuangan dari muka air tanah salin yang mendorong salinitas lahan kering. Zona semi-kering yang rentan terhadap salinisasi mungkin mengalami lebih sedikit curah hujan di bawah skenario pemanasan, mengurangi kenaikan muka air tanah, namun limpasan yang berkurang dapat menyebabkan peningkatan konsentrasi garam di air permukaan (Mills et al ., 2013 ). Salinisasi irigasi muncul dari penerapan langsung air ke lahan pertanian. Ini biasanya lebih asin daripada curah hujan, dan garam menguap bahkan dari penerapan air yang sangat encer, yang mengarah ke tanah permukaan yang asin. Di iklim yang lebih hangat dan kering, laju penguapan dapat meningkat dengan perubahan iklim, dan volume air yang lebih besar cenderung diterapkan untuk menghindari pengeringan tanaman (Vörösmarty et al ., 2010 ). Sementara teknologi yang muncul di bawah pertanian presisi dapat membuat penerapan air lebih efisien, populasi negara berkembang yang meningkat kemungkinan akan mengadopsi pertanian irigasi berteknologi rendah, memperluas tingkat air tawar yang berisiko.
Proliferasi bendungan besar di sungai-sungai besar (Zarfl et al ., 2015 ), serta ribuan bendungan kecil dan matriks padat titik air buatan di lanskap pertanian, berpadu untuk membatasi aliran limpasan air tawar ke zona pesisir. Aliran yang berkurang juga membatasi pengenceran dan pembilasan air pasang surut, meningkatkan salinitasnya. Banyak zona pesisir yang mengalami salinitas terancam oleh naiknya permukaan air laut yang kemungkinan akan menggenangi sistem dataran rendah (Henman & Poulter, 2008 ). Ini akan diperparah dengan meningkatnya eksploitasi sumber daya air tanah tawar dan meningkatnya frekuensi badai dan gelombang badai (misalnya Schuerch et al ., 2013 ). Penggerak antropogenik lainnya dari salinitas air tawar meliputi: pembuangan atau tumpahan air limbah salin yang tidak disengaja dari produksi gas lapisan batu bara dan minyak serpih (Vengosh et al ., 2014 ); penambangan terbuka pasir minyak yang mengekspos sedimen laut dan akuifer garam dangkal (Gibson et al ., 2013 ); dan meluasnya penggunaan garam untuk mencairkan es pada permukaan kedap air (Findlay & Kelly, 2011 ; Kaushal et al ., 2018 ).
Efek biologis dari salinisasi mencakup penggantian taksa yang tidak toleran terhadap garam secara terus-menerus dengan taksa yang dapat menahan konsentrasi yang lebih tinggi (Radke et al ., 2003 ). Peningkatan salinitas membunuh spesies air tawar karena kadar ion natrium dan klorida yang toksik dalam sel-selnya dan berkurangnya kapasitas untuk menyerap ion esensial dan air. Efek-efek ini dapat mengurangi keanekaragaman spesies dan secara signifikan mengubah sistem trofik dengan mengurangi sumber makanan bagi konsumen (Finlayson et al ., 2013 ). Sementara tanaman air tawar dapat menahan interval pendek peningkatan salinitas, periode yang berkelanjutan dapat menyebabkan berkurangnya produktivitas dan mengancam viabilitas rimpang dan benih yang disimpan. Salinisasi dapat menyebabkan stratifikasi kepadatan yang membuat sedimen permukaan menjadi anoksik, yang menyebabkan pergeseran rezim dalam komunitas tanaman air tawar (Davis, Sim & Chambers, 2010 ). Pertumbuhan, kesuburan, dan keanekaragaman invertebrata air tawar juga diketahui menurun dengan meningkatnya salinitas (Pinder et al ., 2005 ). Banyak vertebrata juga terkena dampak, sering kali melalui efek tidak langsung seperti perubahan habitat dan jaring makanan, namun anuran sangat sensitif, terutama pada tahap remaja (Smith et al ., 2007 ). Mitigasi salinisasi dapat mencakup pengendalian pelepasan garam dari sumber titik atau pemompaan akuifer ke muka air tanah yang lebih rendah, tetapi ini cenderung berskala lokal. Pelepasan aliran air tawar yang strategis dapat efektif pada skala yang lebih regional tetapi dapat menimbulkan biaya yang cukup besar, termasuk biaya tidak menggunakan air tersebut untuk tujuan lingkungan atau konsumsi (Herbert et al ., 2015 ).
(11) Penurunan kalsium
Sebagian besar ancaman lingkungan akuatik terkait dengan kelebihan nutrisi pembatas (yaitu eutrofikasi) atau kontaminan kimia yang melebihi konsentrasi aman. Sebaliknya, relatif sedikit stresor antropogenik yang terkait dengan berkurangnya pasokan nutrisi pembatas. Salah satu contoh ancaman yang baru-baru ini diidentifikasi adalah penurunan yang lambat tetapi meluas dalam konsentrasi kalsium (Ca) dalam sistem rendah karbonat di seluruh Amerika Utara bagian timur (Likens et al ., 1998 ; Keller, Dixit & Heneberry, 2001 ; Molot & Dillon, 2008 ), Eropa (Stoddard et al ., 1999 ; Skjelkvåle et al ., 2005 ; Hessen et al ., 2017 ), dan kemungkinan di tempat lain. Ca adalah nutrisi penting untuk semua bentuk kehidupan, tetapi konsekuensi ekologis dari ancaman baru ini masih belum sepenuhnya dipahami.
Meskipun debu kaya Ca mungkin berperan (Hedin et al ., 1994 ), sumber utama Ca untuk air tawar adalah pelapukan lambat batuan dasar induk yang memasok kumpulan Ca dalam tanah tangkapan, yang kemudian berpotensi tersedia untuk diekspor ke danau dan sungai. Bukti yang berkembang menunjukkan bahwa aktivitas manusia telah mengganggu siklus Ca di banyak danau air lunak, mengurangi pasokan Ca dan menurunkan konsentrasi Ca berair di bawah kebutuhan beberapa organisme akuatik melalui dua proses utama (Jeziorski & Smol, 2017 ). Pertama, hujan asam mempercepat pelindian Ca ke dalam danau, dan karenanya, untuk jangka waktu tertentu konsentrasi Ca air danau kemungkinan meningkat. Di daerah dengan geologi yang dicirikan oleh konsentrasi Ca tinggi (misalnya batuan dasar batu kapur), Ca terus mudah terlindi ke saluran air. Namun, di banyak daerah dengan Ca rendah, seperti yang dilapisi oleh batuan dasar granit Prakambrium, pasokan Ca akhirnya habis, karena pemeliharaan konsentrasi yang sesuai terutama bergantung pada proses pelapukan yang lambat. Kedua, karena sejumlah besar Ca terikat dalam kayu, praktik kehutanan dapat berperan sebagai ekspor bersih sebagian cadangan Ca di daerah aliran sungai, sehingga memperburuk hilangnya Ca di daerah aliran sungai (Allen, Clinton & Davis, 1997 ; Watmough, Aherne & Dillon, 2003 ).
Mengidentifikasi efek ekologis dari penurunan Ca jangka panjang, sejauh ini, terutama difokuskan pada Cladocera, sering kali merupakan kelompok invertebrata danau yang dominan dan penting. Analisis awal mengungkapkan bahwa beberapa cladocera berbadan besar (misalnya beberapa Daphnia spp.) memiliki kebutuhan Ca yang relatif tinggi (Jeziorski & Yan, 2006 ; Ashforth & Yan, 2008 ), dengan beberapa populasi tidak dapat bertahan hidup jika, misalnya, konsentrasi Ca ambien turun di bawah 1,5 mg/l. Mengingat bahwa program pemantauan telah mencatat konsentrasi Ca yang lebih rendah di banyak wilayah danau air lunak, muncul kekhawatiran bahwa ancaman lingkungan ini mungkin memengaruhi jaring makanan danau. Benang merahnya adalah bahwa penurunan Ca terjadi secara lambat dan bertahap, memerlukan data paleolimnologi (Jeziorski et al ., 2008 ) atau data pemantauan jangka panjang dalam orde beberapa dekade untuk mengidentifikasi masalah (Molot & Dillon, 2008 ). Atas alasan ini, Jeziorski et al . ( 2008 ) menggunakan analisis fosil Cladocera untuk menunjukkan bahwa, memang, pergeseran besar dalam kumpulan invertebrata dapat dikaitkan dengan menurunnya kadar Ca. Mereka menemukan bahwa banyak danau air lunak sudah menunjukkan tanda-tanda penipisan Ca dengan perubahan bersamaan dalam kumpulan cladocera. Lebih jauh lagi, data palaeolimnologi menunjukkan bahwa penurunan baru-baru ini dalam konsentrasi Ca yang tercatat dalam program pemantauan danau bukan hanya tren kadar Ca yang kembali ke tingkat sebelum pengasaman (seperti yang diharapkan dari konsentrasi Ca yang lebih tinggi di danau selama periode awal pengasaman danau), tetapi kadar Ca saat ini sekarang lebih rendah daripada konsentrasi sebelum pengasaman. Ahli palaeolimnologi mencapai kesimpulan ini karena taksa Daphnia yang sensitif terhadap Ca sering kali umum dalam catatan fosil sebelum pengasaman, yang menunjukkan bahwa kadar Ca cukup tinggi sebelum pengasaman. Penelitian selanjutnya mengkonfirmasi tren keseluruhan ini dalam spektrum ekosistem danau air lunak, yang mungkin juga memengaruhi kelompok biota air tawar lain yang memiliki kebutuhan Ca tinggi (diulas dalam Jeziorski & Smol, 2017 ), seperti udang karang (Hadley et al ., 2015 ).
Meskipun studi tentang penurunan Ca awalnya difokuskan pada taksa yang terdampak oleh berkurangnya ketersediaan Ca (misalnya Daphnia berbadan besar ), penelitian selanjutnya mulai berpusat pada organisme yang dapat memperoleh manfaat dari ancaman baru ini. Misalnya, mengingat Daphnia besar adalah penyaring makanan yang efisien, kematian mereka mungkin terkait dengan mekarnya alga baru-baru ini, karena berkurangnya efek atas-bawah (Korosi et al ., 2012 ). Selain itu, Jeziorski et al . ( 2015 ) mendokumentasikan penggantian Daphnia secara luas dengan Holopedium glacialis , pesaing berlapis jeli dengan kebutuhan Ca rendah. Meskipun keduanya adalah planktivora penyaring makanan, Holopedium memiliki kandungan nutrisi yang lebih rendah daripada Daphnia dan konsentrasi tinggi Holopedium berlapis jeli dapat mengganggu peralatan penyaringan air. ‘Pengjelifikasian danau’ yang terjadi kemudian adalah masalah baru yang berpotensi dapat menjalar melalui jaring makanan.
Solusi untuk ancaman penurunan Ca bukanlah solusi sederhana mengingat banyaknya danau yang terkena dampak dan lokasinya yang biasanya terpencil. Pengurangan lebih lanjut dalam presipitasi asam berpotensi menjadi solusi jangka panjang, meskipun memiliki dampak ekonomi yang signifikan. Dalam skala yang lebih kecil, beberapa upaya lokal telah dimulai untuk mengisi kembali Ca di daerah aliran sungai dengan, misalnya, ‘memupuknya’ dengan abu kayu yang kaya Ca (misalnya Haliburton, Ontario, Kanada). Kemanjuran proyek percontohan ini belum dievaluasi.
(12) Stresor kumulatif
Meskipun ada pengakuan yang sudah lama bahwa stresor lingkungan dapat berinteraksi untuk mempengaruhi ekosistem air tawar, dekade terakhir telah melihat pertumbuhan yang cukup besar dalam minat dalam masalah ‘stresor ganda’ yang potensial (Ormerod et al ., 2010 ; Vörösmarty et al ., 2010 ; Craig et al ., 2017 ). Yang pertama dari tiga alasan utama adalah meningkatnya perampasan sumber daya air tawar untuk penggunaan manusia ditambah dengan dampak hilir yang tumbuh dari aktivitas manusia (Strayer & Dudgeon, 2010 ). Kedua, dampak manusia pada air tawar sering terjadi dalam kombinasi, baik karena aktivitas yang berbeda bertepatan (misalnya urbanisasi dengan industri; pertanian dengan abstraksi; eksploitasi biomassa dengan pelepasan spesies invasif) atau karena mereka mempengaruhi ekosistem air tawar melalui beberapa jalur. Ketiga, perubahan iklim diperkirakan akan memiliki efek langsung dan tidak langsung yang luas pada air tawar (lihat Bagian V.1 ). Dalam bidang minat yang berkembang ini, ada tiga tantangan yang terkait dan menonjol.
Pertama adalah kebutuhan untuk menyelesaikan apakah beberapa stresor air tawar hanya terjadi bersamaan, atau apakah mereka memiliki efek yang berinteraksi. Bukti eksperimental awal menunjukkan bahwa beberapa kombinasi stresor bisa bersifat sinergis (misalnya suhu tinggi x stres toksik), tetapi dalam kebanyakan kasus kombinasi stresor kurang dari aditif (Folt et al ., 1999 ). Pola-pola ini sebagian besar telah didukung oleh meta-analisis baru-baru ini, di mana efek bersih dari stresor ganda pada keanekaragaman hayati dan fungsi ekosistem tampaknya dominan aditif dan antagonis, masing-masing (Jackson et al ., 2016a ). Data dari 88 makalah dan hampir 300 kombinasi stresor mengungkapkan interaksi yang paling umum adalah antagonis (41%), daripada sinergis (28%), aditif (16%) atau pembalikan (15%). Variasi di antara hasil ini menunjukkan perlunya memahami faktor kontekstual yang tepat yang memengaruhi interaksi stresor. Ekosistem atau organisme dengan kepentingan konservasi tinggi sering kali dicirikan oleh persyaratan khusus yang mungkin sangat sensitif terhadap beberapa kombinasi stresor. Lebih jauh lagi, erosi keanekaragaman hayati dapat meningkatkan dampak stresor ganda karena fungsi ekosistem terganggu atau sensitivitas berubah. Misalnya, Vinebrooke et al . ( 2004 ) menggambarkan bagaimana komposisi komunitas danau dapat mengurangi atau meningkatkan respons stresor gabungan tergantung pada sejauh mana spesies berbagi toleransi terhadap stres. Dalam beberapa kasus, efek stresor ganda pada air tawar telah menyebabkan ‘kejutan ekologis’ yang tidak terduga melalui interaksi non-linier atau tertunda dalam sistem yang sebelumnya dipahami dengan baik (Hecky et al ., 2010 ).
Tantangan kedua adalah mengembangkan metode untuk mendiagnosis kepentingan relatif stresor dengan efek kombinatorial. Penjelasan yang mungkin untuk dominasi interaksi antagonis adalah bahwa mereka yang berdampak besar mungkin menutupi atau mengesampingkan efek stresor yang lebih rendah (Jackson et al ., 2016a ). Dalam keadaan ini, menghilangkan stresor dominan mungkin hanya mengungkapkan efek stresor lain tanpa keuntungan keanekaragaman hayati bersih. Sebaliknya, mengidentifikasi efek hierarkis dari stresor yang terjadi bersamaan dapat membantu menargetkan pendekatan sekuensial untuk manajemen dan mengarah pada keuntungan keanekaragaman hayati yang nyata (Kelly et al ., 2017 ). Sejauh ini, bukti dan studi kasus yang dapat diandalkan untuk mengembangkan praktik terbaik yang dapat digeneralisasi terbatas, dan sering kali didasarkan pada pendekatan analisis data untuk kombinasi stresor yang berlaku yang mungkin tidak mewakili efek manajemen stresor sekuensial (Gieswein, Hering & Feld, 2017 ).
Terhadap latar belakang yang tidak pasti ini, tantangan ketiga adalah mengidentifikasi pendekatan pragmatis untuk mengelola berbagai dampak pemicu stres. Manfaat terbesar kemungkinan besar akan diperoleh jika solusi multiguna mengatasi berbagai masalah secara bersamaan – paling mudah dengan memprioritaskan perlindungan sumber daya daripada eksploitasi di daerah tangkapan air atau badan air yang diidentifikasi penting bagi keanekaragaman hayati (misalnya, Arahan Habitat UE 92/43/EEC; lihat Bagian VII ). Solusi daerah aliran sungai menawarkan alternatif berskala lebih kecil, misalnya, di mana ‘zona penyangga’ secara bersamaan memengaruhi kualitas air, melindungi rezim termal, menyediakan struktur habitat, dan mempertahankan subsidi energi, meskipun tidak sama efektifnya untuk semua polutan (Lowrance et al ., 1997 ). Namun, secara keseluruhan, ada kebutuhan mendesak untuk memahami dan mengatasi masalah berbagai pemicu stres, khususnya dampaknya terhadap keanekaragaman hayati air tawar.
VI. ALAT KONSERVASI DAN MANAJEMEN
Meskipun prognosis keseluruhannya suram untuk keanekaragaman hayati air tawar, ada peluang untuk tindakan konservasi dan pengelolaan yang efektif. Alat dan teknologi yang muncul (lihat Bagian VI.2 dan VI.2 ) akan sangat penting dalam mengurangi beberapa ancaman yang muncul (lihat Jackson et al ., 2016b ). Beberapa pendekatan yang ada (lihat Bagian (3) – (5) ) juga dapat membantu mendukung konservasi keanekaragaman hayati sambil memenuhi kebutuhan manusia; namun, ini telah dipenuhi dengan berbagai tingkat keberhasilan, namun menawarkan wawasan tentang efektivitas berbagai strategi konservasi air tawar. Di bagian ini, kami menyajikan daftar pendek alat dan teknik yang relevan dengan konservasi air tawar baik dalam penggunaan yang telah ditetapkan sebelumnya atau potensi penggunaan di masa mendatang, dan yang mencerminkan keahlian kelompok penulis.
(1) DNA Lingkungan
Asam deoksiribosa nukleat (DNA) dari organisme danau, lahan basah, dan sungai terdapat di kolom air sebagai sekresi, sel, jaringan, feses, atau gamet, dan diangkut melalui jaringan drainase. Fragmen DNA lingkungan ini (eDNA) dapat diisolasi dari bahan organik dalam sampel air, diurutkan, dan ditetapkan ke spesies yang diketahui menggunakan metabarkode (Elbrecht & Leese, 2017 ). Potensi aplikasi konservasi teknik eDNA sangat penting dalam mendeteksi spesies air tawar langka dan terancam punah yang keberadaannya tidak dapat dikonfirmasi dengan mudah melalui cara yang lebih konvensional (Jerde et al ., 2013 ; Laramie, Pilliod & Goldberg, 2015 ; Bellemain et al ., 2016 ), dan untuk memantau kolonisasi habitat baru oleh spesies atau patogen yang berpotensi invasif (Rees et al ., 2014 ). Surveilans yang ditargetkan atau ‘aktif’ yang diarahkan untuk mendeteksi eDNA untuk satu spesies yang diminati ini dapat dikontraskan dengan surveilans ‘pasif’, menggunakan sequencing throughput tinggi, di mana eDNA yang diambil sampelnya digunakan untuk menilai komposisi komunitas dan secara oportunistik mengungkapkan keberadaan spesies yang diminati (Simmons et al ., 2016 ). Pendekatan yang terakhir juga memiliki aplikasi potensial untuk bioassessment, karena sinyal eDNA dari komunitas makroinvertebrata dapat digunakan untuk memperkirakan keanekaragaman dengan investasi waktu dan upaya yang lebih sedikit daripada metode pengambilan sampel bentik yang digunakan secara luas saat ini (Rees et al ., 2014 ; Elbrecht & Leese, 2017 ). Aplikasi teknik eDNA yang lebih luas tentu tidak akan menjadi obat mujarab yang dapat menggantikan persyaratan untuk keahlian taksonomi tentang biota air tawar, juga pendekatan tersebut (belum) dapat memberikan informasi kuantitatif yang dapat diandalkan tentang ukuran populasi spesies yang diminati. Meskipun demikian, ketika dikombinasikan dengan metode pengurutan generasi berikutnya, pengumpulan eDNA yang diangkut dalam jaringan sungai menawarkan cara yang terintegrasi secara spasial untuk menilai kekayaan spesies (baik akuatik maupun terestrial) di seluruh daerah aliran sungai, dan dapat mengubah perolehan data keanekaragaman hayati di masa mendatang (Deiner et al ., 2016 ).
(2) Aliran lingkungan
Salah satu pendekatan untuk mengurangi dampak pengaturan aliran pada air tawar adalah praktik alokasi air (aliran lingkungan, atau e-flow) untuk melindungi atau memulihkan ekosistem. Konsensus ilmiah adalah bahwa e-flow harus menyediakan tingkat atau debit air yang meniru variabilitas hidrologi alami dan menggabungkan berbagai aliran yang penting untuk mendukung ekosistem yang berfungsi (Arthington et al ., 2018 ). Dengan memperhitungkan variabilitas hidrograf, e-flow memungkinkan keterhubungan secara longitudinal di sepanjang sungai dan secara lateral di dalam dataran banjir; hal ini penting dalam memungkinkan respons adaptif oleh biota sungai terhadap tantangan hidup di dunia yang lebih hangat, yang memungkinkan pergerakan di antara tempat perlindungan potensial saat kondisi berubah.
e-flows telah merangsang banyak penelitian ke dalam pertanyaan ‘berapa banyak air yang dibutuhkan sungai (atau aliran sungai, atau lahan basah)’? Alokasi air satu ukuran untuk semua untuk daerah aliran sungai secara teoritis dimungkinkan secara global (misalnya, 37% dari aliran tahunan rata-rata) (Pastor et al ., 2014 ), tetapi ‘aturan praktis’ seperti itu tidak mungkin untuk menangkap semua aspek variabilitas aliran yang penting secara ekologis. Sebaliknya, keberhasilan perlindungan dan pemulihan sungai akan bergantung pada pemodelan hubungan yang akurat antara pola hidrologi dan respons ekologis, diikuti oleh penerapan alokasi air dalam kisaran yang ditetapkan oleh ketahanan ekosistem ini (Poff & Zimmerman, 2010 ). Akumulasi data hidrologi jangka panjang diperlukan untuk mengevaluasi tren hidroklimat, untuk mengukur perubahan rezim aliran dan hubungan aliran-ekologi terkait, dan untuk merancang dan menerapkan resep e-flows; tren saat ini dalam cakupan data pengukur aliran di seluruh dunia tidak menggembirakan (Ruhi, Messager & Olden, 2018 ).
Konsensus luas telah muncul di antara praktisi e-flow tentang bagaimana hal ini dapat dicapai melalui pendekatan Batasan Ekologis Perubahan Hidrologi (ELOHA) untuk menentukan model hidro-ekologi dan alokasi air yang relevan secara regional (Poff et al ., 2010 ). Di banyak bagian dunia di mana data yang secara eksplisit menghubungkan perubahan hidrologi dengan respons ekologis langka, alokasi e-flow harus didasarkan pada data terbatas apa pun yang dapat digunakan untuk pendekatan ELOHA, dilengkapi dengan penilaian risiko dan penilaian profesional terbaik. Dalam keadaan seperti itu, alokasi e-flow dapat diperlakukan sebagai eksperimen yang digerakkan oleh hipotesis dalam restorasi ekologi, dengan hasil yang dipantau, dievaluasi, dan disempurnakan. Analisis hasil harus penting dalam setiap intervensi manajemen: meta-analisis oleh Palmer, Menninger & Bernhardt ( 2010 ) mengungkapkan kekurangan dalam pendekatan ‘jika Anda membangunnya, mereka akan datang’ yang banyak digunakan untuk memulihkan habitat fisik dan aliran di sungai jika stresor lain terus membatasi pemulihan ekologis. Kegagalan semacam itu sering terjadi karena banyak habitat air tawar yang rentan terhadap berbagai stresor yang saling berinteraksi (Craig et al ., 2017 ).
(3) Alien dan akuakultur
Spesies invasif telah menimbulkan efek yang sangat merusak pada ekosistem air tawar penerima (Gallardo et al ., 2016 ). Namun, tidak boleh diabaikan bahwa beberapa spesies non-asli sekarang dapat memainkan peran ekologis penting dalam lingkungan yang diubah manusia, seperti mendukung jaring makanan danau (Twardochleb & Olden, 2016 ) dan fungsi ekosistem sungai (Moore & Olden, 2017 ). Spesies telah berulang kali dan sengaja diperkenalkan di luar jangkauan asli mereka dengan tujuan untuk mendukung ketahanan pangan, peluang rekreasi dan rehabilitasi ekosistem. Ketika pelestarian lingkungan air tawar yang hampir murni tidak lagi menjadi pilihan yang realistis, prospek peningkatan layanan ekosistem melalui spesies asing yang diperkenalkan dapat menjadi pilihan – dan memiliki paralel yang jelas dalam pertanian terestrial. Mata pencaharian manusia merupakan pertimbangan utama di beberapa bagian Asia, Afrika dan Amerika Selatan, terlepas dari masalah konservasi, sedangkan kebutuhan untuk melindungi keanekaragaman hayati asli memiliki pengaruh yang lebih kuat pada keputusan di Amerika Utara dan Eropa, di mana ketergantungan pada perikanan artisanal air tawar umumnya lebih rendah. Beberapa pihak berpendapat bahwa spesies asing dapat, dalam keadaan tertentu (misalnya Gozlan, 2008 ), berkontribusi pada tujuan konservasi dengan menyediakan habitat atau melakukan fungsi ekosistem yang diinginkan (Schlaepfer, Sax & Olden, 2011 ). Bahkan penyerbu terkenal seperti kerang dreissenid dapat memberikan manfaat pengelolaan danau melalui aktivitas penyaringan dan pengendalian mekarnya alga (McLaughlan & Aldridge, 2013 ). Namun, yang lain sangat tidak setuju (Vitule et al ., 2012 ), dengan alasan bahwa risiko pengenalan alien lebih besar daripada peran bermanfaat apa pun yang mungkin mereka mainkan dalam meningkatkan layanan ekosistem. Misalnya, kerusakan ekologis dan ekonomi yang disebabkan oleh kerang dreissenid (Nakano & Strayer, 2014 ) tidak diimbangi oleh manfaat layanan penyaringan yang disediakan oleh hewan-hewan biofouling ini.
Penurunan global dalam perikanan tangkap air tawar (Youn et al ., 2014 ) akan meningkatkan kasus untuk memperluas akuakultur – yang sering kali didasarkan pada spesies yang diperkenalkan atau berpotensi invasif – untuk memenuhi kekurangan hasil panen liar untuk mendukung populasi manusia yang terus meningkat. Penurunan produksi alami ikan air tawar (relatif terhadap akuakultur) merupakan masalah yang sangat memprihatinkan mengingat hal itu menyediakan setara dengan semua protein hewani makanan untuk 158 juta orang, dengan populasi miskin dan kurang gizi yang sangat bergantung pada perikanan ini dibandingkan dengan sumber laut atau akuakultur (McIntyre, Reidy Liermann & Revenga, 2016 ). Hasil panen perikanan air tawar secara konsisten telah diremehkan (FAO, 2016 ; Fluet-Chouinard, Funge-Smith & McIntyre, 2018 ), dan kepentingan globalnya kurang dihargai (Lynch et al ., 2017 ; Reid et al ., 2017 ). Setidaknya 21 juta orang terlibat secara rutin dalam perikanan air tawar (lebih dari sepertiga dari total perikanan tangkap global) dan sebagian besar adalah operator skala kecil yang terkonsentrasi di Asia dan, kedua, Afrika (FAO, 2016 ). Lebih banyak lagi, khususnya perempuan, terlibat dalam penangkapan ikan untuk memenuhi kebutuhan hidup secara informal dengan hasil tangkapan yang berkontribusi pada kesejahteraan keluarga. Praktik semacam itu tidak dapat dengan mudah digantikan oleh akuakultur.
Akuakultur dapat menyebabkan berkembang biaknya parasit, penyakit, dan masuknya spesies baru, serta mencemari perairan penerima dengan limbah dan obat-obatan yang terkait dengan budidaya ikan intensif (FAO, 2016 ). Mengesampingkan kerugian ini, ikan budidaya mungkin bukan pengganti yang memadai untuk perikanan tangkap. Ikan liar lebih bergizi (kandungan protein dan mikronutrien lebih tinggi) daripada ikan yang dibudidayakan, bahkan dalam spesies yang sama (Youn et al ., 2014 ); dengan demikian, peralihan ke konsumsi ikan tersebut ketika tangkapan liar menurun (dengan asumsi bahwa itu dapat dilakukan) akan menghasilkan pola makan yang lebih buruk. Lebih jauh, kebetulan spasial antara perikanan air tawar produktif dan ketahanan pangan yang rendah (McIntyre et al ., 2016 ), serta antara tangkapan pedalaman per kapita dan kemiskinan ekstrem (Lynch et al ., 2017 ), menyoroti peran penting sungai dan danau dalam menyediakan protein dan mikronutrien bersumber lokal dan berbiaya rendah. Meskipun pengembangan akuakultur lebih lanjut dapat menggantikan sebagian kebutuhan pangan, akan jauh lebih baik untuk mengamankan penyediaan layanan ekosistem ini dengan melindungi perikanan ini dan habitat yang menopangnya, dengan hak mereka sendiri (Dudgeon, 2014 ), tetapi juga mengingat korelasi yang tampak antara keanekaragaman hayati dan perikanan yang stabil dan menghasilkan banyak hasil (Brooks et al ., 2016 ). Kebutuhan untuk memastikan bahwa perikanan tangkap air tawar sepenuhnya dipertimbangkan dalam keputusan tentang pengelolaan sumber daya air akan memerlukan kontribusinya terhadap ketahanan pangan yang dinilai, dihargai, dan dikomunikasikan dengan andal kepada para pengambil keputusan dan masyarakat.
(4) Pembongkaran saluran ikan dan bendungan
Penelitian tentang perangkat yang memungkinkan ikan untuk melintasi bendungan (di kedua arah) sangat dibutuhkan, karena banyak bendungan tidak memiliki fasilitas tersebut atau telah memasang struktur yang gagal untuk melewati spesies fokus – biasanya salmonid – atau komunitas ikan yang lebih luas (Pelicice et al ., 2015 ). Memang, beberapa ahli ekologi ikan yang disegani menganggap jalur ikan sebagai teknologi yang gagal yang tidak menyediakan jalur yang memadai – bahkan untuk spesies fokus – meskipun telah digunakan selama beberapa dekade (Brown et al ., 2013 ). Penilaian efektivitas berbagai desain dan jenis jalur ikan untuk memfasilitasi jalur bagi spesies ikan migrasi yang representatif sangat dibutuhkan, terutama di daerah tropis (Silva et al ., 2018 ). Penelitian yang ditargetkan tersebut dapat memberikan keuntungan konservasi karena hasilnya dapat diterapkan dengan mudah. Berbagai jenis aliran perlu dinilai untuk mengidentifikasi desain yang paling efektif untuk jalur ikan multispesies (misalnya Steffensen et al ., 2013 ; Yoon et al ., 2015 ), tetapi satu generalisasi yang jelas adalah bahwa, terlepas dari detail desain dan konteks ekologi, efektivitas jalur ikan berbanding terbalik dengan tinggi bendungan. Beberapa keberhasilan dalam membangun kembali migrasi ikan telah dilaporkan untuk ikan trout coklat ( Salmo trutta ) (Calles & Greenberg, 2009 ), salmon Atlantik (Nyqvist et al ., 2017 ) dan Macquarie perch ( Macquaria australasica ) (Broadhurst et al ., 2013 ) – namun hasilnya beragam untuk spesies lain meskipun ada penelitian yang ditargetkan untuk menginformasikan desain dan operasi jalur ikan (Baumgartner et al ., 2014 ).
Bahkan bagi spesies yang merespon dengan baik terhadap jalur ikan, struktur seperti itu tidak lebih dari solusi parsial terhadap hambatan yang ditimbulkan oleh bendungan, karena waduk yang terkait juga merupakan penghalang migrasi – terutama pada arah hilir (Pelicice et al ., 2015 ). Lebih jauh lagi, mereka melakukan sedikit atau tidak sama sekali untuk meringankan dampak bendungan dan waduk pada non-ikan, seperti udang migrasi (Holmquist, Schmidt-Gengenbach & Yoshioka, 1998 ). Satu-satunya solusi teknis yang diketahui adalah membuka atau menghapus bendungan sepenuhnya. Lebih dari 1200 bendungan telah dihapus di AS dalam 40 tahun terakhir, dan tingkat penghapusan dekade meningkat secara eksponensial (Bellmore et al ., 2016 ). Peristiwa seperti itu sering didorong oleh bahaya yang ditimbulkan oleh infrastruktur yang menua, tetapi dapat menghasilkan keuntungan konservasi di mana rute migrasi dibangun kembali. Bendungan yang lebih besar menjadi subjek perhatian, dengan yang terbesar adalah pemindahan Bendungan Glines Canyon (64 m tinggi) dari Sungai Elwah pada tahun 2014. Sungai merespons dengan cepat terhadap pemindahan bendungan, mengikis dan mendistribusikan kembali sedimen dan kembali ke kondisi sebelum bendungan dibendung dalam hitungan tahun, bukan dekade (O’Connor, Duda & Grant, 2015 ). Pemulihan ekologi lebih lambat tetapi tetap saja cukup cepat, dan salmonid dan ikan migrasi lainnya dengan mudah menjajah habitat yang baru tersedia di hulu (Grant & Lewis, 2015 ). Sementara tingkat pembangunan bendungan – terutama yang besar – jauh melampaui jumlah pemindahan (Bellmore et al ., 2016 ), praktik ini memiliki momentum: pada tahun 2016, pemerintah California dan Oregon mengumumkan rencana untuk menghapus empat bendungan pembangkit listrik tenaga air di Sungai Klamath sebagai bagian dari upaya untuk memulihkan perikanan salmon.
(5) Perubahan iklim dan relokasi spesies yang terkendali
Kecepatan perubahan iklim diperkirakan akan melampaui kemampuan banyak spesies air tawar untuk beradaptasi atau menyebar ke lingkungan yang lebih mendukung iklim (Brook et al ., 2008) .; Loarie et al., 2009). Conservation of these species may require managed relocation (also called assisted migration or assisted colonisation) of individuals to locations where the probability of their future persistence is likely to be high, but where the species is not known to have occurred previously (Olden et al., 2011). Yet, there is good reason to question whether managed relocation is a viable conservation strategy. For example, managed relocation promotes the distributional expansion of species and thus may have undesirable effects on other species or ecological processes (Ricciardi & Simberloff, 2009). Decisions regarding the managed relocation of freshwater species are clearly complicated. Quite simply, the effects of introducing a freshwater species to a new location are uncertain (and potentially disastrous), therefore the need for managed relocation must be balanced against the probability of species loss associated with doing nothing [see Olden et al., 2011 for discussion].
VII. IS THERE HOPE FOR CONSERVING FRESHWATER ECOSYSTEMS?
Current rates of extinction, habitat degradation and emerging challenges show that freshwater ecosystems already face pressures larger than any other ecosystem, and threats will intensify in future as the exploitation of freshwater resources grows to meet human demand. Conservation scientists working in freshwater ecosystems, therefore, have potentially important roles in providing evidence for actions to arrest decline, and to protect or restore the world’s lakes, reservoirs, rivers, streams and wetlands. Here we highlight positive actions that illustrate potential options across scales, from local to global. The mechanisms vary, but they include legal regulation, fiscal incentives, market opportunities and voluntary action by learned or civil society, or ideally some combination of these drivers.
In Europe, regulatory instruments range from aiming to achieve good qualitative and quantitative status of all water bodies (e.g. The Water Framework Directive 2000/60/EC) through to protecting specific freshwater ecosystems to support target taxa (e.g. The Habitats Directive 92/43/EEC), for which there is evidence of opportunity. For example, the European Union Urban Waste Water Treatment Directive (91/271/EEC) led to extensive and long-term ecosystem recovery in urban rivers that were once among the world’s most grossly polluted (Vaughan & Ormerod, 2012). Continental-scale regulation has also contributed to the recovery of formerly acidified lakes and rivers ranging from local (e.g. Sudbury, Ontario, Canada) to more extensive areas of Europe and North America – although in these cases biological responses have yet to match chemical trends fully (Kowalik et al., 2007; Ormerod & Durance, 2009; Labaj et al., 2015).
Fiscal incentives are sometimes used by governments to protect water courses in otherwise intensifying agricultural systems using agri-environment schemes (AESs). Examples include: riparian buffer zones to reduce nutrient flux; conservation easements in the USA; and various forms of catchment-sensitive farming with reduced agro-chemical use or livestock density. Although promising for some pollutants (Zhang et al., 2010), comprehensive data are needed to illustrate wider success in tackling multiple stressors sufficiently to engender whole-ecosystem recovery, including that of biodiversity.
Beyond government support, market mechanisms are increasingly considered as a means of managing freshwater catchments – specifically through natural capital accounting and markets for ecosystem services (Ormerod, 2014). The basic concept is to protect catchments as a ‘first line of defence’ or as units of production for natural services from which financial gains can then flow. Investments are typically made to protect soil carbon, maintain runoff, regulate water quality or provide natural flood management, thus providing a financial return, for example, in tradeable water supply, reduced water treatment costs or reduced need for traditional engineered infrastructure. Biodiversity is protected either collaterally, or because organisms have a key role in ecosystem-service delivery (Durance et al., 2016). Although this utilitarian view of natural systems is sometimes criticised, recognition of the role of freshwater ecosystems in human life support – as in the planetary health movement – may be an essential step towards their long-term protection. Key needs are to motivate investors, to move beyond small-scale demonstration projects and to ensure that conservation gains can be guaranteed to outweigh the risks of some resource exploitation implied in some forms of this paradigm.
Members of society and, in particular, non-governmental organisations (NGOs) act as important sources of lobbying, hope and demonstration in freshwater conservation. At a global scale, for example, the 2007 Brisbane Declaration at the Environmental Flows Conference, revised at the 2017 International River Symposium (see Arthington et al., 2018), emphasised the ecosystem-service role of fresh waters and called on governments, development banks, donors, river basin organisations, NGOs, community-based organisations, research institutions and the global private sector to take a range of actions to restore and maintain e-flows (Olden et al., 2014). The effectiveness of this call to action, however, remains to be assessed. Indeed, e-flow requirements have yet to be adequately assessed for most aquatic ecosystems and have been implemented in even fewer. There is still no comprehensive global record of e-flow implementations, nor a good understanding of why some projects have succeeded, while other initiatives have failed to materialise. Major obstacles to e-flow implementation lie largely outside the realm of ecology. They include a lack of political will and public support; constraints on resources, knowledge and local capacity; and institutional barriers and conflicts of interest (Arthington et al., 2018). These are matters of particular concern as a global boom in construction of hydropower dams is underway (Zarfl et al., 2015; Winemiller et al., 2016; Couto & Olden, 2018), and demands for water continue to grow, especially in arid regions, or those experiencing shortages as a result of climate change.
Civil society action has also been instrumental in dam removal – particularly in North America – to restore river systems through improved longitudinal connectivity. Over 1200 dams have now been removed, but evaluations of effects are still scarce or short-term, and there is thus a need for further post-intervention appraisal (Bellmore et al., 2016). In the UK, the NGO sector has been involved both in lobbying for improved river protection, but also in demonstrating practical steps in river conservation. One example is the concept of ‘Keeping Rivers Cool’ by restoring riparian woodlands. In the wake of climate change, the thermal benefits of improved riparian shading under summer conditions are clear, but advantages for native fish conservation, stream energetics and the reduction of sediment loads also appear likely (Lawrence et al., 2014; Wohl et al., 2015; S. Thomas, Griffiths & Ormerod, 2016b).
Potentially the biggest gains for freshwater conservation would arise when different sectors combine efforts. For instance, the new global initiative, the Alliance for Freshwater Life (Darwall et al., 2018), seeks to unite freshwater specialists, from individuals to organisations to governments, who engage in freshwater research, data synthesis, conservation, education and outreach as well as policymaking. Indeed, the global significance of freshwater ecosystems means that all stakeholders – ecosystem managers, policymakers, resource users, NGOs and citizens – should collaborate to make informed decisions that affect freshwater ecosystem viability and productivity. When the voices of inland fisheries professionals and citizens are heard in concert, fisheries success stories often ensue, as evidenced by ‘good news fisheries’ from walleye (Sander vitreus) in Red Lake, Minnesota, USA, to brown trout in Swedish rivers, among many others (Taylor et al., 2016). Moreover, attempts to engage the public through various forms of science communication and education (e.g. citizen science, participation in decision-making) have great potential to alter individual behaviour (e.g. how they vote, how they relate to water) and generate the political will necessary to protect and restore freshwater ecosystems (Cooke et al., 2013).
This short overview of potential actions indicates that there can be hope for the world’s freshwater ecosystems and their biota – but only if these examples inspire action at local, national and global scales in the face of overwhelming pressure. A potential roadmap for the future was outlined in the Rome Declaration (Taylor et al., 2016), which consists of 10 steps – ranging from biological and nutritional to social, economic and political – for responsible inland fisheries that, if followed, will address many emerging threats. However, beyond the sustainability of inland capture fisheries, there remains a lack of specific goals to achieve the conservation of freshwater biodiversity at large. For example, the 2015 United Nations (UN) Sustainable Development Goals (SDGs; see https://sustainabledevelopment.un.org/sdgs) include a goal dedicated to ‘life below water’ (SDG 14) that is concerned exclusively with the oceans, and the constituent targets say nothing about inland waters (Reid et al., 2017). We are in need of numerical targets that forcefully put the case for protecting freshwater ecosystems (e.g. Griggs et al., 2013). Such targets must: (i) treat the causes, not the symptoms, of freshwater biodiversity degradation; (ii) delineate how they are to be delivered, limiting their openness to interpretation; and (iii) include clear and feasible timelines, with short-, medium- and long-term objectives so they may be periodically reviewed and revised (e.g. 1983 management strategy for Lake Balaton, Hungary) (UNEP, 2017). We urge freshwater scientists to engage with the next phases of development of the UN Convention on Biological Diversity, and in particular the post-2020 follow-up to the Aichi Targets, to ensure that these most critically endangered ecosystems are given due prominence. On those actions, the future integrity of fresh waters and their denizens may well depend.
VIII. CONCLUSIONS
(1) In the 12 years since the major pressures responsible for global freshwater biodiversity loss were reviewed in Dudgeon et al. (2006), the prognosis for freshwater biodiversity has worsened, with freshwater species exhibiting steeper population declines (declining by 83% between 1970–2014) than their marine or land-based counterparts.
(2) Freshwater biodiversity continues to be under-represented in the conservation literature (Strayer & Dudgeon, 2010) despite estimates that fresh waters are hotspots of endangerment due to the convergence of disproportionately high biological richness and multiple anthropogenic pressures. Habitat degradation, overexploitation and invasive species – stressors all identified by Dudgeon et al. (2006) – continue to be persistent and ubiquitous threats to freshwater biodiversity with potentially harmful socio-economic effects on human welfare and wellbeing.
(3) Twelve emerging threats to freshwater biodiversity, that are either entirely new since 2006 or have since evolved and require renewed consideration, have been identified herein: (i) changing climates; (ii) e-commerce and invasions; (iii) infectious diseases; (iv) harmful algal blooms; (v) expanding hydropower; (vi) emerging contaminants; (vii) engineered nanomaterials; (viii) microplastic pollution; (ix) light and noise; (x) freshwater salinisation; (xi) declining calcium; and (xii) cumulative stressors. The Anthropocene has ushered in innumerable direct and indirect anthropogenic effects on diverse freshwater taxa, including amphibians, fishes, invertebrates, microbes, plants, turtles and waterbirds, and there exists strong potential for ecosystem-level changes through bottom-up and top-down responses.
(4) As topographically low and hydrologically connected ecosystems, freshwater lakes, reservoirs, rivers, streams and wetlands incur particular risk because chemical, physical, climatic and biological stressor effects can propagate and accumulate from the atmospheric, terrestrial and riparian environments in which fresh waters are embedded. Multiple-stressor problems are therefore a growth area for research. Projected future trajectories of human population growth, accelerating urbanisation, increasing irrigation, rising global temperatures and climatic unpredictability are likely to exacerbate human demands for fresh water while also impairing water quality to compromise ecosystems and threaten biodiversity further. There are clear signs that climate change has already directly impacted freshwater ecosystems and ecological processes, and ambitious water infrastructure projects, coupled with the uncertainties generated by climate change, will further alter fresh waters, posing challenges for human water and food security.
(5) To cope with the increasing pressures on water quantity and quality, decision-makers are primarily considering engineering solutions such as the implementation of environmental flows, as well the construction of fishways and the removal of dams. These solutions have been met with relative success, but are highly context dependent and require cautionary and targeted research approaches. Conversely, alien introductions, aquaculture and the managed relocation of species are techniques unlikely to support human wellbeing while maintaining healthy freshwater ecosystems due to the multiple implicit ecological risks.
(6) A desirable alternative is the effective protection of freshwater capture fisheries and the habitats that sustain them. This provides locally sourced, low-cost and nutritious protein in often impoverished areas while also promoting ecological integrity. Freshwater fisheries’ contribution to human food security must be reliably assessed, valued and communicated if it is to be included in resource-management decisions. At the same time, aquaculture is the fastest growing sector of the food-production industry, with potentially major consequences for freshwater biodiversity.
(7) Environmental DNA as a biomonitoring and bioassessment tool could augment biodiversity data acquisition in the future. It offers a promising potential remedy to the insufficient surveillance technologies and baseline-data deficiencies presented as common obstacles to emerging threat-mitigation efforts. Owing to the fact that fresh waters are subject to multiple pressures, however, any conservation tool or mitigation strategy that mitigates individual stressors will only be effective if co-occurring stressors are also alleviated.
(8) Positive conservation action has brought real and sustained benefits across scales, from local to global, via a variety of mechanisms including: regulatory instruments (e.g. The Water Framework Directive); fiscal incentives (e.g. agri-environment schemes); market opportunities (e.g. investments in ecosystem services with financial returns); and/or societal actions (e.g. dam removal, participation in restoration activities, considering freshwater ecosystems when voting in elections).
(9) We are merely at the beginning of the ‘great acceleration’ of the Anthropocene. Indeed, we may not even be able to imagine which environmental challenges we will face in the coming decades. In order to protect biodiversity and to support human well-being, we need to manage fresh waters collectively across sectors and as hybrid systems – managing freshwater ecosystems as both a pivotal resource for humans as well as highly valuable ecosystems.
(10) Upaya global, seperti yang digariskan oleh Alliance for Freshwater Life , 10 langkah untuk perikanan darat yang bertanggung jawab dalam Deklarasi Roma, dan tindak lanjut pasca-2020 terhadap Target Aichi, diperlukan untuk mengatasi dan membalikkan tren global dalam degradasi ekosistem air tawar, yang merugikan manusia dan alam. Namun, bagaimana kesenjangan antara tujuan mulia ini dan kondisi ekosistem air tawar saat ini serta pemanfaatan jasanya oleh manusia dapat ditutup dengan tantangan yang sangat besar namun perlu.
IX. UCAPAN TERIMA KASIH
Kami berterima kasih kepada kelompok Lab Ekologi Ikan dan Fisiologi Konservasi di Carleton University dan kelompok kerja internasional InFish ( infish.org ) atas diskusi dan umpan balik mereka yang bermanfaat pada konsep dan gambar makalah ini. Kami dengan tulus berterima kasih kepada para pengulas atas komentar yang membangun pada versi awal artikel ini. AJR, IFC, TJM dan SJC juga ingin mengucapkan terima kasih kepada Natural Sciences and Engineering Research Council of Canada (NSERC) atas pendanaannya. AKC dan WWT didukung oleh United States Department of Agriculture National Institute of Food and Agricultur. PTJJ mengucapkan terima kasih kepada David and Lucile Packard Foundation, National Science Foundation dan Niwot Ridge LTER Program. KAK didukung oleh Stephen A. Jarislowsky Foundation. SJO didanai oleh Natural Environment Research Council (NERC) Duress dan proyek-proyek EU MARS di bawah 7th Framework Programme. SJC juga mengucapkan terima kasih kepada pendanaan dari program Canada Research Chairs.
