Ringkasan
Metode infiltrasi vakum Agrobacterium memungkinkan transformasi Arabidopsis thaliana tanpa kultur jaringan tanaman atau regenerasi. Dalam penelitian ini, metode ini dievaluasi dan metode transformasi yang dimodifikasi secara substansial dikembangkan. Proses infiltrasi vakum yang padat karya dihilangkan demi pencelupan sederhana jaringan bunga yang sedang berkembang ke dalam larutan yang mengandung Agrobacterium tumefaciens , sukrosa 5%, dan 500 mikroliter per liter surfaktan Silwet L-77. Sukrosa dan surfaktan sangat penting untuk keberhasilan metode pencelupan bunga. Tanaman yang diinokulasi saat banyak kuncup bunga yang belum matang dan sedikit siliques hadir menghasilkan keturunan yang ditransformasikan pada tingkat tertinggi. Media kultur jaringan tanaman, hormon benzylamino purine, dan penyesuaian pH tidak diperlukan, dan Agrobacterium dapat diaplikasikan pada tanaman pada berbagai kepadatan sel. Aplikasi Agrobacterium yang berulang meningkatkan laju transformasi dan hasil keseluruhan transforman sekitar dua kali lipat. Menutupi tanaman selama 1 hari untuk mempertahankan kelembapan setelah inokulasi juga meningkatkan laju transformasi dua kali lipat. Beberapa ekotipe dapat ditransformasikan dengan metode ini. Metode yang dimodifikasi ini akan memfasilitasi transformasi Arabidopsis dengan hasil tinggi untuk berbagai upaya seperti penandaan gen T-DNA, kloning posisi, atau upaya penggantian gen yang ditargetkan.
Perkenalan
Teknologi transformasi tanaman menawarkan serangkaian peluang untuk penelitian ilmiah dasar dan untuk modifikasi tanaman pangan dan serat. Tanaman transgenik biasanya diproduksi dengan metode kompleks yang memerlukan persiapan sel atau jaringan tanaman secara cermat, pengenalan DNA menggunakan Agrobacterium tumefaciens atau pemboman partikel, pemilihan garis sel yang ditransformasikan, dan regenerasi tanaman ( Christou 1996 ; Hooykaas & Schilperoort 1992 ; Siemens & Schieder 1996 ; Weising et al . 1988 ). Metode transformasi ini memerlukan waktu, tenaga kerja terampil, dan fasilitas laboratorium yang relatif mahal. Sebaliknya, metode ‘ infiltrasi vakum Agrobacterium ‘ adalah prosedur yang relatif baru dan sederhana untuk transformasi Arabidopsis thaliana ( Bechtold et al . 1993 ). Dalam bentuk aslinya, metode ini melibatkan pertumbuhan Arabidopsis hingga tahap pembungaan, pencabutan tanaman, aplikasi Agrobacterium ke seluruh tanaman melalui infiltrasi vakum dalam media pertumbuhan sukrosa/hormon, penanaman kembali, pengumpulan benih beberapa minggu kemudian, dan identifikasi keturunan yang ditransformasi dengan seleksi pada media yang mengandung antibiotik atau herbisida ( Bechtold et al . 1993 ). Teknik ini, yang dapat dilihat sebagai perluasan dari metode transformasi in planta sebelumnya ( Chang et al . 1994 ; Feldmann & Marks 1987 ; Feldmann 1992 ; Katavic et al . 1994 ), menawarkan pengganti untuk metode transformasi Arabidopsis yang digunakan secara luas yang melibatkan kultur jaringan akar dan regenerasi tanaman (misalnya Valvekens et al . 1988 ). Dengan infiltrasi vakum dan metode transformasi in planta lainnya , sebagian besar keturunan yang ditransformasi secara genetik seragam (non-chimeric) dan variasi somaklonal yang terkait dengan kultur jaringan dan regenerasi diminimalkan. Keturunan yang ditransformasi biasanya bersifat hemizigot untuk transgen pada lokus tertentu, yang menunjukkan bahwa transformasi terjadi setelah divergensi garis keturunan sel antera dan ovarium ( Bechtold et al . 1993 ; Feldmann 1992 ). Oleh karena itu, target transformasi yang dapat diwariskan kemungkinan besar adalah jaringan gametofit-progenitor, gametofit dewasa, atau embrio yang baru saja dibuahi.
Alasan utama untuk popularitas metode infiltrasi vakum Agrobacterium adalah kesederhanaan dan keandalannya. Penghapusan kultur jaringan dan regenerasi sangat mengurangi waktu praktik langsung, dan keberhasilan dapat dicapai oleh non-ahli ( Bechtold et al . 1993 ; Bent & Clough 1998 ). Tanaman yang ditransformasi dapat diperoleh pada tingkat yang cukup tinggi sehingga prosedur tersebut dapat digunakan tidak hanya untuk memperkenalkan konstruksi gen spesifik ke dalam tanaman, tetapi juga sebagai metode mutagenesis acak untuk penandaan gen (misalnya Azpiroz-Leehan & Feldmann 1997 ; Hirsch et al . 1998 ; Koncz et al . 1989 ; Mollier et al . 1995 ; Richardson et al . 1998 ). Kelemahan utama dari metode ini adalah bahwa aplikasi yang berhasil hanya dilaporkan untuk satu spesies tanaman, Arabidopsis thaliana .
Untuk meningkatkan metode transformasi Arabidopsis yang sangat banyak digunakan ini dan untuk mendapatkan wawasan yang dapat memfasilitasi transformasi spesies tanaman lain, kami berusaha menguji sejumlah parameter yang terlibat dalam metode transformasi. Beberapa parameter ini juga telah disarankan dan dieksplorasi dalam studi yang tidak dipublikasikan oleh kami sendiri dan peneliti Arabidopsis lainnya (misalnya http://genome-www.stanford.edu/cgi-bin/biosciarabidopsis ). Laporan saat ini menawarkan protokol yang sangat disederhanakan yang merupakan produk dari studi yang terkontrol dan direplikasi. Komponen media infiltrasi telah dihilangkan, seperti halnya proses infiltrasi vakum yang melelahkan dan pencabutan dan penanaman kembali tanaman selama aplikasi Agrobacterium . Tahapan pertumbuhan tanaman telah diidentifikasi di mana jumlah transforman maksimal dapat diperoleh. Keahlian dengan metode DNA rekombinan masih diperlukan untuk menghasilkan konstruksi gen yang diinginkan, tetapi pengenalan konstruksi DNA yang stabil ke dalam genom Arabidopsis dimungkinkan dengan tenaga kerja, peralatan, atau reagen khusus yang minimal. Modifikasi ini mungkin paling penting untuk digunakan dalam proyek transformasi berskala lebih besar seperti penjebakan-peningkat dan bentuk lain dari mutagenesis penandaan gen, ‘pelengkapan shotgun terfokus’ selama tahap akhir proyek kloning posisional, atau upaya penggantian gen spesifik lokasi.
Hasil
Tahap pertumbuhan tanaman
Dari sekian banyak variabel yang hadir dalam protokol transformasi germ-line, salah satu yang terpenting adalah tahap perkembangan tanaman pada saat inokulasi dengan Agrobacterium . Meskipun sebelumnya telah ditunjukkan bahwa transformasi dapat terjadi ketika Agrobacterium diaplikasikan pada roset di lokasi baut inisiasi atau bahkan pada benih sebelum penanaman ( Chang et al . 1994 ; Feldmann & Marks 1987 ; Feldmann 1992 ; Katavic et al . 1994 ), transformasi frekuensi tinggi yang dapat direproduksi dicapai dengan andal pada tanaman di mana perbungaan telah berkembang dan kuncup bunga terlihat jelas ( Bechtold et al . 1993 ). Untuk mengidentifikasi tahap perkembangan perbungaan yang paling rentan terhadap transformasi, kami menggunakan infiltrasi vakum untuk menginokulasi tanaman yang berada pada tahap pertumbuhan yang berbeda: (A) baut primer terpotong, baut sekunder sekitar 1–5 cm (tidak ada bunga terbuka); (B) baut primer terpotong, baut sekunder sekitar 2–10 cm (sedikit bunga terbuka); (C) baut primer tidak terpotong, banyak bunga terbuka dan mulai menghasilkan siliques; dan (D) baut dewasa, banyak siliques sudah berkembang. Dalam enam dari tujuh replikasi, tingkat transformasi tertinggi secara keseluruhan dicapai dengan menggunakan tanaman dari kelompok B ( Gambar 1a ). Tanaman ini memiliki banyak kuncup bunga yang belum matang yang terlihat pada saat inokulasi. Dalam semua replikasi, tanaman dalam kelompok D adalah yang paling tidak rentan terhadap transformasi ( Gambar 1a ). Hasil serupa diperoleh dalam percobaan lain (lihat, misalnya, Gambar 3 ).
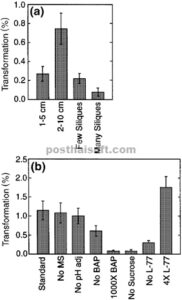
Pengaruh tahap perkembangan perbungaan dan komposisi media inokulasi terhadap laju transformasi.
Untuk setiap perlakuan, tiga atau lebih pot berisi 6–20 tanaman diinokulasi dalam vakum dengan suspensi bakteri pada OD 600 = 0,8. Nilai adalah rata-rata ± SE.
(a) Transformasi tanaman dengan tinggi/tahap perkembangan yang berbeda. (b) Pengaruh modifikasi media inokulasi terhadap laju transformasi (media inokulasi standar mengandung × media MS, pH 5,7, 44 nm BAP , 5% sukrosa, 0,005% Silwet L-77).
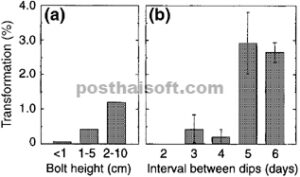
Pengaruh inokulasi celup berulang terhadap transformasi.
Inokulum terdiri dari 5% sukrosa, 0,05% Silwet L-77, dan bakteri yang disuspensikan hingga OD 600 = 0,8. Nilai-nilai tersebut adalah rata-rata ± SE.
(a) Tanaman yang dicelupkan hanya satu kali selama periode pertumbuhan yang sama dengan tanaman yang dicelupkan beberapa kali.
(b) Tanaman yang diinokulasi celup pada interval hari yang ditunjukkan selama periode 15 hari yang dimulai pada hari setelah perbungaan primer dipotong.
Bila beberapa pot Arabidopsis ditanam dan tumbuh bersama, tanaman berbunga dengan laju yang sedikit berbeda. Dalam semua percobaan berikutnya, pot tanaman dibagi menjadi kelompok perlakuan sehingga semua kelompok memiliki distribusi jenis tanaman yang sama. Meskipun demikian, variasi perkembangan dari pot ke pot dalam kelompok perlakuan mungkin merupakan faktor utama yang berkontribusi terhadap galat baku dalam perlakuan eksperimental dalam penelitian yang dilaporkan dalam karya ini. Sumber variasi kedua mungkin adalah tanaman untuk penelitian ini tumbuh dalam kondisi rumah kaca daripada di ruang tumbuh.
Konfirmasi protokol seleksi
Validitas metode seleksi pelat kanamisin yang digunakan untuk mendeteksi bibit keturunan yang ditransformasi dikonfirmasi oleh percobaan hibridisasi DNA. Fragmen DNA dari gen nptII di perbatasan daerah T-DNA pBINm-gfp5-ER ( Haseloff et al . 1997 ) digunakan untuk memeriksa bercak DNA genom yang dipisahkan secara elektroforesis dari tanaman yang resistan terhadap kanamisin atau kontrol yang sensitif terhadap kanamisin. DNA genom dibatasi dengan enzim Hin dIII untuk mengungkapkan fragmen sambungan yang melampaui T-DNA dan ke dalam DNA inang yang berdekatan atau ke dalam salinan ulangan T-DNA. Pita yang ukurannya berbeda dari fragmen Hin dIII hibridisasi dari pBINm-gfp5-ER asli diperoleh di semua dari 42 transforman putatif yang dipilih secara acak yang diperiksa, dan tidak ada pita hibridisasi yang diamati dalam DNA kontrol dari Arabidopsis yang tidak ditransformasi (data tidak ditampilkan). Selain itu, tidak ada tanaman yang resistan terhadap kanamisin secara spontan yang diamati di antara sekitar 3000 benih dari tanaman yang tidak diinokulasi yang ditanam pada media selektif sebagai kontrol dalam percobaan (total > 30.000 benih). Metode seleksi ini juga telah dikonfirmasi dalam penelitian lain (misalnya Bent et al . 1994 ).
Konstruksi pBINm-gfp5-ER yang digunakan dalam penelitian ini memberikan gen untuk protein fluoresensi hijau ke tanaman. Ekspresi fenotipe fluoresensi hijau diamati dengan jelas pada daun dewasa dari 17 dari 19 tanaman Col-0 yang resistan terhadap kanamisin, yang diduga telah ditransformasi dan diuji, dan tidak pada kontrol yang tidak ditransformasi. Berbagai tingkat fluoresensi diamati di antara berbagai transforman. Satu galur dibawa ke generasi T 6 melalui pembuahan sendiri, dan tanaman T 6 tersebut masih mengekspresikan fenotipe fluoresensi hijau.
Penyederhanaan media inokulasi
Dalam protokol sebelumnya untuk transformasi Arabidopsis dengan infiltrasi vakum Agrobacterium , sel Agrobacterium ditumbuhkan dalam medium kaya, dipanen dengan sentrifugasi, lalu disuspensikan dalam medium inokulasi yang pH-nya disesuaikan yang terdiri dari garam dan vitamin Murashige dan Skoog, benzylamino purine (BAP, suatu sitokinin), dan sukrosa ( Bechtold et al . 1993 ). Penggunaan surfaktan Silwet L-77 juga sudah umum. Kami meneliti kontribusi relatif dari komponen-komponen media ini terhadap keberhasilan transformasi menggunakan infiltrasi vakum. Gambar 1(b) menunjukkan bahwa tidak adanya medium MS tidak berpengaruh pada laju transformasi. Medium standar pH-nya disesuaikan menjadi 5,7, tetapi kami menemukan bahwa penyesuaian pH tidak diperlukan ( Gbr. 1b ). pH media kami biasanya di atas 6,0 sebelum penyesuaian pH, yang berada di luar kisaran optimal untuk induksi ekspresi gen Agrobacterium vir yang efektif ( Mantis & Winans 1992 ). Penghapusan BAP dari media inokulasi menyebabkan penurunan dua kali lipat dalam laju transformasi dalam satu percobaan, tetapi tidak memiliki efek signifikan dalam percobaan berikutnya ( Gbr. 1b dan data tidak ditampilkan). Menariknya, kelebihan BAP 1000 kali lipat (44 mm , tingkat yang umum untuk beberapa protokol transformasi tanaman lainnya), merugikan, memberikan laju 5-8 kali lebih rendah daripada tanpa BAP. Sukrosa ditemukan sebagai komponen penting dari media inokulasi. Penghapusan sukrosa mengakibatkan sedikit atau tidak ada transforman dalam sampel yang diuji sekitar 3000 benih per perlakuan ( Gbr. 1b ). Satu-satunya komponen penting lainnya dari media inokulasi adalah surfaktan. Dalam percobaan yang menggunakan vakum untuk membantu inokulasi, kurangnya surfaktan Silwet L-77 menyebabkan penurunan tiga hingga empat kali lipat dalam efisiensi transformasi, sedangkan peningkatan empat kali lipat dalam Silwet L-77 (hingga 0,02%) hampir menggandakan laju transformasi ( Gbr. 1b ). Dalam percobaan ringkasan yang dilakukan secara terpisah dari yang dilaporkan dalam Gambar 1(b) , media inokulasi yang hanya terdiri dari sukrosa dan surfaktan bekerja dengan baik seperti halnya media kompleks, yang memverifikasi bahwa keduanya merupakan satu-satunya komponen penting dari media inokulasi (rata-rata laju transformasi ± kesalahan standar sebesar 0,52% ± 0,19 untuk media yang disederhanakan dibandingkan dengan 0,50% ± 0,16 untuk media kompleks).
Vakum versus celupan bunga
Infiltrasi vakum digunakan untuk memperkenalkan bakteri ke dalam ruang antar sel dalam jaringan tanaman, tetapi alternatifnya adalah dengan hanya merendam bagian tanaman di atas tanah ke dalam larutan Agrobacterium selama beberapa detik, tanpa vakum. Kami menemukan bahwa penggunaan vakum tidak diperlukan untuk transformasi yang berhasil. Dalam percobaan awal, penggunaan surfaktan dalam jumlah rendah (0,005% Silwet L-77) memberikan laju transformasi untuk tanaman yang dicelupkan yang sebanding dengan yang diperoleh dengan infiltrasi vakum ( Tabel 1 ). Dalam percobaan kedua, laju transformasi dua kali lipat lebih rendah dengan perendaman dibandingkan dengan vakum ( Tabel 1 ). Dalam percobaan yang dilaporkan dalam Tabel 1 dan dalam percobaan lain, kami mencatat bahwa Silwet L-77 kurang penting untuk keberhasilan dengan infiltrasi vakum tetapi secara reproduktif meningkatkan keberhasilan transformasi dalam perawatan perendaman. Tahap pertumbuhan optimal untuk transformasi dengan perendaman bunga adalah ketika tanaman mengandung banyak kuncup bunga yang belum terbuka, mirip dengan yang dilaporkan dalam Gambar 1(a) . Metode celupan bunga membutuhkan waktu dan upaya yang jauh lebih sedikit daripada infiltrasi vakum, dan menghasilkan hasil benih yang lebih besar (data tidak ditampilkan), sehingga percobaan selanjutnya difokuskan pada optimalisasi pendekatan ini.
Tabel 1. Inokulasi dengan metode celup bunga dibandingkan dengan inokulasi dengan bantuan vakum
Perlakuan % Transformasi
Percobaan A:
Celupkan/ + L77 0,47 ± 0,16
Vakum/ + L77 0,56 ± 0,13
Percobaan B:
Turun/-L77 0,07 ± 0,06
Celupkan/ + L77 0,23 ± 0,07
Vakum/-L77 0,49 ± 0,20
Vakum/ + L77 0,50 ± 0,16
Inokulum A. tumefaciens disuspensikan kembali hingga OD 600 = 0,8 dalam Media MS dengan BAP, 5% sukrosa, dan (bila diindikasikan) 0,005% Silwet L-77. Nilai adalah rata-rata ± SE.
Perbandingan jumlah surfaktan yang berbeda dalam media inokulasi menunjukkan bahwa kadar Silwet L-77 antara 0,02% dan 0,1% memberikan tingkat transformasi sekitar 20 kali lipat lebih besar daripada 0,005% ketika tanaman diinokulasi dengan cara dicelupkan ( Gbr. 2 ). Jika persentase surfaktan Silwet L-77 ditingkatkan dari 0,005% menjadi 0,05% atau 0,1%, tingkat transformasi dengan cara dicelupkan sama tinggi atau lebih tinggi daripada yang diperoleh dengan menggunakan vakum (misalnya bandingkan Gbr. 2 dan Gbr. 1 ). Kami menggunakan Silwet L-77 0,05% dalam percobaan berikutnya di mana tanaman diinokulasi dengan cara dicelupkan ke dalam bunga. Namun, kehati-hatian disarankan dalam penggunaan kadar surfaktan yang tinggi karena kadar yang lebih tinggi ini dapat menyebabkan nekrosis jaringan tanaman di beberapa lingkungan.
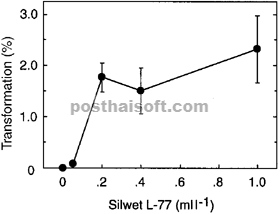
Pengaruh konsentrasi Silwet L-77 terhadap laju transformasi setelah inokulasi celup.
Untuk setiap perlakuan, tiga pot atau lebih yang berisi 6–20 tanaman dicelupkan ke dalam Agrobacterium dan sukrosa 5% yang ditambah dengan jumlah Silwet L-77 yang ditentukan. Inokulum bakteri berada pada OD 600 = 0,8. Nilai adalah rata-rata ± SE.
Analisis media inokulasi yang disederhanakan
Percobaan yang memanipulasi medium inokulasi ( Gambar 1b ) menunjukkan bahwa satu-satunya komponen yang bermanfaat secara signifikan dari medium standar adalah sukrosa dan surfaktan Silwet L-77. Dalam percobaan berikutnya menggunakan metode celupan bunga dan medium inokulasi yang dimodifikasi yang hanya mengandung gula dan 0,05% Silwet L-77, kami menentukan bahwa laju transformasi tidak berubah secara signifikan pada berbagai konsentrasi sukrosa antara 0,5 dan 5% ( Tabel 2 ). Peningkatan tiga hingga empat kali lipat dalam laju transformasi ketika sukrosa digunakan pada 10% dalam rangkaian percobaan ini tidak diamati secara konsisten (misalnya, dalam percobaan terpisah laju transformasi rata-rata 1,62% diperoleh dengan sukrosa 5% sementara hanya laju 0,81% diperoleh dengan sukrosa 10%). Tabel 2 juga menunjukkan bahwa sukrosa food grade yang lebih murah (merek C&H) atau glukosa 5% (jumlah molarnya hampir sama dengan sukrosa 10%) dapat menggantikan sukrosa reagen dengan baik. Media inokulasi yang mengandung manitol dapat merusak tanaman. Ketika diinokulasi dengan Agrobacterium yang disuspensikan dalam manitol 5%, jaringan tanaman di atas tanah menjadi basah kuyup dan kemudian menunjukkan nekrosis daun yang parah atau kematian tanaman 2–4 hari setelah inokulasi. Nekrosis serupa terjadi ketika Agrobacterium tidak dimasukkan dalam media inokulasi manitol.
Tabel 2. Pengaruh berbagai gula terhadap transformasi
Gula % Transformasi
Tanpa gula 0,04 ± 0,01
Sukrosa, 0,5% 0,40 ± 0,13
Sukrosa, 1,25% 0,34 ± 0,03
Sukrosa, 2,5% 0,47 ± 0,13
Sukrosa, 5% 0,36 ± 0,08
Sukrosa, 10% 1,42 ± 0,25
Glukosa, 0,5% 0,14 ± 0,08
Glukosa, 1,25% 0,11 ± 0,08
Glukosa, 5% 0,76 ± 0,29
Glukosa, 10% 0,33 ± 0,12
Manitol, 5% a kematian
5% sukrosa tingkat pangan 0,48 ± 0,27
Tanaman yang dicelupkan ke dalam A. tumefaciens disuspensikan kembali hingga OD 600 = 0,8 dalam Silwet L-77 (0,05%) dengan gula seperti yang disebutkan. Nilai adalah rata-rata ± SE.
Silwet L-77 0,005% untuk pengobatan manitol.
Analisis lebih lanjut tentang protokol
Analisis siliques individual dari tanaman yang diobati dengan Agrobacterium menunjukkan bahwa bunga-bunga individual dari tahap perkembangan tertentu lebih disukai untuk ditransformasikan ( Bechtold et al . 1993 ; C. Desfeux, S. Clough dan A. Bent, hasil yang tidak dipublikasikan). Benih yang ditransformasikan ditemukan dalam minoritas siliques pada tanaman tertentu dan siliques ini tidak terdistribusi secara merata di seluruh tanaman. Jika transformasi bunga bergantung pada tahap perkembangan maka bunga pada tahap tertentu cenderung sangat reseptif terhadap transformasi, dan kami beralasan bahwa beberapa inokulasi Agrobacterium selama pembungaan dapat menghasilkan peningkatan jumlah transforman. Ketika Agrobacterium diaplikasikan pada tanaman dengan cara celupan bunga tiga kali dengan jarak 6 hari di antara setiap aplikasi, laju transformasi dan hasil keseluruhan transforman meningkat sekitar dua kali lipat ( Gbr. 3 dan data tidak ditampilkan). Namun, aplikasi Agrobacterium selama periode 2 minggu dengan interval setiap empat hari atau kurang sangat merugikan kesehatan tanaman. Meskipun beberapa transforman diperoleh setelah inokulasi yang lebih sering ( Gambar 3 ), sebagian besar jaringan tanaman mati dan lebih sedikit benih yang diperoleh dari tanaman tersebut.
Agar transformasi berhasil terjadi, operon gen vir dari Agrobacterium harus aktif secara transkripsi ( Winans 1992 ). Di alam, lokasi luka sering menawarkan sinyal penginduksi vir seperti senyawa fenolik, heksosa, dan pH rendah. Dalam metode transformasi kultur jaringan, senyawa fenolik asetosiringon terkadang ditambahkan untuk menginduksi ekspresi gen vir . Ketika kami mencoba untuk menginduksi terlebih dahulu gen vir dengan menumbuhkan Agrobacterium selama 20 jam dalam medium cair penginduksi vir standar ( Liu et al . 1992 ) alih-alih dalam medium cair kaya, laju transformasi tidak berubah secara signifikan (1,03 kali lipat dari nilai untuk sel yang tumbuh dalam medium cair kaya). Pertumbuhan pada medium CIB penginduksi vir padat ( Fullner et al . 1994 ) pada 19°C menyebabkan penurunan empat kali lipat dalam laju transformasi. Penurunan ini mungkin disebabkan oleh komposisi medium, pertumbuhan pada medium padat, atau suhu pertumbuhan, tetapi bagaimanapun juga tidak menguntungkan.
Dalam penelitian sebelumnya yang menggunakan infiltrasi vakum untuk inokulasi, kami juga meneliti masalah fase pertumbuhan dan kepadatan sel dalam persiapan dan penggunaan inokulum Agrobacterium . Dalam protokol standar kami sebelumnya, sel ditumbuhkan hingga fase stasioner (OD 600 ≈2,0), dipeletkan, dan disuspensikan kembali dalam medium inokulasi hingga OD 600 sekitar 0,8 ( Bent & Clough 1998 ). Ketika Agrobacterium ditumbuhkan hingga fase stasioner dan kemudian disuspensikan kembali pada berbagai konsentrasi inokulum mulai dari OD 600 = 0,15–1,75, terdapat sedikit perbedaan dalam laju transformasi ( Tabel 3 ). Kami juga menemukan bahwa sel yang tumbuh hingga fase stasioner yang sangat akhir (dipersiapkan dari kultur yang ditumbuhkan selama 84 jam) dan diencerkan hingga OD 600 = 0,8 ditransformasikan seefisien kultur yang lebih muda. Dalam percobaan terpisah, kultur Agrobacterium yang tumbuh hingga OD 600 ≈2,0 atau OD 600 = 0,8 dipanen dan disuspensikan kembali hingga OD 600 = 0,8; kultur fase stasioner ditransformasi pada tingkat tiga kali lipat lebih tinggi daripada kultur fase log akhir (rata-rata ± kesalahan standar 0,39% ± 0,13 versus 0,12% ± 0,06).
Tabel 3. Pengaruh Kepadatan Inokulum Agrobacterium terhadap Laju Transformasi
Inokulum OD 600 % Transformasi
0,15 0,50 ± 0,02
0.42 0,21 ± 0,05
0.80 0,51 ± 0,14
1.10 0,51 ± 0,09
1.75 0,57 ± 0,15
0,8 (84 jam) 0,50 ± 0,05
Tanaman diinokulasi dengan infiltrasi vakum dengan A. tumefaciens dalam Media MS dengan BAP, 5% sukrosa dan 0,005% L-77. Semua bakteri disuspensikan kembali dari kultur cair semalam yang segar, kecuali ’84 jam’ dari kultur yang tumbuh selama 84 jam. Nilai adalah rata-rata ± SE.
Protokol standar kami sebelumnya mengharuskan tanaman ditempatkan di bawah kubah plastik atau penutup lain yang menahan kelembapan selama 12–24 jam setelah inokulasi. Sebagai uji kontribusi perlakuan kubah terhadap laju transformasi, sebuah eksperimen dilakukan dengan menggunakan tujuh kultur Agrobacterium yang terpisah tetapi disiapkan dengan cara yang sama untuk merawat kelompok tanaman yang berpasangan. Untuk masing-masing dari tujuh pasang, satu pot ditempatkan di bawah kubah dan yang lainnya dibiarkan terbuka. Menutupi tanaman semalaman setelah inokulasi memberikan laju yang sama atau jauh lebih tinggi dalam semua kasus, dengan laju transformasi keseluruhan (rata-rata ± galat standar) sebesar 0,24% ± 0,08 untuk tanaman berkubah dibandingkan dengan 0,10% ± 0,03 untuk tanaman yang tidak tertutup.
Berbagai ekotipe dan strain Agrobacterium
Untuk menentukan apakah ekotipe Arabidopsis Col-O unik karena dapat ditransformasi dengan cara mencelupkan tanaman ke dalam Agrobacterium yang disuspensikan dalam 5% sukrosa dan 0,05% Silwet L-77, kami mencoba mentransformasi ekotipe Arabidopsis lainnya menggunakan metode celupan bunga ini. Ekotipe Ws-O, Nd-O, No-O ditransformasi pada laju yang mirip dengan Col-O. Sebaliknya, Ler-O, Dijon-G dan Bla-2 ditransformasi pada laju 10 hingga 100 kali lipat lebih rendah (data tidak ditampilkan). Dalam salah satu percobaan, tidak ada transforman yang diperoleh dengan Ler-0. Dalam percobaan yang meneliti penggunaan galur Agrobacterium lainnya , LBA4404 ( Ooms et al . 1982 ), EHA105 ( Hood et al . 1993 ) dan Chry105 (S. Clough, hasil tidak dipublikasikan) berhasil digunakan untuk mentransformasi ekotipe Col-0 dengan metode celupan bunga.
Diskusi
Pada tahun 1993, Bechtold dan koleganya menerbitkan metode asli mereka untuk transformasi Arabidopsis dengan infiltrasi vakum Agrobacterium ( Bechtold et al . 1993 ). Sejak saat itu sejumlah modifikasi pada protokol mereka telah disarankan (misalnya http://genome-www.stanford.edu/cgi-bin/biosciarabidopsis ), tetapi tidak ada laporan formal dari eksperimen terkontrol untuk menilai lebih lanjut metode transformasi ini tersedia hingga baru-baru ini ( Richardson et al . 1998 ). Studi saat ini dimulai untuk memberikan penilaian tersebut dan untuk mengidentifikasi perbaikan yang memfasilitasi transformasi berthroughput tinggi. Peningkatan dan penyederhanaan pada transformasi Arabidopsis diidentifikasi yang membuat protokol yang relatif nyaman menjadi lebih mudah dan bahkan lebih nyaman.
Kami menemukan bahwa transforman Arabidopsis dapat diperoleh pada tingkat tinggi (0,5–3% dari semua benih keturunan) hanya dengan mencelupkan tanaman berbunga dalam Agrobacterium yang disuspensikan dalam larutan yang mengandung sukrosa (atau glukosa) dan surfaktan Silwet L-77. Media kultur jaringan tanaman, penyesuaian pH, pengatur pertumbuhan tanaman, dan pertumbuhan atau penggunaan Agrobacterium pada kepadatan kultur tertentu tidak penting untuk transformasi tingkat tinggi yang berhasil. Yang terpenting, infiltrasi vakum ditemukan tidak diperlukan selama surfaktan yang sesuai digunakan. Protokol yang dimodifikasi memungkinkan perawatan populasi Arabidopsis skala besar dalam pengaturan rumah kaca tanpa memerlukan peralatan vakum atau untuk mencabut dan menanam kembali tanaman. Kombinasi metode ini dengan metode seleksi throughput tinggi (seperti pendekatan sand-bed/Basta dari Bouchez et al . 1993 ) memungkinkan generasi ribuan transforman Arabidopsis independen yang efisien.
Tiga persyaratan utama untuk transformasi yang berhasil adalah: (1) tahap perkembangan tanaman yang benar (jumlah maksimum kelompok kuncup bunga yang belum terbuka); (2) gula; dan (3) surfaktan dan/atau vakum untuk membantu infiltrasi. Peneliti dapat menggunakan vakum, surfaktan, atau keduanya untuk membantu pengiriman bakteri ke sel tanaman target – kami memperoleh tingkat transformasi yang sama dengan kedua metode tersebut. Kami juga menemukan bahwa transformasi dapat dicapai tanpa vakum atau surfaktan, serta tanpa sukrosa atau glukosa, tetapi hanya secara tidak konsisten atau jarang. Sementara surfaktan lain mungkin bekerja, Silwet L-77 awalnya dipilih ( Whalen et al . 1991 ) karena mengurangi tegangan permukaan lebih dari kebanyakan surfaktan dan, pada dosis dengan fitotoksisitas rendah, sangat meningkatkan masuknya bakteri ke dalam jaringan tanaman yang relatif tidak dapat diakses. Penggunaan surfaktan juga memungkinkan transformasi setelah penyemprotan jaringan bunga Arabidopsis dengan Agrobacterium (data tidak ditampilkan). Namun, metode penyemprotan dapat menimbulkan masalah penahanan dan kontaminasi silang, serta menimbulkan masalah keselamatan pekerja (aerosol Silwet L-77 dapat membahayakan jaringan kornea khususnya).
Tampaknya ada tahap perkembangan bunga yang ideal baik untuk akses Agrobacterium ke jaringan target atau untuk kerentanan jaringan tersebut terhadap transformasi. Tahap ideal ini ditargetkan lebih berhasil dengan inokulasi berulang pada hari yang berbeda. Namun, manfaat inokulasi berulang (di tangan kami, peningkatan dua hingga tiga kali lipat dalam laju transformasi) mungkin tidak selalu membenarkan upaya tambahan yang diperlukan. Kami menemukan bahwa tanaman dirugikan oleh aplikasi ulang Agrobacterium yang berlebihan dengan interval kurang dari 4 hari.
Penutupan tanaman yang diinokulasi dengan kubah plastik untuk menjaga kelembapan tinggi selama 12–24 jam pertama setelah inokulasi bermanfaat, karena menghasilkan transforman sekitar dua kali lebih banyak. Kami berasumsi bahwa kubah memperpanjang ketersediaan air permukaan tempat sel Agrobacterium motil dapat berenang untuk mencapai sel target potensial, meskipun kelembapan mungkin sama pentingnya dalam menjaga jaringan inang dalam konfigurasi yang mudah diakses. Efek penutup kubah dapat bervariasi tergantung pada suhu, panjang hari, intensitas cahaya, dan faktor lingkungan lainnya yang bervariasi di antara laboratorium.
Transfer T-DNA dari Agrobacterium ke inang memerlukan, antara lain, aktivasi ekspresi gen Agrobacterium vir oleh produk virA dan virG ( Winans 1992 ). Ekspresi gen vir sangat rendah ketika Agrobacterium tumbuh di media cair kaya seperti LB. Meskipun demikian, metode infiltrasi vakum telah berhasil secara luas menggunakan Agrobacterium yang tumbuh di media kaya, dan kami menemukan bahwa pertumbuhan strain A. tumefaciens GV3101(pMP90)(pBin-gfp5-ER) dalam media penginduksi vir standar tidak secara substansial meningkatkan laju transformasi. Sebagian besar peristiwa transformasi tampaknya terjadi setelah Agrobacterium menyesuaikan diri secara metabolik dengan lingkungan inang, dan dapat terjadi beberapa hari setelah tanaman diinokulasi. Namun, kecocokan yang tepat antara genotipe inang dan strain Agrobacterium , plasmid Ti, dan vektor biner mungkin masih penting. Studi kuantitatif yang disajikan dalam karya ini menggunakan GV3101(pMP90), strain berdasarkan genotipe C58 dan pTiC58 yang telah terbukti produktif jika digunakan bersama Arabidopsis ( Bechtold et al . 1993 ; Katavic et al . 1994 ; Koncz & Schell 1986 ). Metode celupan bunga juga berhasil jika digunakan bersama strain Agrobacterium LBA4404, EHA105, dan Chry105.
Metode celupan bunga sangat berhasil untuk transformasi beberapa ekotipe Arabidopsis termasuk Col-0, Ws-0, Nd-0 dan No-0, tetapi tidak sama efisiennya dengan semua ekotipe. Kurang berhasilnya kami dengan Ler-0 mungkin disebabkan oleh kompatibilitas yang rendah dengan Agrobacterium , atau pada tahap pertumbuhan tanaman yang digunakan. Perbungaan Ler-0 berkembang secara berbeda dari kebanyakan ekotipe lainnya, dan perbungaan pada tanaman Ler-0 yang digunakan dalam percobaan kami mungkin secara perkembangan berada di belakang atau di depan ekotipe seperti Col-0. Yang lain juga menemukan bahwa Ler-0 lebih sulit atau bervariasi daripada ekotipe seperti Col-0 ketika digunakan untuk transformasi in planta , tetapi ada banyak laporan informal dan formal tentang keberhasilan transformasi ekotipe ini dengan metode in planta (misalnya http://genome-www.stanford.edu/cgi-bin/biosciarabidopsis , Richardson et al . 1998 ). Perbedaan spesifik ekotipe dalam kerentanan Arabidopsis terhadap Agrobacterium juga telah didokumentasikan untuk sistem transformasi berbasis kultur jaringan ( Nam et al . 1997 ).
Laporan penggunaan infiltrasi vakum Agrobacterium atau metode serupa untuk transformasi spesies tanaman selain Arabidopsis tidak tersedia. Ini mungkin sebagian karena upaya yang tidak memadai, mengingat bahwa tingkat transformasi 10 kali lipat atau 100 kali lipat lebih rendah daripada yang ditemukan dengan Arabidopsis akan memerlukan penyaringan 10.000 atau lebih benih. Salah satu motivasi untuk penelitian saat ini adalah untuk mengidentifikasi pendekatan yang paling efektif menggunakan Arabidopsis , tanaman yang cocok untuk transformasi dengan aplikasi Agrobacterium pada jaringan bunga, sehingga metode serupa dapat diterapkan pada spesies lain. Tugas utama di luar cakupan penelitian saat ini adalah untuk mengidentifikasi jaringan target yang awalnya ditransformasi ketika Arabidopsis diobati menggunakan protokol ini. Keberhasilan metode celupan bunga menyiratkan bahwa jaringan garis benih yang ditransformasi, pada beberapa titik selama prosedur, terpapar dan dapat diakses oleh Agrobacterium yang telah diterapkan secara pasif pada jaringan bunga hanya dengan pencelupan.
Versi awal metode ini dan metode terkait telah dikenal sebagai ‘ infiltrasi vakum Agrobacterium ‘ atau ‘ transformasi In planta ‘ ( Bechtold et al . 1993 ; Chang et al . 1994 ; Feldmann 1992 ; Katavic et al . 1994 ). Sehubungan dengan metode saat ini, nama-nama ini tidak akurat atau ambigu karena telah digunakan sebelumnya untuk menggambarkan metode yang sangat berbeda. Untuk memberikan nama yang berbeda yang menggambarkan proses ini, kami mengusulkan istilah ‘floral dip’ untuk metode di mana tanaman ditransformasi dengan aplikasi langsung Agrobacterium ke jaringan bunga tanpa menggunakan vakum atau perangkat penekan lainnya. Metode pilihan kami untuk transformasi Arabidopsis dapat ditemukan di bawah Prosedur eksperimental, dan protokol floral dip yang ringkas tersedia di http://www.cropsci.uiuc.edu/∼a-bent/protocol.html , atau atas permintaan dari penulis.
Prosedur Eksperimen
Pertumbuhan tanaman
Tanaman Arabidopsis ditanam hingga tahap berbunga di rumah kaca yang teduh, 24°C siang/20°C malam, dengan pencahayaan natrium tekanan tinggi tambahan yang diaktifkan selama 18 jam siang hari ketika tingkat cahaya luar ruangan turun di bawah 250 μEinstein m –2 s –1 . Kecuali dinyatakan lain, tanaman yang digunakan adalah tanaman Arabidopsis ekotipe Col-0 yang secara genetik ditandai dengan alel rps2–201 dari gen resistensi RPS2 ( Kunkel et al . 1993 ). Tanaman biasanya ditanam 1–2 per pot 25 cm2 atau 6–20 per pot 64 cm2 di tanah pot yang dibasahi (Sunshine Mix #1; Sun Gro Horticulture Inc., Bellevue, WA, AS). Untuk mencegah tanah dalam pot yang lebih besar jatuh ke media inokulasi, tanah ditimbun sedikit di atas tepi wadah tanaman, benih ditanam, dan tanah kemudian ditutup dengan kasa jendela nilon atau kain tule (kerudung) dan diikat dengan karet gelang. Untuk mendapatkan lebih banyak kuncup bunga per tanaman, perbungaan dipotong setelah sebagian besar tanaman membentuk cabang primer, sehingga mengurangi dominasi apikal dan mendorong munculnya beberapa cabang sekunder secara bersamaan. Tanaman diinfiltrasi atau dicelupkan ketika sebagian besar perbungaan sekunder tingginya sekitar 1–10 cm (4–8 hari setelah pemotongan).
Protokol standar untuk kultur Agrobacterium tumefaciens dan inokulasi tanaman
Strain Agrobacterium tumefaciens GV3101(pMP90) ( Koncz & Schell 1986 ) yang membawa plasmid biner pBINm-gfp5-ER ( Haseloff et al . 1997 ) digunakan dalam semua percobaan yang datanya ditampilkan. Kecuali disebutkan, bakteri ditumbuhkan ke fase stasioner dalam kultur cair pada 25–28°C, 250 rpm dalam LB yang disterilkan (10 g tripton, 5 g ekstrak ragi, 5 g NaCl per liter air) yang membawa tambahan kanamisin (25 μg ml –1 ). Kultur biasanya dimulai dari pengenceran 1:100 kultur semalam yang lebih kecil dan ditumbuhkan selama sekitar 18–24 jam. Sel dipanen dengan sentrifugasi selama 20 menit pada suhu ruangan pada 5500 g dan kemudian disuspensikan kembali dalam media infiltrasi hingga OD 600 akhir sekitar 0,80 sebelum digunakan. Media inokulasi celupan bunga yang telah direvisi mengandung 5,0% sukrosa dan 0,05% (yaitu 500 μl l –1 ) Silwet L-77 (OSi Specialties, Inc., Danbury, CT, AS). Media inokulasi ‘standar’ sebelumnya ( Bent & Clough 1998 ) terdiri dari Medium Basal Murashige & Skoog dengan kekuatan 1/2 (Sigma Chemicals #M-5519, St. Louis, MO, AS), 5,0% sukrosa, 44 nm benzylamino purine (10 μl l –1 dari stok 1 mg ml –1 dalam DMSO; Sigma Chemicals #B-3274), 0,005% Silwet L-77, pH disesuaikan menjadi 5,7. Media lainnya seperti yang disebutkan.
Untuk perendaman bunga, inokulum ditambahkan ke gelas kimia, tanaman dibalikkan ke dalam suspensi ini sehingga semua jaringan di atas tanah terendam, dan tanaman kemudian diangkat setelah 3–5 detik pengadukan lembut. Untuk infiltrasi vakum, gelas kimia yang berisi tanaman yang terendam dalam inokulum ditempatkan ke dalam ruang (toples kaca) dan vakum diterapkan hingga gelembung udara dikeluarkan dari jaringan tanaman. Dengan menggunakan pompa vakum, ini biasanya memerlukan waktu 30–60 detik. Vakum kemudian ditahan selama 5–15 detik lagi, selama waktu itu larutan mendidih dengan kuat, dan vakum kemudian dilepaskan dengan cepat. Tanaman yang dicelupkan atau diinfiltrasi vakum dikeluarkan dari gelas kimia, ditempatkan dalam baki plastik dan ditutup dengan kubah plastik bening yang tinggi untuk menjaga kelembapan. Tanaman dibiarkan di lokasi yang kurang cahaya atau gelap semalaman dan dikembalikan ke rumah kaca keesokan harinya; perawatan dilakukan untuk menjaga tanaman yang berbentuk kubah agar tidak terkena sinar matahari langsung. Kubah diangkat sekitar 12–24 jam setelah perawatan. Tanaman ditanam selama 3–5 minggu hingga siliques berwarna cokelat dan kering, dengan menjaga agar baut dari setiap pot tetap menyatu dan terpisah dari pot di sebelahnya menggunakan selotip dan/atau kertas lilin. Benih dipanen dengan menarik perlahan perbungaan yang dikelompokkan menggunakan jari di atas selembar kertas bersih. Sebagian besar bahan batang dan polong dikeluarkan dari kertas dengan meniup perlahan dan benih disimpan dalam tabung mikrofuge dan disimpan pada suhu 4°C dalam kondisi kering.
Pemilihan transforman putatif menggunakan penanda antibiotik
Benih disterilkan permukaannya dengan metode fase cair atau uap. Untuk sterilisasi cair, benih pertama-tama diolah dengan etanol 95% selama 30–60 detik, kemudian dengan pemutih 50% (2,625% natrium hipoklorit, volume akhir) yang mengandung 0,05% Tween 20 selama 5 menit, diikuti dengan tiga kali pembilasan dengan air steril. Untuk sterilisasi fase uap, benih dalam wadah terbuka ditempatkan ke dalam tabung desikator 10 l, ditempatkan di lemari asam. Tepat sebelum menutup desikator, gelas kimia 250 ml yang berisi 100 ml pemutih ditambahkan dan 3 ml HCl pekat ditambahkan dengan hati-hati ke dalam pemutih. Desikator dengan asap klorin tetap tertutup rapat selama 4 atau 15 jam. Bahasa Indonesia: Untuk memilih tanaman yang ditransformasi, benih yang disterilkan disuspensikan dalam agarosa steril 0,1% dan ditanam pada pelat seleksi kanamisin pada kepadatan sekitar 3000 benih per pelat 150 × 15 mm 2 , diperlakukan dingin selama 2 hari, dan kemudian tumbuh selama 7–10 hari dalam lingkungan yang terkendali pada 24°C di bawah 23 jam cahaya 50–100 μEinstein m –2 s –1 . Pelat seleksi berisi media 1/2X MS (Sigma Chemicals #M-5519), agar 0,8% (Sigma Chemicals #A-1296), 50 μg ml –1 kanamisin monosulfat. Dalam beberapa percobaan, pelat Petri dan tutupnya disegel dengan pita bedah selama minggu pertama pertumbuhan. Kelembapan berlebih selama pertumbuhan dihilangkan dengan membuka pelat sebentar dan mengibaskan kelembapan dari tutupnya. Transforman diidentifikasi sebagai bibit tanaman yang resistan terhadap kanamisin yang menghasilkan daun hijau dan akar yang tumbuh baik dalam media selektif. Beberapa transforman ditanam hingga dewasa dengan cara ditransplantasikan, sebaiknya setelah perkembangan 3–5 daun dewasa, ke dalam tanah pot yang sangat lembab. Di tempat yang diuji, DNA genom dari tanaman yang resistan terhadap kanamisin dicerna dengan enzim restriksi Hin dIII, dipisahkan secara elektroforesis, diblotting, dan kemudian diuji dengan fragmen Pst I 1,9 kb dari gen nptII dari pBINm-gfp5-ER pada dasarnya seperti pada Ausubel et al . (1997) . Laju transformasi, dinyatakan sebagai ‘persentase transformasi’, dihitung sebagai [(# bibit tanaman yang resistan terhadap kanamisin)/(total # bibit tanaman yang diuji)] × 100.
Ekspresi protein fluoresensi hijau diuji dengan mengamati daun yang dipotong dalam dudukan air pada mikroskop Olympus Vanox-T yang dilengkapi dengan filter eksitasi 20-BP405 nm dan cermin dichroic 455 nm.
Ucapan Terima Kasih
Pekerjaan ini didukung oleh hibah dari Dewan Penelitian Kedelai Utara Tengah.
