Abstrak
Mekanisme sorpsi untuk pengikatan arsenik (As) ke gugus fungsi tiol (-SH) dalam bahan organik alami (NOM) dapat memainkan peran penting dalam mengendalikan mobilitas dan bioavailabilitas As anorganik dalam lingkungan anaerobik, termasuk sawah. Ada minat besar dalam perilaku As dalam lingkungan tanah-air anaerobik karena kekhawatiran atas penyerapan As ke dalam padi. Di sini, kami meneliti sorpsi arsenit (As(III)) ke resin Ambersep GT74 yang difungsikan tiol sebagai model untuk situs pengikatan tiol dalam NOM. Tujuan khusus dari pekerjaan ini adalah untuk mengevaluasi kinetika dan reversibilitas adsorpsi As(III) ke situs tiol. Kami melakukan eksperimen adsorpsi dan desorpsi, dan eksperimen kinetika untuk mengevaluasi aspek kesetimbangan dan kinetik adsorpsi As(III) ke adsorben kaya tiol. Kinetika adsorpsi dijelaskan dengan baik oleh model orde pertama sepotong-sepotong, dengan adsorpsi yang relatif cepat selama 24 jam pertama diikuti oleh adsorpsi lambat selama 72 jam tambahan. Model isoterm Langmuir yang sesuai menunjukkan bahwa nilai afinitas dan kapasitas Ambersep GT74 untuk As(III) tidak berbeda secara signifikan pada rentang pH yang umum untuk sistem tanah-air alami. Percobaan desorpsi mengonfirmasi bahwa penyerapan As(III) bersifat ireversibel pada konsentrasi As(III) berair rendah, yang menunjukkan bahwa As(III) yang terikat pada permukaan yang mengandung tiol akan tetap tidak bergerak dan kemungkinan besar tidak tersedia untuk penyerapan biologis setelah perubahan kimia larutan tanah.
Ringkasan Bahasa Sederhana
Arsenik (As) di tanah yang tergenang air, seperti sawah, menimbulkan risiko karena potensi penyerapan oleh tanaman padi. Studi ini meneliti bagaimana arsenit As(III), bentuk umum arsenik, mengikat gugus yang mengandung sulfur (-SH) dalam bahan organik alami, yang membantu melumpuhkan arsenik dalam lingkungan anaerobik. Dengan menggunakan bahan sintetis (Ambersep GT74) sebagai model untuk tempat pengikatan ini, kami mengevaluasi seberapa cepat arsenit menempel, kekuatan pengikatannya, dan apakah prosesnya dapat dibalik. Temuan menunjukkan bahwa arsenit mengikat dengan cepat dalam 24 jam pertama, dengan pengikatan yang lebih lambat selama beberapa hari berikutnya. Kekuatan dan kapasitas pengikatan tetap konsisten di seluruh rentang pH tanah yang umum. Yang penting, setelah arsenit mengikat pada konsentrasi rendah, ia tidak mudah terlepas, bahkan jika kondisinya berubah. Ini menunjukkan bahwa arsenik yang terikat sulfur cenderung tetap tidak bergerak dan tidak tersedia untuk diserap tanaman, mengurangi mobilitas dan bioavailabilitasnya di tanah anaerobik.
Singkatan
A A
alumina aktif
Sebagai
arsenik
DOM
bahan organik terlarut
ICP-MS
Spektrometri Massa Plasma yang Digabungkan Secara Induktif
NOM
bahan organik alami
RMSE
kesalahan akar kuadrat rata-rata
S organisasi
kandungan sulfur organik
1. PENDAHULUAN
Kontaminasi arsenik (As) pada lingkungan akuatik dan terestrial merupakan masalah yang sudah diketahui. Dalam beberapa tahun terakhir telah ada perhatian yang lebih besar terhadap dinamika biogeokimia As di lingkungan persawahan, yang terutama dimotivasi oleh kekhawatiran tentang paparan manusia terhadap As melalui konsumsi beras (Khan et al., 2010 ; Marin et al., 1993 ). Arsenik terutama dimobilisasi dalam lingkungan bawah permukaan anaerobik ini melalui pelarutan reduktif fase oksida besi (Fe), dan melalui reduksi arsenat (As(V)) menjadi arsenit yang lebih mobil (As(III)) (Gallegos et al., 2007 ), yang biasanya merupakan bentuk dominan As anorganik dalam lingkungan reduksi. Tanah lahan basah dan persawahan kaya akan bahan organik alami (NOM) dari vegetasi yang membusuk, yang memainkan peran penting dalam memicu bakteri heterotrofik yang mereduksi fase oksida Fe untuk melarutkan As (Akai et al., 2004 ). Di luar peran NOM yang diakui dengan baik sebagai donor elektron untuk metabolisme mikroba, terdapat berbagai interaksi langsung dan tidak langsung antara As dan NOM yang memengaruhi spesiasi, mobilitas, dan nasib As melalui jalur yang belum sepenuhnya dipahami (Abu-Ali et al., 2022 ; Bushmann et al., 2006 ; Pothier et al., 2020 ; Redman et al., 2002 ; Yoon et al., 2024 ).
Kelompok fungsional tiol dalam NOM memiliki afinitas tinggi terhadap As(III) (Hoffman et al., 2012, 2014 ; Spuches et al., 2005 ), dan ada bukti yang berkembang bahwa kompleksasi As(III) dengan NOM kaya S (di mana S adalah sulfur) dapat memainkan peran penting dalam mengendalikan nasib As(III) di lingkungan kaya NOM (Abu-Ali et al., 2022 ; Langner et al., 2011 ; Pothier et al., 2020 ; Yoon et al., 2022 ). Misalnya, Yoon et al. ( 2022 ) menunjukkan bahwa penyerapan As(III) oleh mikroba dihambat dengan adanya NOM kaya S, kemungkinan sebagian karena kompleksasi As(III)–NOM, dan studi lanjutan menggunakan spektroskopi struktur halus serapan sinar-X (EXAFS) yang diperluas untuk menunjukkan bahwa As(III) bereaksi dengan NOM Sungai Mississippi Hulu yang dikoordinasikan dengan lokasi S (Yoon et al., 2023 ). Dalam studi lain, asam humat yang dimodifikasi dengan tiol secara efektif memobilisasi As dari tailing tambang (Qian et al., 2022 ). As(III) diketahui mengikat gugus tiol dalam protein dan memodelkan fungsi tiol dalam fitokhelatin, mekanisme di mana tanaman menyerap As(III) di akar dan batang (Song et al., 2010 ). Meskipun kesadaran akan dampak NOM kaya tiol terhadap perilaku lingkungan As(III) semakin meningkat, studi mekanistik kompleksasi As(III)–tiol masih cukup terbatas (Arencibia et al., 2020 ; Hao, Han, & Meng, 2009 ; Hao, Han, Wang, & Meng, 2009 ). Sementara konstanta stabilitas untuk kompleksasi As(III) dengan fungsionalitas tiol tersedia (Hoffman et al., 2014 ; Spuches et al., 2005 ), sejauh pengetahuan kami, reversibilitas reaksi ini dan kinetika reaksi kompleksasi As(III)–tiol belum banyak dipelajari dan dipahami.
Di sini, kami meneliti kinetika dan reversibilitas reaksi kompleksasi As(III)–thiol menggunakan resin Ambersep GT74 yang kaya thiol sebagai model interaksi As(III) dengan NOM kaya S yang mungkin ada di tanah sawah. Kami melakukan pengukuran desorpsi As(III) dari Ambersep, penilaian langsung terhadap reversibilitas pengikatan As(III) ke thiol, untuk menjawab pertanyaan yang belum terjawab mengenai peran thiol yang terkait dengan bahan organik terlarut (DOM) dalam memediasi reaksi kompleksasi As(III) dan NOM. Kami juga meneliti kinetika adsorpsi As(III) ke Ambersep, faktor penting untuk memahami persaingan di antara berbagai sorben untuk As(III). Tujuan dari penelitian ini adalah untuk memperluas pemahaman tentang pengikatan As(III) ke fungsi thiol sehingga dapat lebih memahami bagaimana NOM kaya S dalam sistem tanah–air dapat memengaruhi mobilitas dan nasib As. Kekhawatiran yang berkembang tentang spesiasi dan nasib As di tanah sawah pertanian memerlukan perhatian baru terhadap pentingnya bagian tiol untuk bahan organik tanah berkaitan dengan interaksi As di lingkungan kaya organik.
2 BAHAN DAN METODE
2.1 Reagen dan bahan kimia
Semua larutan disiapkan di dalam ruang anaerobik (Laboratorium Coy; 96%–97% N 2 ; 3%–4% H 2 < 10 ppM O 2 ), menggunakan air Milli-Q yang telah direbus dan dibersihkan dengan gas nitrogen (N 2 ) selama minimal 30 menit. Larutan arsenit (As(III)) disiapkan dari natrium arsenit (Fisher Scientific) dan resin khelasi Ambersep GT74 (Dupont Chemical Company) digunakan sebagai model adsorben kaya tiol untuk As(III). Ambersep GT74 adalah resin asam lemah yang terutama telah digunakan sebagai adsorben untuk spesies kationik termasuk merkuri, kadmium, timbal, perak, dan tembaga yang memiliki afinitas tinggi terhadap sulfur (DuPont Water Solutions, 2020 ). Ambersep GT74 telah digunakan dalam penelitian sebelumnya sebagai adsorben kaya tiol untuk As(III) (Hoffman et al., 2012 ). Sebelum digunakan, resin dicuci bersih dengan air anoksik dan disimpan dalam ruang anaerobik hingga digunakan dalam percobaan penyerapan.
2.2 Titrasi potensiometri
Konstanta disosiasi proton (p Ka ) dan kerapatan situs gugus fungsi Ambersep GT74 ditentukan menggunakan titrasi asam-basa potensiometri dalam larutan NaCl 30 mM di bawah atmosfer N 2 menggunakan pengaturan titrasi terkendali dengan pH meter Thermo Orion. 0,45 g Ambersep dipindahkan ke 100 mL larutan NaCl 30 mM dan pH diatur menjadi 12 menggunakan NaOH. Suspensi kemudian dititrasi dengan HCl 0,3 M. Suspensi dicampur dengan batang pengaduk magnetik dan pelat. Sebanyak 7 mL HCl ditambahkan ke suspensi Ambersep. Pemodelan data titrasi menggunakan program Protofit awalnya memungkinkan lebih dari satu situs pengikatan, tetapi ditentukan bahwa model satu situs lebih tepat (Turner & Fein, 2006 ). Kriteria yang digunakan untuk membuat penentuan ini adalah bahwa penambahan situs kedua gagal menurunkan root mean square error (RMSE) lebih dari 5%.
2.3 Percobaan kinetika sorbsi
Percobaan kinetika sorpsi dilakukan dalam rangkap tiga di dalam ruang anaerobik pada suhu 29°C, suhu sekitar di dalam ruang anaerobik akibat katalis yang dipanaskan dalam pembersih oksigen. Kinetika adsorpsi As(III) dipelajari sebagai fungsi pH (5,4, 6,5, atau 8) dan konsentrasi awal As(III) (2,5, 10, dan 25 µM). Percobaan dilakukan dengan 22,5 mg Ambersep dalam 10,6 mL larutan dalam tabung sentrifus 15 mL pada pemutar tabung. Kekuatan ionik diberikan oleh 30 mM NaCl. Sampel dikumpulkan pada 0, 0,5, 1, 2, 6, 12, 36, 48, 72, dan 96 jam, disaring melalui filter 0,2 µm, dan diawetkan dalam asam nitrat 2%.
2.4 Model kinetik
Persamaan laju orde pertama semu (Maji et al., 2008 ; Malash & El-Khaiary, 2010 ) digunakan untuk menggambarkan kinetika serapan. Untuk proses yang menunjukkan fase “cepat” dan “lambat”, model orde pertama semu sepotong-sepotong (Zhang & Selim, 2005 ) dapat digunakan:
(1)
di mana C adalah konsentrasi As terlarut (mM), t adalah waktu (h), dan k 1 dan k 2 (h −1 ) adalah konstanta laju orde pertama semu untuk fase “cepat” dan “lambat”, masing-masing. t cepat dan t lambat merujuk pada rentang waktu untuk fase “cepat” dan “lambat”, yang ditentukan secara empiris. Konstanta laju ditentukan melalui regresi linier sepotong-sepotong dari konsentrasi As(III) yang ditransformasikan logaritma natural sebagai fungsi waktu.
Ide Inti
Model Langmuir menunjukkan afinitas dan kapasitas yang sama untuk As(III) pada Ambersep GT74 pada kisaran pH 5,4–8.
Kinetika adsorpsi menghadirkan dua fase, yaitu fase “cepat” dan fase “lambat”, yang menunjukkan adanya batas difusi.
Uji desorpsi menunjukkan penyerapan As(III) yang ireversibel pada konsentrasi rendah, yang menunjukkan imobilitas.
2.5 Percobaan adsorpsi dan desorpsi
Percobaan adsorpsi kesetimbangan dilakukan dalam rangkap tiga di dalam ruang anaerobik pada suhu 29°C pada pH 5,4, 6,5, atau 8. Komposisi media dan rasio Ambersep/larutan sama dengan yang digunakan dalam percobaan kinetika. Konsentrasi As(III) awal berkisar antara 2 hingga 600 µM. Tabung diaduk menggunakan pemutar tabung selama 96 jam. Sampel dikumpulkan pada waktu 0 dan 96 jam, disaring melalui filter membran 0,2-µm, dan diawetkan dalam asam nitrat 2%. Untuk proses desorpsi, setiap tabung didekantir dan 10,6 mL elektrolit segar ditambahkan ke setiap tabung. Tabung dicampur selama 96 jam lagi, pada saat itu larutan diambil sampelnya, disaring, dan diawetkan untuk analisis spektrometri massa plasma yang digabungkan secara induktif (ICP-MS). Data isoterm dijelaskan menggunakan model Langmuir sebagai berikut:
(2)
di mana q adalah kerapatan adsorpsi (mmol As g Ambersep −1 ), q max adalah kerapatan adsorpsi maksimum (mmol As g Ambersep −1 ), K ads adalah konstanta kesetimbangan (L mmol As −1 ), dan C adalah konsentrasi As dalam kesetimbangan dengan permukaan resin Ambersep (mmol As L −1 ). Model tersebut disesuaikan dengan data melalui regresi nonlinier di Matlab menggunakan fungsi nlinfit. Kesesuaian model dievaluasi berdasarkan RMSE.
2.6 Analisis kimia
Konsentrasi arsenik dianalisis menggunakan Agilent 7800 ICP-MS dengan sel tumbukan helium dan rodium sebagai standar internal in-line. Kontrol kualitas dilakukan dengan pengukuran berkala terhadap standar, blanko, sampel ulang, dan standar pemeriksaan (Maguffin et al., 2020 ). Potensi interferensi poliatomik dari ArCl + pada m/z = 75 dinilai dengan menguji sampel yang dicampur dengan NaCl hingga 100 mM, dan tidak ada yang terdeteksi. Standar kalibrasi disiapkan menggunakan standar multi-elemen yang dapat dilacak (Millipore Sigma Trace CERT).
3 HASIL DAN PEMBAHASAN
3.1 Karakterisasi Ambersep GT74
Data titrasi potensiometri Ambersep GT74 diilustrasikan dalam Gambar S1 . Penyertaan situs pengikatan kedua dicoba untuk menilai apakah model satu situs adalah yang paling tepat. Namun, pemasangan data dengan Protofit menunjukkan bahwa situs pengikatan kedua tidak meningkatkan kebaikan pemasangan secara signifikan, karena RMSE hanya menurun sebesar 1,1% (dari 0,9320 menjadi 0,9214; Gambar S2 ). Oleh karena itu, model satu situs dianggap memadai untuk menggambarkan data. Pemasangan data dengan Protofit menggunakan model satu situs memberikan ap Ka sebesar 9,6, yang hampir berada dalam kisaran p Ka s tiol protein dan non-protein sebesar 7,5–9,5 dan dalam kisaran p Ka s metanetiol dan etanetiol tersubstitusi sebesar 7,7–11,9 (Manceau & Nagy, 2019 ; Zheng et al., 2019 ). Kepadatan situs fungsional ditentukan sebesar 0,34 mmol g −1 .
3.2 Kinetika adsorpsi
Kinetika adsorpsi As(III) pada pH yang berbeda dan konsentrasi awal As(III) menunjukkan proses penyerapan dengan fase “cepat” awal selama 24 jam, diikuti oleh fase “lambat” yang berlanjut hingga 96 jam (Gambar 1 ) . Setiap fase dapat dijelaskan menggunakan kinetika pseudo-orde pertama. Parameter k1 dan k2 yang paling sesuai dilaporkan dalam Tabel 1. k1 bergantung pada konsentrasi, dengan nilai yang lebih besar untuk konsentrasi awal yang rendah (2,5 µM) daripada untuk konsentrasi awal yang lebih tinggi (10 dan 25 µM As(III)). Misalnya, pada pH 5,4, perbedaan relatif dalam nilai k1 adalah 45 % antara 2,5 dan 10 µM, dan 55% antara 2,5 dan 25 µM. Nilai k 1 untuk 10 dan 25 µM tidak berbeda secara signifikan di semua tingkat pH, dan tidak ada hubungan yang jelas antara k 1 dan pH yang diamati. Perbedaan relatif antara nilai k 1 dan k 2 menurun dengan meningkatnya konsentrasi As(III) awal. Pada pH 6,5, perbedaan ini adalah 95% untuk 2,5 µM, dibandingkan dengan 72% dan 76% untuk 10 dan 25 µM. Di luar tren ini, tidak ada pola sistematis dalam ketergantungan konsentrasi atau pH k 2 yang terlihat.
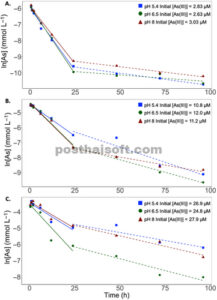
Penentuan konstanta laju orde pertama semu untuk kinetika adsorpsi As(III) pada resin Ambersep GT74 pada konsentrasi awal As(III) µM (A) rendah, (B) sedang, dan (C) tinggi pada setiap nilai pH dan dibagi menjadi fase cepat (garis utuh) dan fase lambat (garis putus-putus). Kotak biru = pH 5,4, lingkaran hijau = pH 6,5, segitiga merah = pH 8.
TABEL 1. Parameter model pseudo orde pertama sepotong-sepotong pada pH 5,4, 6,5, dan 8.
Parameter model kinetik orde pertama semu sepotong-sepotong pada pH 5,4
Konsentrasi awal As(III)
k1 (h − 1 )
k 2 (h -1 )
Kesalahan standar sisa R 2
2,83 µM
0,154 ± 1,06 × 10 − 2
b. 1,52 × 10−2 ± 1,15 × 10−3
0.22
0,062 tahun
0,98
0,99
10,8 µM
bd 8,52 × 10−2 ± 3,19 × 10−3
d. 4,05 × 10−2 ± 9,19 × 10−3
0,065 tahun
0.49
0,99
0,91
26,9 µM
bd 6,93 × 10−2 ± 1,10 × 10v −2
sekitar 1,97 × 10−2 ± 6,59 × 10−3
0.22
0.35
0,91
0.82
Parameter model kinetik orde pertama semu sepotong-sepotong pada pH 6,5
Konsentrasi awal As(III)
k1 (h − 1 )
k 2 (h -1 )
Kesalahan standar sisa R 2
2,63 µM
0,168 ± 2,26 × 10 − 3
b. 8,33 × 10− 3 ± 3,74 × 10− 3
0,046 tahun
0.20
0,99
0.71
12,0 µM
c 0,118 ± 1,00 × 10 − 2
sekitar 3,33 × 10− 2 ± 2,09 × 10− 3
0.20
0.11
0,97
0,99
24,8 µM
c0,120 ± 2,26 × 10 − 2
sekitar 2,90 × 10−2 ± 5,64 × 10−3
0.46
0.30
0,88
0,93
Parameter model kinetik orde pertama semu sepotong-sepotong pada pH 8
Konsentrasi awal As(III)
k1 (h − 1 )
k 2 (h -1 )
Kesalahan standar sisa R 2
3,03 µM
0,142 ± 6,45 × 10 − 3
SM 1,36 × 10− 2 ± 1,26 × 10− 3
0.13
0,067 tahun
0,99
0,98
11,2 µM
cd 0,119 ± 7,07 × 10 − 3
e 2,14 × 10 − 2 ± 3,11 × 10 − 3
0.14
0.17
0,99
0,96
27,9 µM
menjadi 6,56 × 10 − 2 ± 1,07 × 10 − 2
iklan 2,56 × 10 − 2 ± 3,33 × 10 − 3
0.22
0.18
0,90
0,97
Catatan : Superskrip di samping nilai k1 dan k2 menunjukkan perbedaan signifikan dari uji perbedaan signifikan jujur (HSD) Tukey.
Sebagian besar penelitian lingkungan tentang kinetika serapan As(III) berfokus pada permukaan mineral daripada ligan organik. Sejumlah penelitian sebelumnya tentang serapan As(III) pada tanah, oksida besi, dan mineral besi sulfida telah melaporkan fase “cepat” dan “lambat” yang serupa untuk reaksi serapan (Barrachina et al., 1996 ; Couture et al., 2013 ; Elkhatib et al., 1984 ; Raven et al., 1998 ). Fase “lambat” sering dikaitkan dengan difusi intra atau interpartikel. Di sini, data tidak memberikan penjelasan mekanistik untuk fenomena kinetika cepat dan lambat, tetapi masuk akal bahwa difusi intrapartikel ke situs pengikatan tiol yang terletak di dalam manik-manik Ambersep dapat menjelaskan pola ini. Studi kinetik serapan As(III) pada tiol telah dilaporkan untuk alumina teraktivasi (AA) dan AA fungsionalisasi tiol (AA-SH), dan serapan cepat awal diikuti oleh serapan lambat juga dilaporkan untuk sistem ini (Hao, Han, & Wang, 2009 ). Pada pH netral dan menggunakan konsentrasi As(III) awal 66,7 µM, Hao, Han, Wang, dan Meng ( 2009 ) menetapkan k1 , konstanta laju orde pertama semu untuk serapan As(III) pada AA dan AA-SH sebesar 0,31 dan 0,26 h −1 ; sementara itu, nilai k1 tertinggi studi kami ditetapkan sebesar 0,17 h −1 pada pH 6,5 dan menggunakan konsentrasi As(III) awal 2,63 µM . Penyerapan kontaminan ke dalam NOM tanah juga secara umum dianggap dibatasi oleh difusi (Pignatello & Xing, 1995 ).
3.3 Adsorpsi dan desorpsi
Isoterm adsorpsi dan kecocokan model Langmuir As(III) pada resin Ambersep pada tiga nilai pH berbeda ditunjukkan pada Gambar 2 (lingkaran biru). Nilai p Ka dan kerapatan situs tiol Ambersep dibandingkan dengan adsorben lain yang mengandung tiol pada Tabel S1 . Tabel S2 dan S4 merangkum parameter model Langmuir dan membandingkannya dengan penelitian dengan adsorben As umum lainnya. Fase awal isoterm yang curam pada konsentrasi As(III) kesetimbangan rendah mencerminkan afinitas tinggi Ambersep terhadap As(III). Nilai Q maks berkisar dari 0,047 ± 0,0045 hingga 0,053 ± 0,0065 mmol As(III)/g Ambersep, tanpa pola yang jelas terkait dengan pH. Kerapatan situs pengikatan tiol ditentukan melalui titrasi potensiometri (Gambar S1–S3 ) menjadi 0,34 mmol g −1 . Ini menghasilkan rasio As(III)/thiol sekitar 0,15:1. Dalam sebuah studi pada AA fungsionalisasi thiol, Hao, Han, dan Meng ( 2009 ) menetapkan rasio As(III)/thiol dalam eksperimen serapan berkisar dari 0,19:1 hingga 0,47:1 dengan ujung bawah rentang tersebut mirip dengan perkiraan kami. Hoffman dkk. ( 2014 ) menetapkan jumlah koordinasi As(III) yang terikat pada thiol Ambersep mendekati 3, konsisten dengan stoikiometri reaksi As(III):thiol 0,33:1 yang diamati untuk glutation (Spuches dkk., 2005 ). Temuan dari Abu-Ali dkk. ( 2022 ) selanjutnya menunjukkan bahwa pada rasio As(III)/karbon organik terlarut yang relevan secara lingkungan, kandungan sulfur organik yang lebih tinggi (S org ) dalam DOM meningkatkan kompleksasi, dan analisis plot Scatchard mengungkapkan kepadatan situs tiol yang bervariasi (0,0048–0,018 µmol mmol −1 C), yang menunjukkan bahwa tiol tetap berlebih bahkan pada konsentrasi As(III) yang tinggi, terutama dalam sistem yang kaya S org seperti tanah sawah. Sebaliknya, telah disarankan di tempat lain bahwa untuk permukaan dengan kepadatan tiol rendah, atau untuk molekul asam humat dengan struktur kaku, stoikiometri pengikatan 1:1 mungkin lebih mungkin terjadi (Catrouillet et al., 2015 ). Walaupun hasil kami tidak memberikan estimasi stoikiometri pengikatan As–S, hasil tersebut mengindikasikan bahwa pada rentang rasio pengikatan As(III):thiol yang masuk akal dari 0,33:1 hingga 1:1, thiol akan tetap berlebih ketika isoterm mengindikasikan bahwa permukaannya jenuh.
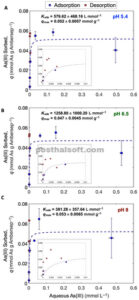
Isoterm sorpsi untuk As(III) pada resin Ambersep GT74 pada (A) pH 5,4, (B) pH 6,5, dan (C) pH 8 (lingkaran biru). Garis biru putus-putus menunjukkan kecocokan model Langmuir. Data dari percobaan desorpsi ditunjukkan sebagai kotak merah.
Data dari percobaan desorpsi juga ditunjukkan pada Gambar 2 (kotak merah). Ada perbedaan antara data adsorpsi dan desorpsi setelah 96 jam desorpsi, yang menunjukkan tingkat ireversibilitas dalam penyerapan As(III) pada Ambersep. Perbedaan antara data adsorpsi dan desorpsi khususnya terlihat pada konsentrasi As(III) kesetimbangan ≤2 µM, sementara pada konsentrasi sekitar 4 µM dan lebih tinggi, data desorpsi mulai konvergen dengan model isoterm adsorpsi (lihat gambar sisipan). Ini menunjukkan bahwa tingkat reversibilitas mungkin bergantung pada konsentrasi. “Histeresis desorpsi” seperti itu telah diamati dalam studi penyerapan As pada mineral (Zhang & Selim, 2005 ). Ireversibilitas penyerapan As pada permukaan ini telah dikaitkan dengan transpor terbatas difusi dari situs pengikatan, di antara mekanisme lainnya. Mekanisme ini sebagian selaras dengan data kinetik dua fase kami, yang menunjukkan bahwa difusi dapat membatasi akses ke beberapa situs pengikatan.
Sementara studi tentang pengikatan As(III) ke tiol dalam NOM atau material fungsional terbatas, telah ada lebih banyak penelitian tentang pengikatan As(III) ke tiol dalam protein, karena ini adalah mekanisme kunci toksisitas As(III) (Shen et al., 2013 ). Sejumlah studi dari literatur protein melaporkan bahwa pengikatan As(III) ke tiol dalam protein bersifat reversibel (Barchowsky et al., 1996 ; Chen et al., 2015 ; Jan et al., 2006 ; Liang & Drueckhammer, 2014 ), yang berbeda dari temuan kami yang menunjukkan tingkat ireversibilitas dalam pengikatan As(III)–Ambersep karena perbedaan antara data adsorpsi dan desorpsi pada konsentrasi As(III) kesetimbangan di bawah 2 µM. Eksperimen adsorpsi kompetitif dalam campuran dua-adsorben yang dilakukan di Hoffmann et al. menunjukkan bahwa distribusi As(III) antara permukaan Ambersep dan ferrihidrit bergantung pada adsorben tempat As(III) awalnya terikat, yang juga menunjukkan tingkat ketidakterbalikan dalam pengikatan As(III)–Ambersep. Ada kemungkinan bahwa ketidakterbalikan yang diamati dengan Ambersep disebabkan oleh akses terbatas difusi ke tempat pengikatan, yang secara umum sesuai dengan data kinetika dua fase yang kami amati, bukan karena ketidakterbalikan ikatan kimia. Penentuan pasti tentang alasan perilaku ini berada di luar cakupan kontribusi ini.
3.4 Reversibilitas adsorpsi As(III) pada Ambersep
Untuk menentukan tingkat pelepasan As(III) sebagai hasil dari proses desorpsi dengan resin Ambersep GT74, perhitungan dilakukan dengan mempertimbangkan konsentrasi As(III) dalam kesetimbangan setelah percobaan desorpsi, volume larutan, dan massa total As(III) yang awalnya diserap ke resin. Ketika konsentrasi As(III) dalam kesetimbangan dari desorpsi meningkat, persentase As(III) yang dilepaskan terus meningkat, dengan persentase tertinggi pada pH 6,5. Yang penting, tidak lebih dari 15% As(III) yang awalnya dimuat ke Ambersep terdesorpsi dari permukaan. Selain itu, ketika jumlah As(III) yang diserap meningkat, persentase As(III) rendah untuk setiap pH yang diuji.
Sejumlah penelitian telah menunjukkan bahwa pengikatan spesies As anorganik dan organik ke tiol dalam protein dan senyawa model lainnya (misalnya, glutation) bersifat reversibel (Delnomdedieu et al., 1993 ), tetapi hanya ada sedikit penelitian yang meneliti proses ini dengan tiol dalam NOM. Eksperimen adsorpsi kompetitif dalam campuran dua-adsorben yang dilakukan di Hoffmann et al. menunjukkan bahwa distribusi As(III) antara permukaan Ambersep dan ferrihidrit bergantung pada adsorben mana As(III) awalnya terikat. Hal ini sangat menunjukkan tingkat ireversibilitas dalam adsorpsi As(III) ke Ambersep. Di sini, kami menggunakan eksperimen sorpsi-desorpsi untuk memberikan bukti langsung bahwa pengikatan As(III) ke Ambersep sebagian besar bersifat ireversibel, setidaknya jika tidak ada sorben kompetitif yang kuat untuk As(III) (Delnomdedieu et al., 1994 ). Bukti untuk irreversibilitas paling kuat pada konsentrasi As(III) rendah dalam air, sementara pada konsentrasi As(III) yang lebih tinggi, data desorpsi konvergen dengan data adsorpsi. Hal ini menunjukkan bahwa tingkat reversibilitas mungkin bergantung pada konsentrasi. Oleh karena itu, aspek baru dari penelitian kami adalah temuan sorpsi ireversibel As(III) terhadap Ambersep GT74, setidaknya pada konsentrasi As(III) dalam air <2 µM, yang kemungkinan disebabkan oleh pembentukan kompleks bola-dalam (Pintor et al., 2020 ). Mekanisme adsorpsi bola-dalam ini selanjutnya didukung oleh kesamaan tingkat adsorpsi yang diuji pada kekuatan ionik yang berbeda antara 0,003 dan 0,3 M yang ditunjukkan pada Gambar S4 .
3.5 Implikasi lingkungan
Dalam penelitian ini, kami mempelajari adsorpsi dan desorpsi As(III) pada resin Ambersep GT74 yang difungsikan dengan tiol sebagai sistem model untuk memahami interaksi As(III) dengan ligan tiol pada NOM. Temuan ini menunjukkan bahwa penyerapan As(III) dicirikan oleh proses kinetik dua fase, dengan akses terbatas difusi ke tempat pengikatan yang berpotensi mengendalikan laju penyerapan. Khususnya, penyerapan ditemukan sebagian besar bersifat ireversibel pada konsentrasi As(III) kesetimbangan rendah, yang menunjukkan bahwa NOM yang kaya tiol dapat melumpuhkan As(III) dalam sistem alami. Ketidakterbalikan ini dapat mengurangi mobilitas dan bioavailabilitas As(III), mengurangi penyerapannya oleh tanaman di tanah pertanian, seperti sawah, tempat NOM melimpah.
Hasil ini juga menunjukkan bahwa gugus tiol dalam NOM dapat bertindak sebagai tempat penampungan penting bagi As(III), khususnya dalam lingkungan anaerobik tempat interaksi tersebut cenderung terjadi. Kurangnya pengaruh kekuatan ionik pada penyerapan lebih lanjut mendukung mekanisme kompleksasi bola dalam, yang memperkuat stabilitas interaksi ini dalam berbagai kondisi lingkungan. Dengan menjelaskan kinetika dan reversibilitas pengikatan As(III)–tiol, penelitian ini memberikan wawasan berharga tentang spesiasi, mobilitas, dan retensi arsenik dalam tanah yang kaya organik.
Temuan-temuan ini konsisten dengan penelitian-penelitian sebelumnya tentang interaksi logam(loid)-NOM, seperti karya Olk et al. ( 2019 ), yang menekankan peran fraksi humik dalam bahan organik tanah dalam mengendalikan perilaku logam(loid). Demikian pula, penelitian Liu et al. ( 2022 ) tentang Hg(II) dan HgS nanopartikel di tanah sawah selanjutnya menunjukkan pentingnya ligan-ligan berbasis sulfur, seperti gugus tiol, dalam spesiasi dan transformasi logam di tanah sawah. Bersama-sama, penelitian-penelitian ini menyoroti NOM yang kaya tiol sebagai mediator penting dalam retensi dan transformasi arsenik dan logam(loid) lain di tanah sawah. Memahami interaksi-interaksi ini memiliki implikasi penting untuk pengelolaan kontaminasi arsenik dalam sistem pertanian. Strategi-strategi yang ditujukan untuk meningkatkan atenuasi alami mobilitas dan bioavailabilitas arsenik melalui pengelolaan NOM dapat membantu mengurangi risiko-risiko terhadap kesehatan manusia yang terkait dengan paparan arsenik melalui padi dan tanaman-tanaman lain. Penelitian lebih lanjut diperlukan untuk mengeksplorasi peran komponen NOM lainnya dalam memodulasi mobilitas arsenik dan untuk memeriksa penerapan yang lebih luas dari temuan ini pada berbagai sistem tanah.
KONTRIBUSI PENULIS
Anita A. Sanchez : Konseptualisasi; kurasi data; analisis formal; investigasi; metodologi; validasi; visualisasi; penulisan—draf asli; penulisan—peninjauan dan penyuntingan. Matthew C. Reid : Akuisisi pendanaan; administrasi proyek; sumber daya; supervisi; validasi; penulisan—peninjauan dan penyuntingan.
UCAPAN TERIMA KASIH
Anita A. Sanchez mengucapkan terima kasih kepada Program Doktor Minoritas (MPHD) Alfred P. Sloan Foundation (Penghargaan hibah: G-2019-11435) dari Program Keragaman di bidang Teknik Cornell. Pendanaan tambahan untuk pekerjaan ini disediakan oleh NSF Award 1905175.
PERNYATAAN KONFLIK KEPENTINGAN
Penulis menyatakan tidak ada konflik kepentingan.
