Abstrak
Kontrol kualitas RNA menjadi semakin penting dengan munculnya vaksin dan terapi berbasis mRNA. Namun, metode konvensional seperti LC–MS sering kali memerlukan peralatan dan keahlian khusus, sehingga membatasi penerapannya pada eksperimen dengan hasil tinggi. Di sini, kami mengoptimalkan biosensor integritas RNA yang telah dikarakterisasi sebelumnya, yang memberikan keluaran kolorimetri sederhana, menggunakan Desain Eksperimen (DoE). Melalui putaran berulang Desain Penyaringan Definitif (DSD) dan validasi eksperimental, kami secara sistematis mengeksplorasi berbagai kondisi pengujian untuk meningkatkan kinerja biosensor. Optimalisasi menghasilkan peningkatan 4,1 kali lipat dalam rentang dinamis dan mengurangi persyaratan konsentrasi RNA hingga sepertiga, sehingga meningkatkan kegunaan secara signifikan. Modifikasi penting meliputi pengurangan konsentrasi protein reporter dan oligonukleotida poli-dT dan peningkatan konsentrasi DTT, yang menunjukkan lingkungan reduksi untuk fungsionalitas yang optimal. Yang terpenting, biosensor yang dioptimalkan mempertahankan kemampuannya untuk membedakan antara RNA yang tertutup dan tidak tertutup bahkan pada konsentrasi RNA yang lebih rendah. Secara keseluruhan, biosensor kami yang lebih baik menawarkan kinerja yang lebih baik dan pengurangan kebutuhan sampel, membuka jalan bagi pengendalian kualitas RNA yang cepat dan hemat biaya dalam berbagai situasi, termasuk lingkungan dengan sumber daya terbatas.
1. PENDAHULUAN
Dengan munculnya teknologi inovatif seperti vaksin mRNA dan terapi terkait, kontrol kualitas RNA menjadi semakin penting. 1 Tidak seperti DNA, RNA secara inheren kurang stabil karena strukturnya yang beruntai tunggal dan keberadaan gula ribosa, bukan gula deoksiribosa. Kerentanan gugus hidroksil dalam RNA terhadap hidrolisis semakin meningkatkan kemungkinan degradasinya. 2 Ketidakstabilan inheren ini mengharuskan persyaratan penyimpanan suhu sangat rendah awal untuk vaksin mRNA SARS-CoV-2, yang menimbulkan tantangan untuk distribusi di daerah pedesaan. 3 Akibatnya, ada kebutuhan mendesak untuk memastikan integritas RNA tidak hanya selama produksi, tetapi juga berpotensi pada titik penggunaan. Dengan demikian, menjadi penting untuk mengembangkan pengujian yang dapat dilakukan oleh non-ahli dan tanpa memerlukan peralatan khusus. Sementara RNA yang diproduksi melalui transkripsi in vitro (IVT) lebih stabil daripada mRNA in vivo, sebagian karena stabilitas yang diberikan oleh formulasi, salah satu masalah utama dengan mRNA IVT adalah kurangnya mesin capping alami, yang meningkatkan stabilitas RNA, efisiensi translasi, dan pengenalan imun. 4 Untuk mengimbangi hal ini, mRNA IVT ditutup setelah transkripsi melalui perlakuan enzimatik atau melalui transkripsi bersama dengan menambahkan analog cap kimia ke dalam reaksi. 5
Berbagai metode saat ini ada untuk menilai integritas RNA yang ditinjau dalam Ref. [ 6 ] termasuk elektroforesis gel, 7 , 8 mobilitas molekuler, amplifikasi templat, 9 , 10 hibridisasi oligonukleotida komplementer, 11 probe aptamer, 12 biosensor fluoresensi, 12 kromatografi cair 13 atau interaksi protein-RNA. 14 Teknik-teknik ini biasanya menghasilkan keluaran berdasarkan fluoresensi, refraksi/transmisi cahaya, atau arus listrik, sehingga menantang untuk diimplementasikan dalam pengaturan non-laboratorium. Meskipun biosensor telah dikembangkan untuk meningkatkan analisis diagnostik untuk integritas RNA, mereka masih memiliki keterbatasan tertentu. 15 , 16 Salah satu kesulitan dengan masing-masing teknik ini adalah bahwa mereka memerlukan peralatan khusus, dan profesional terlatih untuk melakukan eksperimen.
Sebelumnya, kami telah mengembangkan biosensor yang mampu mengenali struktur tutup m7G dan ekor poliA secara bersamaan untuk mengukur persentase RNA utuh dalam sampel. 17 Biosensor menggunakan protein chimeric yang direkayasa (B4E, fusi protein eIF4E murine dan β-laktamase) yang mengenali tutup 5′, dan manik-manik fungsionalisasi oligonukleotida deoksitimidina terbiotinilasi yang mengikat ekor poliA. Jika salah satu atau kedua komponen ini tidak ada, tidak ada sinyal yang diamati. Biosensor juga dirancang untuk menghasilkan perubahan warna sebagai keluaran yang dapat divisualisasikan, menjadikannya pendekatan berteknologi rendah yang tidak perlu digunakan dalam pengaturan berbasis laboratorium jika diinginkan. Meskipun biosensor ini tidak mampu menentukan total hasil RNA, ia akurat dalam mengamati degradasi. Namun, ada keterbatasan dalam panjang RNA yang dapat diamati secara akurat, dengan sinyal menurun untuk molekul RNA yang lebih panjang. Meskipun hal ini dapat dikompensasi dengan menggunakan peningkatan konsentrasi dalam pengujian, hal ini berarti bahwa lebih dari satu dosis vaksin RNA akan diperlukan untuk setiap pengujian kontrol kualitas. Di sini, untuk mengatasi keterbatasan ini, kami melakukan penyaringan berbagai kondisi menggunakan Design of Experiments (DoE) untuk meningkatkan batas deteksi biosensor dan rasio signal-to-noise dengan molekul RNA yang lebih panjang (Gambar 1 ).
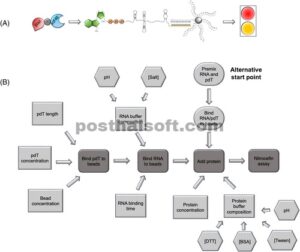
Desain eksperimen untuk optimasi pengujian biosensor. (a) Skema alur kerja pengujian biosensor, dengan pengikatan kompleks eIF4-β-laktamase ke tutup 5′ RNA. Keberadaan ekor poliA memungkinkan pengikatan ke oligonukleotida terbiotinilasi poli-dT yang terikat pada manik streptavidin. Pengembangan dengan nitrocefin menunjukkan perubahan warna dari kuning ke merah dengan adanya RNA berukuran penuh. (b) Diagram alir proses pengambilan keputusan untuk desain pengaturan eksperimen dengan berbagai komponen yang dimodifikasi. Abu-abu gelap menunjukkan alur kerja protokol, dengan bentuk oval menunjukkan titik awal alternatif untuk pengujian. Kotak persegi panjang adalah kondisi yang dapat diubah pada setiap langkah, dan jika beberapa komponen menjadi faktor dalam parameter yang dapat diubah ini, maka hal ini ditunjukkan dengan kotak heksagonal.
Kami memilih untuk menggunakan desain penyaringan definitif (DSD) untuk mengevaluasi komponen penting dari uji biosensor. Awalnya dijelaskan oleh Jones dan Nachtsheim, 18 desain faktor tiga tingkat ini menghilangkan bias efek sekunder sambil membatasi jumlah pengujian. Kami menetapkan total delapan faktor yang penting, yang menurut Jones dan Nachtsheim, berada di atas ambang batas di mana penggunaan DSD cukup untuk mencakup ruang desain yang sama dengan desain faktorial penuh. Desain penyaringan definitif sering digunakan untuk mengidentifikasi faktor-faktor utama yang memiliki dampak paling besar pada sistem, yang kemudian dapat dieksplorasi melalui penyaringan faktorial penuh. Namun, adalah mungkin untuk mengasah desain ruang menggunakan pengujian DSD iteratif untuk bergerak menuju yang optimal, ini bermanfaat jika beberapa komponen diidentifikasi sebagai signifikan yang akan membuat faktorial penuh melelahkan dan sulit dicapai. 19 Kami menggunakan model bertahap dengan titik henti kriteria informasi Bayesian (BIC) untuk menyesuaikan model regresi untuk DSD, yang telah terbukti menjadi metode paling akurat untuk prediksi di luar sampel. 19 – 21 Model ini menganalisis desain menggunakan analisis kuadrat penuh, memberikan indikasi efektor utama di samping interaksi dua faktor. 22 Dengan memasangkan DSD dengan validasi eksperimental selama beberapa putaran, kami telah menunjukkan pentingnya mengeksplorasi seluruh ruang desain saat merancang dan mengoptimalkan biosensor baru. Melalui DoE, kami telah membuat biosensor yang memiliki peningkatan 4,1 kali lipat dalam rentang dinamis dibandingkan dengan desain asli kami dan yang menggunakan RNA sepertiga lebih sedikit. Kedua perubahan tersebut meningkatkan kegunaan biosensor secara umum, tetapi juga dalam pengaturan non-laboratorium dengan meningkatkan sinyal biosensor, membuat perubahan lebih terlihat oleh mata.
2 BAHAN DAN METODE
2.1 Bahan kimia dan media
Strain bakteri dikulturkan dalam medium Lennox lysogeny broth (LB) (1% pepton dari kasein, 0,5% ekstrak ragi, 0,5% NaCl) yang ditambah dengan 37,5 μg mL −1 kanamisin atau 100 μg mL −1 ampisilin. Bahan kimia umum termasuk β-D-1-thiogalactopyranoside (IPTG), dithiothreitol (DTT), bovine serum albumin (BSA), dan phenylmethylsulfonyl fluoride (PMSF) dibeli dari Sigma Aldrich (Dorset, Inggris). Tween-20, Dynabeads™ MyOne™ Streptavidin T1, dan Oxoid™ nitrocefin dibeli dari ThermoFisher Scientific (Paisley, Inggris). Oligonukleotida disintesis oleh Invitrogen (Paisley, Inggris). Enzim restriksi dibeli dari New England Biolabs (Hertfordshire UK).
2.2 Strain dan plasmid
Manipulasi DNA rekombinan bakteri dilakukan pada strain Escherichia coli NEB 5-α (New England Biolabs). Ekspresi protein dilakukan pada BL21 (DE3, New England Biolabs). Plasmid pET28a-B4E (Addgene 162.067) dan pRSET-T3 telah dijelaskan sebelumnya. 17 DNA yang mengkode protein spike SARS-CoV2 dan urutan domain pengikat reseptor (RBD) disintesis oleh GeneArt™ Gene Synthesis (ThermoFisher Scientific). Plasmid CFPS-Spike dan CFPS-RBD dibuat menggunakan metode perakitan DNA Gibson 23 menggunakan plasmid CFPS-lucA 24 sebagai tulang punggung dan mengganti sisipan luciferase dengan urutan protein Spike dan RBD, masing-masing. Semua plasmid diverifikasi urutannya (Eurofins Genomics, Ebersberg, Jerman). Plasmid diekstraksi menggunakan kit mini prep Qiagen (Manchester, Inggris) dan fragmen linier dimurnikan menggunakan kit pembersihan dan konsentrat Zymo (Zymo Research, California, AS).
2.3 Produksi mRNA in vitro
Untuk transkripsi in vitro dari RNA yang ditutup dan tidak ditutup, pRSET-T3 dilinearisasi dengan PspXI dan plasmid CFPS-Spike atau CFPS-RBD dilinearisasi dengan NruI. mRNA yang ditutup disiapkan menggunakan kit HiScribe™ T7 ARCA (dengan tailing, New England Biolabs) sesuai dengan petunjuk pabrik. Secara singkat, reaksi dilakukan menggunakan 1 μg plasmid yang dilinearisasi selama 3 jam pada suhu 37 °C sebelum melanjutkan ke reaksi tailing dan langkah-langkah perlakuan DNase.
Untuk menghasilkan RNA tanpa tutup, 1 μg cetakan DNA yang dilinearisasi ditambahkan ke reaksi 200 μL yang berisi 1× buffer transkripsi dan 400 U RNA polimerase T7 (ThermoFisher Scientific), 1,5 mM masing-masing NTP (ThermoFisher Scientific) dan 80 U penghambat RNase murine (New England Biolabs). Reaksi diinkubasi pada suhu 37 °C semalaman. Cetakan DNA dihilangkan dengan pencernaan menggunakan 5 μL DNaseI (New England Biolabs) selama 1 jam pada suhu 37 °C.
Baik RNA yang ditutup maupun yang tidak ditutup dimurnikan menggunakan RNA Clean & Concentrator-25 (Zymo Research) untuk menghilangkan sisa buffer dan NTP. Kemurnian RNA diperiksa dengan visualisasi pada gel pemutih [8] dan kuantifikasi dilakukan menggunakan spektrofotometer.
2.4 Pelipatan ulang RNA
Sebelum digunakan dalam uji biosensor, sampel RNA dilipat ulang seperti yang dijelaskan sebelumnya untuk memulihkan struktur tersier. 17 , 25 Singkatnya, setelah pencairan, RNA diencerkan hingga konsentrasi yang dibutuhkan untuk percobaan dalam Buffer A (50 mM HEPES, 100 mM KCl, pH 7,4) atau seperti yang ditentukan oleh desain percobaan, dan diinkubasi pada suhu 80 °C selama 2 menit, diikuti dengan 2 menit lagi pada suhu 60 °C. MgCl2 ditambahkan hingga konsentrasi akhir 1 mM dan sampel diinkubasi selama 30 menit pada suhu 37 °C. Sampel disimpan di atas es sebelum digunakan.
2.5 Pemurnian protein
Plasmid pET28a-B4E ditransformasikan menjadi BL21 (DE3) dan ditumbuhkan semalam dalam LB yang mengandung 37,5 μg mL −1 kanamisin pada suhu 30 °C dengan pengocokan pada kecepatan 250 rpm. Keesokan paginya, 1,25% (v/v) dari kultur semalam digunakan untuk menginokulasi 200 mL media LB dalam labu 2 L dan ditumbuhkan pada suhu 25 °C hingga OD 600 sebesar 0,5–0,6 tercapai. Ekspresi B4E diinduksi dengan menambahkan IPTG hingga konsentrasi akhir 0,5 mM. Kultur dibiarkan tumbuh selama 16 jam pada suhu 25 °C, 250 rpm. Kultur disentrifugasi pada kecepatan 4000 ×g selama 20 menit pada suhu 4 °C. Supernatan dibuang, dan pelet disuspensikan kembali dalam 5 mL buffer lisis (50 mM NaH2PO4 , 1 M NaCl, 20 mM imidazole, 0,1% Triton-100X, 10 mM beta-merkaptoetanol, 5% gliserol) per 1 g berat sel basah, ditambah dengan 1 mM PMSF dan 1 mg mL −1 lisozim , dan diinkubasi pada suhu 4 °C selama 30 menit. Sel-sel diganggu oleh sonikasi selama 140 detik (10 detik aktif, 10 detik istirahat, amplitudo 35%) di atas es. Fraksi yang larut dikumpulkan dengan sentrifugasi pada 16.000 ×g selama 30 menit pada suhu 4 °C. Supernatan yang telah dibersihkan diinkubasi dengan 1 mL resin agarosa Ni-NTA 50% (Qiagen) per 4 mL lisat selama 1 jam pada suhu 4 °C dengan pengadukan yang lembut. Sampel dan resin dimasukkan ke dalam kolom polipropilena dan larutan lisis dibersihkan melalui aliran gravitasi. Kolom dicuci dua kali dengan 4 mL buffer pencuci (50 mM NaH2PO4 , 1 M NaCl, 50 mM imidazol, 5% gliserol ) . Akhirnya, total lima fraksi elusi dikumpulkan dalam dua langkah: dua fraksi 0,3 mL menggunakan buffer elusi 1 (50 mM NaH2PO4 , 1 M NaCl , 5% gliserol, 75 mM imidazol) dan tiga fraksi 0,3 mL menggunakan buffer elusi 2 (50 mM NaH2PO4 , 1 M NaCl, 5% gliserol, 250 mM imidazol ) .
Fraksi-fraksi tersebut diperiksa kemurniannya menggunakan gel SDS-PAGE dan fraksi-fraksi dengan konsentrasi protein tertinggi digabungkan dan buffer ditukar sebanyak tiga kali ke dalam buffer penyimpanan protein (50 mM HEPES, 100 mM KCl, 10% (v/v) gliserol) menggunakan kolom sentrifugal Amicon® Ultra-15 MWCO 30 KDa (Sigma Aldrich). Kolom sentrifugal digunakan untuk mengonsentrasikan protein hingga 200 μL dan konsentrasi akhir diukur menggunakan kit uji protein Pierce™ BCA (ThermoFisher Scientific).
2.6 Pengujian biosensor
Uji biosensor dasar dilakukan seperti yang dijelaskan sebelumnya 17 dengan semua modifikasi yang dinyatakan dalam deskripsi percobaan. Semua langkah inkubasi dilakukan pada suhu ruangan pada rotator pada 60 rpm. Secara singkat, dalam tabung PCR, 10 μL Dynabeads™ MyOne™ Streptavidin T1 dicuci tiga kali dengan 20 μL Buffer A (50 mM HEPES, 100 mM KCl, pH 7,4) menggunakan rak magnetik. Manik-manik tersebut kemudian disuspensikan kembali dalam 20 μL Buffer A 2× (100 mM HEPES, 200 mM KCl, pH 7,4). 20 μL poli-dT terbiotinilasi 3,75 μM (pdT25) dalam air bebas RNase ditambahkan dan diinkubasi selama 10 menit. Manik-manik dicuci dengan 20 μL Buffer A, sebelum 20 μL sampel RNA yang dilipat ulang pada konsentrasi 0,3 μM ditambahkan dan diinkubasi selama 20 menit. Manik-manik kemudian dicuci dengan 100 μL Buffer B (33 mM HEPES, 66 mM KCl, 0,1% BSA, 0,1% Tween-20, 6 mM DTT, pH 7,4) sebelum 50 μL 0,45 μM B4E yang diencerkan dalam Buffer B ditambahkan dan diinkubasi selama 1 jam. Protein yang tidak terikat dihilangkan dengan tiga kali pencucian dengan 200 μL Buffer B. Manik-manik yang dicuci disuspensikan kembali dalam 200 μL Buffer A yang 8 μL di antaranya digunakan dalam uji nitrocefin.
2.7 Uji Nitrocefin
Sebanyak 192 μL larutan nitrocefin 0,1 mM (dalam buffer fosfat 50 mM, pH 7) dicampur dengan 8 μL manik-manik dalam pelat 96-sumur. Absorbansi pada 492 nm dipantau dari waktu ke waktu menggunakan pembaca pelat CLARIOstar (BMG Labtech Ltd., Aylesbury, Inggris). Pembacaan dikumpulkan setiap 1 menit selama 90 menit. Semua uji biosensor dijalankan dalam rangkap tiga dan mencakup kontrol negatif yang mengganti RNA yang ditutup dengan RNA yang tidak ditutup.
2.8 Desain percobaan
DSD tiga tingkat digunakan untuk menentukan pentingnya setiap komponen dalam desain eksperimen menggunakan perangkat lunak JMP Pro 15 (JMP UK & Western Europe, Marlow, UK). Sembilan faktor dipilih berdasarkan pra-penyaringan untuk menentukan dampak faktor pada uji biosensor. Faktor yang dipilih adalah konsentrasi garam dan pH buffer RNA, konsentrasi oligo pdT 25 , konsentrasi protein B4E, konsentrasi BSA, Tween-20, dan DTT dalam buffer protein dan konsentrasi garam dan pH buffer protein (Gambar 1 ). Batas atas dan bawah ditentukan secara eksperimental. Regresi langkah maju menggunakan titik henti kriteria informasi Bayesian (BIC) dengan nilai – p 0,1 dilakukan menggunakan JMP untuk menyesuaikan model regresi untuk DSD. Data dari uji biosensor diubah dalam salah satu dari tiga cara yang digunakan untuk menyesuaikan model: (i) penyesuaian akhir, di mana pembacaan absorbansi biosensor akhir setelah 90 menit dikoreksi dengan mengurangi kontrol negatif, (ii) rasio akhir, di mana pembacaan absorbansi biosensor akhir setelah 90 menit dibagi dengan kontrol negatif, dan (iii) penyesuaian tengah di mana nilai absorbansi setelah 10 menit dikoreksi dengan mengurangi kontrol negatif. Model DSD dijalankan sebanyak 4 kali dengan setiap putaran mencakup data dari semua putaran sebelumnya.
3 HASIL DAN PEMBAHASAN
3.1 Memaksimalkan penangkapan RNA untuk meningkatkan kekuatan sinyal
Sebelum menggunakan DoE untuk mengoptimalkan biosensor RNA, tiga faktor yang tidak sesuai dalam kerangka DSD diselidiki secara terpisah untuk menentukan dampaknya pada pengujian (Gambar 2 ). Kami berhipotesis bahwa efisiensi penangkapan RNA dapat dikurangi karena halangan sterik pada permukaan manik dan hal ini dapat membatasi reaksi pembangkitan sinyal secara keseluruhan yang memengaruhi rasio sinyal terhadap derau dan batas deteksi. Oleh karena itu, kami memeriksa tiga faktor yang terkait dengan peningkatan penangkapan RNA. Yang pertama adalah konsentrasi manik yang digunakan dalam langkah penangkapan RNA awal. Kondisi dasar menggunakan 10 μL bubur Dynabeads™ MyOne™ Streptavidin T1. Konsentrasi ini ditingkatkan dan diturunkan untuk mengamati apakah pengikatan RNA dapat ditingkatkan, sehingga mengubah karakteristik biosensor (Gambar 2a ). Misalnya, menggunakan lebih sedikit manik dalam langkah penangkapan dapat menghasilkan kepadatan RNA yang lebih tinggi pada permukaan penyangga dan ini dapat menghasilkan sinyal yang lebih tinggi. Alternatifnya, jika halangan sterik pada permukaan manik-manik karena cakupan RNA yang tinggi mencegah langkah pengikatan hilir terjadi secara efisien, maka meningkatkan jumlah manik-manik dalam langkah penangkapan dapat meningkatkan sinyal dengan mengurangi kepadatan RNA. Oleh karena itu, kami mengevaluasi volume bubur manik-manik berkisar antara 2 hingga 20 μL dalam langkah penangkapan RNA. Mengurangi jumlah manik-manik menurunkan sinyal dari biosensor, dengan pengujian yang mengandung 2 μL bubur manik-manik dalam langkah penangkapan awal hanya menunjukkan 30% dari aktivitas kondisi dasar pada akhir reaksi 90 menit, sedangkan menggunakan 5 μL bubur manik-manik mempertahankan 65% aktivitas. Menariknya, pengujian yang mengandung 15 μL bubur manik-manik tidak mengikuti tren linier ini dan menunjukkan pengurangan aktivitas sebesar 18% dibandingkan dengan kondisi awal. Peningkatan volume bubur manik yang digunakan pada langkah penangkapan awal hingga 20 μL memang menunjukkan peningkatan aktivitas sekitar 7% dibandingkan dengan kondisi dasar, tetapi ini tidak signifikan secara statistik menggunakan uji-t tak berpasangan ( p = 0,143). Selain itu, dengan mempertimbangkan biaya manik, kami memutuskan bahwa peningkatan ini tidak cukup untuk menjamin biaya tambahan yang akan dikaitkan dengan penggandaan konsentrasi manik pada langkah penangkapan.

Memaksimalkan penangkapan RNA awal untuk meningkatkan fungsionalitas uji biosensor. (a) Mengubah volume manik-manik yang digunakan dalam penangkapan RNA memengaruhi penangkapan RNA. Volume bubur manik-manik berkisar antara 2 hingga 20 μL digunakan. Sampel dijalankan dalam rangkap tiga (ditutup) dan disesuaikan untuk kontrol negatif (tidak ditutup). (b) Meningkatkan panjang oligo poli-dT menggunakan urutan DNA acak sebagai pengisi mengurangi sinyal biosensor. Oligo dari 25 nukleotida (semua dT) atau 50 nukleotida (25 dT ditambah 25 nukleotida acak) digunakan. Batang kesalahan adalah simpangan baku reaksi rangkap tiga dari yang ditutup dan tidak ditutup (kontrol negatif). (c) Preinkubasi RNA dengan oligo poli-dT mengurangi sinyal biosensor. Tiga kondisi dijalankan; kondisi standar pengikatan awal pdT25 ke manik streptavidin, inkubasi RNA dan pdT25 bersama-sama dalam kondisi standar (Premix 1), inkubasi RNA dan pdT25 bersama-sama dan penghilangan langkah resuspensi dalam Buffer A (Premix 2). Batang galat adalah deviasi standar dari reaksi rangkap tiga dari yang ditutup dan tidak ditutup (kontrol negatif).
Faktor kedua yang kami selidiki adalah jarak antara permukaan manik dan oligo dT yang digunakan untuk menangkap RNA. Dalam desain asli, digunakan oligo poli-dT 25 nukleotida terbiotinilasi. 17 Namun, kami berhipotesis bahwa memindahkan dT lebih jauh dari permukaan dapat meningkatkan penangkapan RNA dengan memberikan fleksibilitas yang lebih besar dan mengurangi halangan sterik. Oleh karena itu, spacer 25 nukleotida ditambahkan antara biotin dan urutan poli-dT. Spacer dirancang menggunakan generator DNA acak untuk memastikan tidak ada bias, struktur sekunder, atau interaksi diri yang diperkenalkan (Tabel S1 ). Kedua oligo dibandingkan dalam uji biosensor standar (Gambar 2b ). Bertentangan dengan hipotesis kami bahwa memperkenalkan spacer dapat mengurangi halangan sterik, tampak jelas bahwa oligo yang lebih panjang secara signifikan menghambat sinyal biosensor (sekitar ~35%). Oleh karena itu, oligo poli-dT awal (pdT 25 ) digunakan untuk studi optimasi.
Akhirnya, pengujian biosensor melibatkan penangkapan RNA melalui oligo poli-dT yang telah terikat pada manik-manik. Akan tetapi, ada kemungkinan bahwa konformasi 3D RNA mencegahnya mengikat secara efisien. Oleh karena itu, kami menguji apakah pra-inkubasi oligo poli-dT dengan RNA, diikuti dengan pengikatan kompleks ke manik-manik streptavidin akan meningkatkan karakteristik biosensor. Dua percobaan pra-inkubasi yang berbeda dilakukan. Dalam kedua kasus, 0,3 μg RNA dan 0,3 μM oligo poli-dT dicampur pada suhu ruangan selama 30 menit pada rotator pada kecepatan 60 rpm diikuti dengan pencampuran dengan manik-manik. Selanjutnya, manik-manik dicuci dan disuspensikan kembali dalam buffer 2X A (Premix 1) seperti pada pengujian dasar atau langkah ini dihilangkan (Premix 2). Gambar 2c menunjukkan bahwa sinyal biosensor berkurang pada kedua kondisi pengujian. Ada kemungkinan bahwa prainkubasi mencegah pengikatan kompleks oligo RNA-poli-dT ke manik-manik streptavidin. Mengabaikan langkah di mana manik-manik disuspensikan kembali dalam buffer 2X A (Premix 2), secara signifikan mengurangi efektivitas biosensor ( uji- t tak berpasangan pada titik akhir p = 0,0002), yang selanjutnya menyoroti pentingnya langkah ini dalam pengujian. Oleh karena itu, penambahan komponen dibiarkan seperti pada pengujian dasar (Gambar 1b ) untuk eksperimen optimasi.
3.2 Desain penyaringan definitif untuk pengujian biosensor RNA yang lebih baik
Untuk setiap DoE, ruang desain perlu ditetapkan terlebih dahulu dengan batas atas dan bawah dipilih sehingga semua hasil yang dirancang menghasilkan sinyal bukan nol. Kami awalnya memilih sembilan faktor yang dianggap penting untuk pengujian: konsentrasi garam dan pH buffer RNA, konsentrasi pdT 25 , pH dan konsentrasi garam, BSA, Tween-20 dan DTT dalam buffer protein, dan konsentrasi protein B4E. Pekerjaan kami sebelumnya telah menetapkan rentang pH protein dan buffer RNA dan konsentrasi protein B4E dan pdT25 yang dapat digunakan dalam penyaringan. 17 Namun, untuk lima kondisi yang tersisa, batas atas dan bawah diuji pada dua titik waktu yang berbeda untuk mengidentifikasi rentang yang sesuai (Gambar 3 , Gambar S1 ). Masing-masing kondisi batas bawah, tengah, dan atas untuk masing-masing faktor memberikan sinyal bukan nol, dengan dampak yang berbeda pada pengujian dan, seperti yang diharapkan, tidak selalu ada korelasi linier antara faktor dan sinyal biosensor (Gambar 3 ). Perubahan konsentrasi KCl dalam buffer protein (Gambar 3b ) tidak berdampak signifikan pada pengujian, dengan perbedaan kurang dari 0,2 unit absorbansi pada ketiga kondisi, dan akibatnya konsentrasi tersebut dihilangkan dari DSD. Untuk faktor lainnya, kami menggunakan kondisi yang ditetapkan sebagai batas atas dan batas bawah.

Menetapkan batas atas dan bawah untuk desain penyaringan definitif. Rata-rata Abs492 yang diambil pada 1200 detik atau 6460 detik dari uji biosensor diplot terhadap kondisi rendah, sedang, atau tinggi untuk setiap faktor ( n = 3). (a) Konsentrasi garam dalam buffer RNA, (b) Konsentrasi garam dalam buffer protein, (c) Konsentrasi BSA (%), (d) Konsentrasi Tween-20 (%), (e) Konsentrasi DTT (mM).
Delapan kondisi yang tersisa dimasukkan ke dalam program JMP Pro 15 DSD dengan batas bawah, tengah, dan atas yang telah ditentukan sebelumnya (Tabel S2 ). Pengujian dibagi menjadi tiga blok dengan pengujian tengah disertakan untuk memantau variabilitas dan empat pengujian tambahan disertakan oleh perangkat lunak JMP untuk memperluas ruang desain, sehingga totalnya ada 23 reaksi (Tabel 1 ). Pengujian tengah disertakan sebagai komponen model dan blok diskalakan sesuai dengan itu untuk mempertimbangkan perbedaan yang terjadi dari menjalankan eksperimen pada hari yang berbeda (Gambar S2B , S2P , S2R ). Setiap eksperimen menyertakan kontrol negatif, untuk memastikan bahwa perubahan yang diamati bukan karena peningkatan sinyal latar belakang terlepas dari keberadaan RNA (Gambar S2 ). Untuk memutuskan keluaran mana yang akan digunakan dalam pemasangan model, kami mempertimbangkan berbagai faktor. Pertama, sementara kami tertarik pada kondisi pengujian yang menyebabkan peningkatan sinyal, seperti yang ditunjukkan sebelumnya, kami tidak ingin hal ini mengorbankan latar belakang yang tinggi, jadi pemasangan model pada absorbansi maksimum tidaklah cukup. Misalnya, pada Gambar S2E , baik sinyal maupun latar belakangnya tinggi, yang menunjukkan kondisi yang buruk. Oleh karena itu, kami menguji berbagai transformasi sinyal terhadap kontrol negatif, baik penyesuaian, di mana kontrol negatif dikurangi (‘penyesuaian akhir’), atau rasio di mana sinyal dibagi dengan kontrol negatif (mirip dengan rasio sinyal terhadap derau, ‘rasio akhir’). Kami juga mempertimbangkan apakah kami dapat mengidentifikasi kondisi yang menyebabkan laju reaksi awal yang lebih cepat, dengan menyesuaikan model dengan keluaran pada titik waktu awal reaksi ( t = 10 menit, ‘penyesuaian tengah’), daripada titik akhir. Semua model dijalankan sebagai model regresi langkah maju menggunakan nilai p sebesar 0,1.
TABEL 1. Desain penyaringan definitif untuk 23 pengujian awal termasuk pengujian pusat untuk tiga blok dan empat pengujian tambahan.
Blok RNA [NaCl] Bahasa Inggris pH-nya [pdT25] μM [Protein] μM BSA (%) Usia remaja-20 (%) [DTT] mM pH-Protein
1 1 150 9 10 0.122 1 0.1 10 6
2 1 100 7.5 5.5 0,366 tahun 0,55 0,55 5.5 7.5
3 1 150 6 1 0,366 tahun 1 1 10 9
4 1 50 6 1 0.61 0.1 1 1 9
5 1 150 9 1 0.61 0.1 1 5.5 6
6 1 100 6 1 0.122 0.1 0.1 1 6
7 1 50 9 10 0,366 tahun 0.1 0.1 1 6
8 1 50 6 10 0.122 1 0.1 5.5 9
9 1 100 9 10 0.61 1 1 10 9
10 2 150 9 1 0.61 1 0.1 1 7.5
11 2 50 6 10 0.122 0.1 1 10 7.5
12 2 150 6 10 0.61 0,55 0.1 1 9
13 2 50 7.5 10 0.61 1 1 1 6
14 2 150 7.5 1 0.122 0.1 0.1 10 9
15 2 50 9 1 0.122 0,55 1 10 6
16 2 100 7.5 5.5 0,366 tahun 0,55 0,55 5.5 7.5
17 3 50 6 1 0.61 1 0.1 10 6
18 3 100 7.5 5.5 0,366 tahun 0,55 0,55 5.5 7.5
19 3 150 9 10 0.122 0.1 1 1 9
20 3 50 9 5.5 0.61 0.1 0.1 10 9
21 3 50 9 1 0.122 1 0,55 1 9
22 3 150 6 10 0.61 0.1 0,55 10 6
23 3 150 6 5.5 0.122 1 1 1 6
Ketiga model tersebut masing-masing mengidentifikasi faktor kunci yang berbeda. Misalnya, model ‘end adjusted’ mengidentifikasi konsentrasi DTT dan pdT 25 serta interaksi orde kedua dari pH buffer protein dengan dirinya sendiri dan konsentrasi DTT sebagai komponen penyumbang utama (Gambar S3 ). Model ‘end ratio’ juga mengidentifikasi konsentrasi pdT 25 dan interaksi orde kedua dari pH buffer protein sebagai hal yang penting, bersama dengan pH buffer protein. Akhirnya, model ‘mid adjusted’ mengidentifikasi sejumlah besar faktor signifikan secara statistik, beberapa di antaranya tumpang tindih dengan model lainnya (misalnya, konsentrasi DTT dan pdT 25 ) dan beberapa di antaranya tidak (misalnya, pH buffer RNA, konsentrasi garam buffer RNA, interaksi orde kedua dari konsentrasi garam RNA dan konsentrasi protein, untuk daftar lengkap lihat Gambar S4A ). Untuk menentukan model mana yang paling sesuai dengan tujuan peningkatan biosensor RNA, masing-masing digunakan untuk memprediksi kondisi yang memaksimalkan nilai ‘rasio akhir’, ‘penyesuaian akhir’ atau ‘penyesuaian tengah’, masing-masing (Tabel S3 ), dan serangkaian reaksi yang sesuai dengan kondisi ini dijalankan (Gambar 4a,b , Gambar S4B ). Untuk masing-masing, disertakan uji coba dengan kondisi dasar 17 , serta uji coba surplus yang diidentifikasi dengan cara alternatif untuk menyesuaikan model guna menyediakan data tambahan untuk penyempurnaan (misalnya, menggunakan penyesuaian standar alih-alih regresi bertahap).
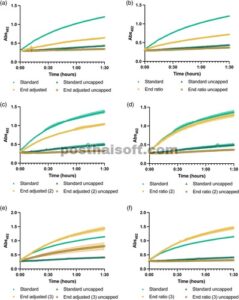
Kurva respons uji biosensor menggunakan kondisi yang disarankan dari desain penyaringan definitif menggunakan berbagai algoritme model. Batang galat adalah deviasi standar dari reaksi rangkap tiga. (a) Model akhir yang disesuaikan putaran 1, (b) Model rasio akhir putaran 1, (c) Model akhir yang disesuaikan putaran 2, (d) Model rasio akhir putaran 2, (e) Model akhir yang disesuaikan putaran 3, (f) Model rasio akhir putaran 3.
Yang langsung terlihat adalah bahwa penggunaan kondisi yang ditunjukkan oleh model ‘mid adjusted’ meningkatkan kecepatan respons biosensor, tetapi juga meningkatkan sinyal latar belakang kontrol negatif (Gambar S4B ). Oleh karena itu, ini bukan model yang sesuai untuk peningkatan biosensor RNA dan model ini dihapus dari semua analisis mendatang. Kondisi yang disarankan oleh model ‘end adjusted’ dan ‘end ratio’ menghasilkan penurunan absorbansi absolut dibandingkan dengan kondisi awal; namun, kontrol negatif juga berkurang (Gambar 4a,b ), yang menghasilkan rasio signal-to-noise yang lebih baik.
Berikutnya, kedua model ‘end adjusted’ dan ‘end ratio’ dijalankan lagi dengan menggabungkan data tambahan dari percobaan yang dioptimalkan (Tabel S4 ), dengan total 29 kali percobaan termasuk satu kali percobaan tengah tambahan (Gambar S3C,D ). Untuk kedua model, faktor yang paling penting adalah interaksi dua faktor dari konsentrasi protein dengan dirinya sendiri. Sementara ada kesamaan lain, seperti signifikansi interaksi antara pH buffer protein dengan dirinya sendiri, dan interaksi dua faktor antara pdT25 dan Tween, ada juga beberapa perbedaan, seperti konsentrasi BSA yang signifikan dalam model ‘end ratio’ tetapi tidak dalam model ‘end adjusted’. Selain itu, jumlah komponen yang diidentifikasi sebagai signifikan secara statistik oleh model ‘end ratio’ lebih tinggi (12 vs. 10). Sekali lagi, kedua model digunakan untuk menyarankan kondisi yang dioptimalkan (Gambar 4c,d ). Meskipun tidak ada satu pun rangkaian kondisi yang menunjukkan peningkatan sinyal biosensor dibandingkan dengan kondisi dasar, keduanya menunjukkan penurunan absorbansi absolut dari kontrol negatif, yang mengarah pada peningkatan lebih lanjut dalam rasio sinyal terhadap derau (2,74 untuk kondisi dasar, 3,11 untuk kondisi yang disarankan oleh model ‘penyesuaian akhir’, dan 3,51 untuk kondisi yang disarankan oleh model ‘rasio akhir’). Pengurangan latar belakang pengujian menyebabkan peningkatan dalam rentang dinamis biosensor yang menunjukkan kedua model cocok untuk mengeksplorasi pengoptimalan lebih lanjut.
Karena perbaikan yang diamati pada putaran kedua, putaran ketiga optimasi dilakukan, lagi-lagi menggunakan data yang dihasilkan sebelumnya, serta menggabungkan data dari putaran 2 dari kondisi yang disarankan oleh kedua model (Tabel S5 ). Hal ini menghasilkan 5 kondisi tambahan dengan total 34 kali pengujian, yang ditetapkan pada 5 blok dengan 5 titik pusat disertakan (Gambar S3E,F ). Faktor serupa memiliki dampak signifikan pada model seperti pada iterasi sebelumnya, seperti interaksi dua faktor konsentrasi protein dengan dirinya sendiri, tetapi sedangkan sebelumnya kedua model menunjukkan interaksi antara pdT 25 dan Tween menjadi signifikan, hanya model ‘rasio akhir’ yang menunjukkan bahwa ini adalah komponen signifikan pada putaran 3.
Kondisi yang disarankan oleh kedua model menghasilkan peningkatan absorbansi absolut dari biosensor RNA (Gambar 4e,f ). Untuk kondisi yang disarankan dari model ‘end adjusted’, absorbansi titik akhir sebesar 1,44 teramati, dibandingkan dengan 1,15 dari kondisi dasar. Ini serupa dengan kondisi yang disarankan oleh model ‘end ratio’, yang memberikan absorbansi titik akhir sebesar 1,46. Keduanya menunjukkan peningkatan sinyal sekitar 25% dibandingkan dengan kondisi dasar. Namun, model ‘end adjusted’ juga menunjukkan peningkatan pada garis dasar kontrol negatif, yang berarti rasio sinyal terhadap derau berkurang dari 2,77 menjadi 1,77. Secara komparatif, kontrol negatif dari kondisi yang disarankan oleh model ‘end ratio’ mempertahankan sinyal yang berkurang seperti yang terlihat dari putaran kedua optimasi, menghasilkan rasio sinyal terhadap derau sebesar 4,71. Ini merupakan peningkatan sebesar 1,7 kali lipat dibandingkan dengan kondisi dasar. Hal ini menunjukkan model ‘rasio akhir’ lebih baik menangkap interaksi antara sinyal dan latar belakang.
Untuk menentukan apakah kondisi (Tabel S6 ) telah konvergen, model ‘rasio akhir’ dijalankan sekali lagi, diisi dengan data dari optimasi sebelumnya, dengan total 39 kali pengujian di 6 blok dengan 6 titik pusat. Ada konvergensi yang hampir sama dengan kondisi sebelumnya (Tabel S5 ); satu-satunya perbedaan adalah pengurangan konsentrasi protein dari 0,45 menjadi 0,2 μM (Gambar S5 ). Hal ini memberikan keyakinan bahwa kondisi yang telah kami identifikasi adalah optimum lokal untuk memaksimalkan sinyal dan rasio sinyal terhadap derau dari biosensor RNA.
3.3 Dampak desain baru pada persyaratan konsentrasi sampel RNA
Untuk menguji fungsionalitas biosensor, kami mencampur rasio yang berbeda dari RNA yang ditutup dan tidak ditutup untuk mengamati apakah biosensor mampu membedakan perbedaan dalam kualitas RNA (Gambar 5a ). Lebih jauh, kami tertarik untuk mengamati bagaimana batas deteksi berubah dengan panjang RNA yang berbeda, karena sebelumnya kami mengamati bahwa sinyal berkurang dengan urutan RNA yang lebih panjang. 17 Oleh karena itu, selain menggunakan templat linierisasi pRSET-T3, kami juga menggunakan dua templat tambahan, templat CFPS-RBD (ekspresi domain pengikatan reseptor dari SARS-CoV2 yang dimediasi IRES), dan templat CFPS-Spike (ekspresi protein lonjakan yang dimediasi IRES), yang menghasilkan RNA 700 nt dan 3800 nt, masing-masing (Gambar 5 ). Kondisi optimal kami mengakibatkan ketidakmampuan biosensor untuk secara akurat membedakan antara RNA yang 100% ditutup dan yang hanya 80% ditutup. Untuk target pRSET-T3, tidak ada perbedaan signifikan dalam sinyal antara keduanya. Yang lebih menarik, baik CFPS-RBD maupun CFPS-Spike RNA menunjukkan sinyal yang lebih tinggi untuk sampel dengan 80% RNA yang dilapisi dibandingkan dengan sampel dengan 100% RNA yang dilapisi. Pembalikan ini menunjukkan kepada kami bahwa sinyal tersebut mungkin sekarang terlalu jenuh dan bahwa mengurangi konsentrasi RNA, yang pada akhirnya akan bermanfaat untuk setiap uji penyaringan, terutama dengan RNA panjang seperti vaksin, dapat meningkatkan sistem.

Pengujian biosensor menggunakan berbagai konsentrasi RNA yang dibungkus dengan panjang yang berbeda. (a) RNA pRSET-T3 (2700 nt, (b) RNA CFPS-RBD (700 nt), (c) RNA CFPS-Spike (3800 nt). Batang kesalahan adalah deviasi standar dari reaksi rangkap tiga.
Untuk menguji hipotesis kami bahwa menurunkan konsentrasi RNA yang digunakan dalam uji biosensor akan memulihkan kemampuannya untuk membedakan antara sampel dengan jumlah RNA yang lebih besar, sampel yang mengandung pRSET-T3 dan CFPS-Spike RNA dijalankan menggunakan konsentrasi total 0,3, 0,2, dan 0,1 μM dengan 80% atau 100% capping (Gambar 6 ). Kedua konsentrasi RNA yang lebih rendah memulihkan kemampuan biosensor untuk dapat membedakan antara RNA yang 100% tertutup dan 80% tertutup. Namun, untuk konsentrasi total 0,1 μM RNA pRSET-T3, sinyal absorbansi akhir berkurang, dan oleh karena itu kami mengusulkan penggunaan RNA 0,2 μM untuk semua uji mendatang.

Mengurangi konsentrasi RNA meningkatkan fungsionalitas uji biosensor dengan kondisi yang dioptimalkan. (a) pRSET 0,1 μM RNA, (b) pRSET 0,2 μM RNA, (c) pRSET 0,3 μM RNA, (d) Spike 0,1 μM RNA, (e) Spike 0,2 μM RNA, (f) Spike 0,3 μM RNA. Batang galat adalah deviasi standar dari reaksi rangkap tiga.
4 DISKUSI
Desain eksperimen memungkinkan kami untuk mengevaluasi ruang desain yang besar untuk perbaikan uji biosensor guna menilai pembatasan dan integritas RNA. Salah satu aspek yang paling menarik adalah seberapa tangguh kondisi awal, dengan beberapa iterasi model DoE yang diperlukan sebelum kondisi tersebut mengalahkan kondisi awal dalam rasio signal-to-noise dan batas deteksi. Modifikasi penting adalah penurunan pada protein B4E dan konsentrasi pdT 25 , serta peningkatan jumlah DTT yang diperlukan, yang menunjukkan lingkungan reduksi sebagai kondisi terbaik untuk fungsionalitas penuh. Penurunan konsentrasi pdT 25 mungkin sebagian bertanggung jawab atas perilaku oversaturasi pada konsentrasi RNA tinggi dalam kondisi yang dioptimalkan. Selain itu, oligomerisasi diri B4E melalui pembentukan ikatan disulfida sebelumnya telah diamati selama pemurnian, 26 yang berpotensi dicegah melalui peningkatan konsentrasi DTT.
Peningkatan kondisi biosensor menghasilkan pengurangan jumlah RNA yang dibutuhkan untuk pengujian. Efek yang tidak terduga ini pada akhirnya akan bermanfaat terutama saat menangani RNA yang lebih panjang, seperti vaksin mRNA Covid19 yang panjangnya 4284 nukleotida. 27 Perbedaan ini memiliki dampak yang substansial, pengurangan sepertiga penggunaan RNA, terlepas dari panjangnya, akan mengurangi jumlah material yang dibutuhkan untuk pengujian, yang berpotensi meningkatkan kelayakan penggunaan pengujian ini untuk pengoptimalan proses manufaktur, penyaringan dengan hasil tinggi, atau di lapangan tanpa khawatir akan menipisnya persediaan.
Penggunaan nitrocefin dalam pengujian dapat menghasilkan latar belakang yang tinggi karena konsentrasi substrat yang ditambahkan yang tinggi, yang akan mengurangi sensitivitas pengujian. 28 Beralih ke substrat fluoresen, seperti CCF2-FA, yang dapat digunakan pada konsentrasi yang lebih rendah dapat lebih meningkatkan sensitivitas pengujian yang mengarah pada pengurangan lebih lanjut dalam jumlah RNA yang dibutuhkan. Keuntungan menggunakan DSD dibandingkan metode DoE alternatif adalah berkurangnya jumlah pengujian yang dibutuhkan untuk mencapai biosensor yang optimal. 18 Metode yang dapat diterapkan ini akan memungkinkan pengoptimalan yang mudah jika terjadi modifikasi lebih lanjut pada pengujian biosensor, misalnya jika substrat fluoresen alternatif digunakan. Lebih jauh, pendekatan kami dengan mempertimbangkan total absorbansi dan latar belakang menunjukkan kekuatan desain eksperimen, karena pendekatan satu faktor pada satu waktu mungkin tidak menghasilkan peningkatan keseluruhan dalam pengujian, khususnya ketika interaksi antara faktor diidentifikasi. Alur kerja yang kami usulkan yang menggabungkan DSD dan validasi eksperimental akan berlaku untuk desain biosensor lain dengan keluaran kuantitatif, yang menunjukkan fleksibilitas proses kami. Pada akhirnya, biosensor kami kini tidak hanya memiliki karakteristik yang lebih baik, tetapi juga mengurangi jumlah RNA yang diperlukan untuk digunakan.
4 DISKUSI
Desain eksperimen memungkinkan kami untuk mengevaluasi ruang desain yang besar untuk perbaikan uji biosensor guna menilai pembatasan dan integritas RNA. Salah satu aspek yang paling menarik adalah seberapa tangguh kondisi awal, dengan beberapa iterasi model DoE yang diperlukan sebelum kondisi tersebut mengalahkan kondisi awal dalam rasio signal-to-noise dan batas deteksi. Modifikasi penting adalah penurunan pada protein B4E dan konsentrasi pdT 25 , serta peningkatan jumlah DTT yang diperlukan, yang menunjukkan lingkungan reduksi sebagai kondisi terbaik untuk fungsionalitas penuh. Penurunan konsentrasi pdT 25 mungkin sebagian bertanggung jawab atas perilaku oversaturasi pada konsentrasi RNA tinggi dalam kondisi yang dioptimalkan. Selain itu, oligomerisasi diri B4E melalui pembentukan ikatan disulfida sebelumnya telah diamati selama pemurnian, 26 yang berpotensi dicegah melalui peningkatan konsentrasi DTT.
Peningkatan kondisi biosensor menghasilkan pengurangan jumlah RNA yang dibutuhkan untuk pengujian. Efek yang tidak terduga ini pada akhirnya akan bermanfaat terutama saat menangani RNA yang lebih panjang, seperti vaksin mRNA Covid19 yang panjangnya 4284 nukleotida. 27 Perbedaan ini memiliki dampak yang substansial, pengurangan sepertiga penggunaan RNA, terlepas dari panjangnya, akan mengurangi jumlah material yang dibutuhkan untuk pengujian, yang berpotensi meningkatkan kelayakan penggunaan pengujian ini untuk pengoptimalan proses manufaktur, penyaringan dengan hasil tinggi, atau di lapangan tanpa khawatir akan menipisnya persediaan.
Penggunaan nitrocefin dalam pengujian dapat menghasilkan latar belakang yang tinggi karena konsentrasi substrat yang ditambahkan yang tinggi, yang akan mengurangi sensitivitas pengujian. 28 Beralih ke substrat fluoresen, seperti CCF2-FA, yang dapat digunakan pada konsentrasi yang lebih rendah dapat lebih meningkatkan sensitivitas pengujian yang mengarah pada pengurangan lebih lanjut dalam jumlah RNA yang dibutuhkan. Keuntungan menggunakan DSD dibandingkan metode DoE alternatif adalah berkurangnya jumlah pengujian yang dibutuhkan untuk mencapai biosensor yang optimal. 18 Metode yang dapat diterapkan ini akan memungkinkan pengoptimalan yang mudah jika terjadi modifikasi lebih lanjut pada pengujian biosensor, misalnya jika substrat fluoresen alternatif digunakan. Lebih jauh, pendekatan kami dengan mempertimbangkan total absorbansi dan latar belakang menunjukkan kekuatan desain eksperimen, karena pendekatan satu faktor pada satu waktu mungkin tidak menghasilkan peningkatan keseluruhan dalam pengujian, khususnya ketika interaksi antara faktor diidentifikasi. Alur kerja yang kami usulkan yang menggabungkan DSD dan validasi eksperimental akan berlaku untuk desain biosensor lain dengan keluaran kuantitatif, yang menunjukkan fleksibilitas proses kami. Pada akhirnya, biosensor kami kini tidak hanya memiliki karakteristik yang lebih baik, tetapi juga mengurangi jumlah RNA yang diperlukan untuk digunakan.
KONTRIBUSI PENULIS
Rochelle Aw: Konseptualisasi; investigasi; penulisan – draf asli; analisis formal; metodologi; validasi. Karen Polizzi: Konseptualisasi; perolehan dana; penulisan – tinjauan dan penyuntingan; administrasi proyek; supervisi.
UCAPAN TERIMA KASIH
Penulis ingin mengucapkan terima kasih kepada UKRI Agile Covid response (BB/W010771/1) atas pendanaannya. Penulis juga ingin mengucapkan terima kasih kepada Ignacio Moya-Ramirez atas bantuannya dalam mengatasi masalah.
PERNYATAAN KONFLIK KEPENTINGAN
Penulis tidak memiliki konflik kepentingan untuk dideklarasikan.
