ABSTRAK
Latar belakang
Kanker kolorektal (CRC) menempati peringkat ketiga sebagai kanker dengan prevalensi tertinggi di seluruh dunia. Penelitian terkini menunjukkan potensi menjanjikan dari mikroRNA (miRNA) dalam memprediksi status sel tumor yang bersirkulasi (CTC), dan analisis gabungannya dapat membuka jalan bagi kemajuan signifikan dalam menilai risiko kanker metastasis. Di sini, kami menyelidiki tanda-tanda miRNA yang bersirkulasi yang terkait dengan status CTC pada CRC metastasis (mCRC).
Metode
Status CTC pasien mCRC dinilai menggunakan teknologi AdnaTest ColonCancer, yang mendeteksi sel tumor menggunakan pendekatan imunomagnetik dan mengkarakterisasikannya berdasarkan penanda permukaan spesifik kolon. Profil miRNA dianalisis menggunakan mikroarray miRNA Agilent pada 8 individu positif CTC, 8 individu negatif CTC, dan delapan individu sehat. Implikasi fungsional miRNA yang terganggu dan interaksinya dengan mRNA target, TF, dan lncRNA ditentukan melalui analisis in silico yang komprehensif . Kandidat miRNA yang diekspresikan secara berbeda dalam kelompok positif CTC dan negatif CTC, yang memiliki bukti sebelumnya untuk perannya dalam biologi CRC, divalidasi menggunakan qPCR.
Hasil
Kami mengidentifikasi dua kelompok miRNA yang tidak teratur terkait dengan status CTC dan beberapa biomarker kandidat dalam jaringan regulasi miRNA yang disarankan. Tiga miRNA (hsa-miR-199a-5p, hsa-miR-326, hsa-miR-500b-5p), yang mengalami penurunan regulasi pada kelompok CTC-positif dibandingkan dengan kelompok CTC-negatif, dikonfirmasi oleh qPCR dan diprioritaskan sebagai prediktor kandidat status CTC dalam mCRC.
Kesimpulan
Temuan kami menunjukkan kandidat biomarker yang dapat digunakan untuk memprediksi status CTC pada individu dengan mCRC. Hal ini juga dapat memberikan wawasan baru tentang aplikasi pengobatan translasi baru dalam pengelolaan mCRC melalui deteksi CTC terkait CRC berbasis miRNA.
1 Pendahuluan
Kanker kolorektal (CRC) merupakan salah satu kanker dengan prevalensi tertinggi dan penyebab kematian akibat kanker ketiga di seluruh dunia [ 1 ]. Hampir 25% pasien menunjukkan metastasis pada diagnosis awal, dan sekitar 50% pasien CRC pada akhirnya akan mengalami metastasis [ 2 ]. Namun, fitur klinikopatologis dan mekanisme regulasi epigenetik CRC metastasis (mCRC) masih belum sepenuhnya dipahami [ 3 ]. Penelitian terbaru tentang perubahan genetik, transkripsi, dan epigenetik bertujuan untuk mengidentifikasi aplikasi klinis masa depan sebagai biomarker atau target terapi potensial pada CRC [ 4 , 5 ].
Analisis sirkuloma tumor dalam biopsi cair dapat menangkap heterogenitas klonal tumor [ 6 ]. Sel tumor yang bersirkulasi (CTC), komponen utama analit biopsi cair, dilepaskan dari tumor primer ke dalam sirkulasi dan terlibat dalam pengembangan metastasis tumor saat terlokalisasi di jaringan yang jauh [ 6 – 8 ]. Metode isolasi dan pengayaan CTC bergantung pada sifat fisiknya (strategi berbasis ukuran, kepadatan, dan muatan listrik) dan karakteristik biologis (ekspresi penanda protein permukaan dan viabilitas) sel tumor [ 9 ]. Namun, kemunculan CTC yang langka menyebabkan tantangan dalam deteksi dan karakterisasi namun mengarah pada temuan negatif palsu [ 10 , 11 ].
MikroRNA (miRNA) adalah reservoir lain dari biomarker kanker dalam biopsi cair dan memberikan informasi berharga tentang heterogenitas tumor [ 6 , 7 , 12 ]. miRNA adalah RNA non-coding yang terdiri dari 18-24 nukleotida yang bertanggung jawab untuk regulasi pasca-transkripsi ekspresi gen, jalur metabolisme seluler, dan proses perkembangan. Teknologi throughput tinggi adalah pendekatan yang kuat untuk profil miRNome yang memungkinkan karakterisasi miRNA spesifik kanker dan menawarkan perspektif baru tentang peran fungsional miRNA dalam kanker [ 13 – 15 ]. Temuan analisis miRNome kanker mengklasifikasikan miRNA sebagai onkogenik atau tumor-supresif; dengan demikian, mengungkap mekanisme miRNA dalam tumorigenesis memiliki potensi besar dalam manajemen CRC [ 14 ]. Khususnya, miRNA terkait metastasis, yang dikenal sebagai “metastamiRs” mengatur proses dan jalur molekuler dalam perkembangan ganas, meskipun belum ada yang diterapkan dalam praktik klinis [ 16 ].
Meskipun literatur melaporkan beberapa miRNA sebagai kandidat biomarker untuk manajemen CRC, pengetahuan saat ini menunjukkan bahwa analisis gabungan biomarker berbasis biopsi cair dapat menghasilkan hasil yang lebih kuat dengan nilai praktis dan klinis [ 5 , 17 , 18 ]. Oleh karena itu, status CTC dan profil ekspresi miRNA yang dideteksi oleh analisis biopsi cair memiliki potensi besar untuk mengevaluasi risiko perkembangan metastasis CRC [ 19 , 20 ]. Selain itu, miRNA yang bersirkulasi memiliki janji yang luar biasa sebagai biomarker untuk klasifikasi pasien berdasarkan status CTC, dan analisis multi-analit CTC dan miRNA dapat menawarkan alat pengobatan translasi baru untuk praktik klinis dalam mCRC. Studi ini bertujuan untuk menyelidiki tanda tangan miRNA yang terkait dengan status CTC yang dapat meningkatkan aplikasi klinis CTC dalam manajemen mCRC.
2 Bahan dan Metode
2.1 Sampel
Penelitian ini dilakukan di Departemen Onkologi Medis, Departemen Bedah Umum, dan Departemen Biologi Molekuler dan Genetika, Universitas Bursa Uludag, Turki. Setelah Deklarasi Helsinki, persetujuan tertulis diperoleh dari semua peserta saat pendaftaran, dan spesimen dikumpulkan menggunakan protokol yang disetujui oleh Komite Etik Dewan Peninjauan Kelembagaan Universitas Bursa Uludag (2011-KAEK-26/117). Sampel darah dari 48 pasien mCRC dan 50 individu sehat (HI) berusia ≥ 18 tahun dipelajari antara Agustus 2022 dan Mei 2023. HI tidak memiliki riwayat kanker, kecurigaan, atau keluhan, atau penyakit kronis apa pun. Sampel darah vena perifer sebanyak 10 mL dikumpulkan dari pasien mCRC setidaknya 7 hari setelah penerapan intervensi terapeutik terakhir dalam BD Vacutainer ACD-A (Becton-Dickinson, Franklin Lakes, NJ, AS) dan diproses dalam waktu 4 jam setelah darah diambil untuk protokol AdnaTest (QIAGEN GmbH, Hilden, Jerman). Selain itu, sampel darah vena perifer sebanyak 7–8 mL dikumpulkan dari semua peserta dalam tabung EDTA untuk isolasi RNA total. Semua sampel disimpan pada suhu −20°C hingga ekstraksi RNA.
2.2 Pengayaan dan Deteksi Sel Tumor yang Beredar
2.2.1 Pengayaan CTC dengan Metode Seleksi Sel Imunomagnetik
AdnaTest EMT-2/StemCell Detect (QIAGEN GmbH, Hilden, Jerman) dan AdnaTest ColonCancerDetect (QIAGEN GmbH, Hilden, Jerman) digunakan untuk pengayaan CTC menurut petunjuk pabrik pembuatnya. Secara singkat, 5 mL darah dipindahkan ke AdnaTube (QIAGEN GmbH, Hilden, Jerman) dan diinkubasi dengan antigen terkait tumor yang dikonjugasikan dengan manik magnetik berlapis oligo-(dT)25 untuk memperkaya CTC. Campuran antibodi terhadap epitop Epithelial Cell Adhesion Molecule ( EpCAM ), Human Epidermal Growth Factor Receptor 2 ( Her2 ), dan Epidermal Growth Factor Receptor ( EGFR ) digunakan untuk pengayaan dalam inkubator berputar selama 30 menit pada suhu RT, dan lisat sel dipisahkan dengan AdnaMag-L (QIAGEN GmbH, Hilden, Jerman). Untuk mencegah kontaminasi leukosit, semua sampel darah diproses dan dicuci dengan AdnaWash Leukocyte Reducer (QIAGEN GmbH, Hilden, Jerman) 3 kali dan dipindahkan ke tabung pengumpulan baru setelah setiap pencucian.
2.2.2 PCR Multipleks dan Penentuan Status CTC
mRNA diisolasi dari lisat dan eluat CTC dengan manik magnetik berlapis oligo(dT)25 dengan AdnaMag-S (QIAGEN GmbH, Hilden, Jerman). Lisat yang dieluasi ditranskripsi balik menggunakan kit AdnaTest EMT-2/StemCell Detect (QIAGEN GmbH, Hilden, Jerman) dan Kit Sensiscript RT (QIAGEN GmbH, Hilden, Jerman). cDNA yang dihasilkan diproses dalam PCR multipleks untuk transkrip terkait tumor dalam AdnaTest ColonDetect Primer Mix (QIAGEN GmbH, Hilden, Jerman), termasuk Carcinoembryonic Antigen ( CEA ), EGFR , dan EpCAM , serta ß-Actin sebagai kontrol positif. PCR multipleks dilakukan menggunakan HotStarTaq Master Mix (QIAGEN GmbH, Hilden, Jerman). Fragmen divisualisasikan dan ditentukan dengan elektroforesis gel agarosa 3% sesuai dengan rekomendasi produsen.
2.3 Analisis Mikroarray MiRNA
2.3.1 Isolasi RNA Total
Total RNA diisolasi dari darah utuh menggunakan kit miRNeasy Serum/Plasma Advanced (QIAGEN GmbH, Hilden, Jerman) mengikuti protokol pabrik pembuatnya. Volume awal darah tepi adalah 600 μL, dan cel-miR-39-3p sintetis (0,16 fmol) (QIAGEN GmbH, Hilden, Jerman) ditambahkan ke dalam lisat. Total RNA dielusi dalam 30 μL air bebas RNase. Kuantitas dan kualitas RNA dievaluasi menggunakan Qubit 4 Fluorometer (Thermo Scientific, Waltham, MA, AS) dengan RNA High Sensitivity Assay (Invitrogen, Carlsbad, CA, AS). RNA Integrity Number (RIN) dinilai menggunakan Agilent 2100 Bioanalyzer (Agilent, Santa Clara, CA, AS) dan kit RNA 6000 Nano (Agilent Technologies, Santa Clara, CA).
2.3.2 Profil miRNA dengan Sistem Mikroarray Agilent
Profil ekspresi miRNA dari 24 sampel [CTC positif ( n = 8), CTC negatif ( n = 8) dan HIs ( n = 8)] dianalisis menggunakan Agilent Microarrays (SurePrint G3 Human miRNA r21 8x60K; Cat no. #G4872A Agilent Technologies Inc.) dan kit Pelabelan dan Hibridisasi miRNA (Agilent Technologies Inc.) sesuai dengan petunjuk pabrik pembuatnya. Karakteristik demografi dan klinis dari sampel yang dipilih untuk analisis microarray diberikan dalam Tabel S1 . Volume awal total RNA adalah 100 ng yang diekstraksi dari darah tepi dan diberi label dengan sianin 3-pCp. Setelah itu, termasuk 2570 probe manusia, slide hibrida dipindai menggunakan Agilent SureScan Microarray Scanner (Model G2600D; Agilent Technologies Inc.) dan gambar dianalisis oleh perangkat lunak Agilent Feature Extraction (v.12.2.0.7) (Agilent Technologies Inc.). Data ekspresi yang diperoleh diproses menggunakan perangkat lunak GeneSpring GX (v.14.9) (Agilent Technologies Inc.). Data disimpan ke dalam basis data NCBI Gene Expression Omnibus (Nomor Akses GSE285322).
2.3.3 Analisis Data
Tingkat ekspresi miRNA dievaluasi dalam lima kelompok berbeda: Kelompok 1, CTC(+) versus CTC(−); Kelompok 2, CTC(+) versus HI; Kelompok 3, CTC(−) versus HI; Kelompok 4, mCRC [CTC(+)&CTC(−)] versus HI; dan Kelompok 5, CTC(+) versus CTC(−) versus HI. Kelompok 1–4 digunakan untuk melakukan perbandingan dua kelompok DEM guna mengidentifikasi pola ekspresi miRNA unik yang mungkin spesifik terhadap ada atau tidaknya CTC. Pola-pola ini dinilai, dan kandidat miRNA ditentukan dengan mengevaluasi irisan dan pelengkap kelompok menggunakan diagram Venn. Uji- t tidak berpasangan sedang digunakan untuk mendeteksi DEM dengan perubahan lipatan (FC) ≥ 2 atau ≤ −2 dan kriteria p < 0,05. Uji Analisis Variasi (ANOVA) digunakan untuk analisis tiga kelompok yang dilakukan untuk Kelompok 5. Signifikansi statistik ditetapkan sebagai p < 0,05. Diagram Venn diperoleh dari VENNY (v.2.1) ( https://bioinfogp.cnb.csic.es/tools/venny/ ).
2.4 Analisis Bioinformatika
Beberapa alat bioinformatika daring dan perangkat lunak berlisensi digunakan untuk analisis fungsional in silico dari DEM yang tidak teratur (Gambar S1 ). Selain itu, miRNA dan gen targetnya di seluruh kelompok DEM dibandingkan dengan data The Cancer Genome Atlas (TCGA) dan Genotype-Tissue Expression (GTEx). Basis data MicroRNA Data Integration Portal (mirDIP) ( http://ophid.utoronto.ca/mirDIP ) digunakan untuk memprediksi target umum dari DEM yang diprioritaskan dalam kelompok DEM-1 dan DEM-2. Analisis ekspresi, plot stadium patologis, dan analisis kelangsungan hidup keseluruhan (OS) dilakukan pada kumpulan data TCGA dan GTEx dari gen yang umumnya ditargetkan milik kelompok DEM dalam basis data Gene Expression Profiling Interactive Analysis (GEPIA) ( http://gepia.cancer-pku.cn ). Hubungan regulasi antara DEM dan faktor transkripsi (TF) ditentukan dengan basis data TransmiR (v.2.0) ( https://www.cuilab.cn/transmir ). Lebih jauh lagi, lncRNA terkait DEM ditentukan dengan basis data RNA Interactome Database (RNAInter) (v.4.0) ( http://www.rnainter.org ). Peran DEM dalam jalur molekuler diselidiki oleh basis data miRNet (v.2.0) ( https://www.mirnet.ca ). Basis data DIANA-miRPath (v.3.0) ( http://www.microrna.gr/miRPathv3 ) digunakan dalam analisis pengayaan jalur KEGG dengan uji hipergeometrik. Selain itu, analisis pengayaan fungsional miRNA dilakukan dalam perangkat lunak Ingenuity Pathway Analysis (IPA) (QIAGEN GmbH, Hilden, Jerman) menggunakan fitur “Disease & Functions”, dengan hasil yang difilter menurut kategori penyakit dan anotasi fungsional. miRNA yang termasuk dalam kelompok DEM dibandingkan dengan data sekuensing RNA dalam dataset Adenokarsinoma Kolon (COAD) (jaringan pasien n = 444, jaringan normal n = 8) dan Adenokarsinoma Rektum (READ) (jaringan pasien n = 161, jaringan normal n = 3) dari database TCGA dengan menggunakan database CancerMIRNome ( http://bioinfo.jialab-ucr.org/CancerMIRNome ).
2.5 Validasi PCR Kuantitatif miRNA Terkait CRC
Kami melakukan PCR kuantitatif (qPCR) pada tiga miRNA yang mengalami disregulasi (hsa-miR-199a-5p, hsa-miR-326, dan hsa-miR-500b-5p) yang dipilih dari kelompok DEM-1, yang menunjukkan pola ekspresi yang berubah pada kelompok CTC(+) dibandingkan dengan kelompok CTC(−) dan ditemukan berhubungan dengan CRC pada IPA (Tabel S10 ). MiRNA ini juga mengalami disregulasi yang signifikan pada dataset TCGA COAD dan READ. Kohort validasi mencakup semua pasien mCRC yang dikelompokkan berdasarkan status CTC [CTC(+) = 32 dan CTC(−) = 18] bersama dengan 42 sampel sehat tambahan. Informasi klinis untuk seluruh sampel disediakan pada Tabel S2 . Sintesis cDNA dilakukan menggunakan miRCURY LNA miRNA RT Kit (QIAGEN GmbH, Hilden, Jerman) pada Siklus Termal SimpliAmp (Applied Biosystems, Foster City, CA), mengikuti protokol pabrik pembuatnya. qPCR dilakukan dalam rangkap tiga menggunakan kit PCR miRCURY LNA miRNA SYBR Green menggunakan Rotor-Gene Q (QIAGEN GmbH, Hilden, Jerman), mengikuti protokol pabrik pembuatnya. Tingkat ekspresi miRNA ditentukan menggunakan Perangkat Lunak Q-Rex, dengan snRNA U6 (QIAGEN GmbH, Hilden, Jerman) sebagai kontrol endogen. Tingkat ekspresi relatif miRNA dihitung menggunakan metode 2 −ΔΔCT . Analisis Karakteristik Operasi Penerima (ROC) dilakukan menggunakan GraphPad Prism (v.10.1.2, Perangkat Lunak GraphPad, San Diego, CA, AS) untuk mengevaluasi potensi diagnostik miRNA yang dipilih, dengan mempertimbangkan nilai area di bawah kurva (AUC) yang lebih besar dari 0,7 sebagai signifikan.
3 Hasil
3.1 Deteksi dan Karakterisasi CTC
Status CTC pasien mCRC dideteksi dengan kit AdnaTest EMT-2/StemCell Select dan AdnaTest CTC Detect dan ditentukan dengan mengamati pita dari 3 gen ( CEA , EGFR dan EpCAM ). Pita ß-Actin diamati pada semua sampel. Tidak ada pita yang diamati pada kontrol negatif. Empat pita gen ( CEA , EGFR , EpCAM dan ß-Actin ) diamati pada kontrol positif. Selain itu, kontrol RT juga dilakukan untuk mengendalikan langkah-langkah sebelum tahap PCR Multiplex, dan tidak ada pita yang diamati. Jika sebuah fragmen yang termasuk setidaknya satu dari gen CEA , EGFR , dan EpCAM terdeteksi dalam elektroforesis gel, sampel dievaluasi sebagai CTC(+), dan sampel yang tidak terdeteksi fragmennya dianggap sebagai CTC(−). Hasil elektroforesis gel menunjukkan bahwa 30 sampel dievaluasi sebagai CTC(+), dan dengan hasil ini, tingkat positif CTC kami adalah 62%. Jumlah sampel dalam kelompok CTC(+) yang hanya ditemukan pita milik penanda EGFR adalah 7, sedangkan jumlah sampel yang hanya ditemukan pita terkait penanda CEA adalah satu. Dua puluh dua sampel menunjukkan positif untuk penanda CEA dan EGFR secara keseluruhan. Tidak ada sampel yang menunjukkan bahwa penanda EpCAM positif. Karakteristik klinis pasien yang dikelompokkan menurut status CTC dan distribusi biomarker diberikan dalam Tabel 1 .
TABEL 1. Distribusi penanda terkait mCRC dengan karakteristik klinis pasien.
EGFR(+) ( n =7) CEA(+) ( n = 1) EGFR dan CEA (+) ( n = 22) CTC(−) ( n =18)
Tipe histologis
Adenokarsinoma usus besar, n (%) 34 (70.8) 4 (57) 1 (100) 15 (68.2) 13 (72.2)
Adenokarsinoma rektum, n (%) 10 (20.8) 2 (28.5) — 7 (31.8) 2 (11.1)
Lainnya, n (%) 4 (8.4) 1 bahasa inggris (14.5) — — 3 (16.6)
Metastasis
Hati, n (%) 39 (81.25) 7 (100) — 17 (77.4) 11 (61.2)
Hati + Paru-paru, n (%) 3 (6.25) — 1 (100) 2 (9.1) 1 (5.5)
Paru-paru, n (%) 2 (4.2) — — 1 (4.4) 1 (5.5)
Lainnya, n (%) 4 (8.3) — — 2 (9.1) 5 (27.8)
Lokasi
Kolon sigmoid, n (%) 20 (41.7) 2 (28.5) 1 (100) 11 (50) 6 (33.3)
Kolon rektosigmoid, n (%) 12 (25) 2 (28.5) — 6 (27.2) 4 (22.2)
Rektum, n (%) 8 (16.7) 2 (28.5) — 4 (18.2) 2 (11.1)
Titik dua kanan, n (%) 4 (8.3) — — — 4 (22.2)
Lainnya, n (%) 4 (8.3) 1 bahasa inggris (14.5) — 1 (4.4) 2 (11.1)
Kelangsungan hidup
Hidup, n (%) 32 (66.7) 5 (71.5) — 16 (72.8) 11 (61.1)
Mati, n (%) 16 (33.3) 2 (28.5) 1 (100) 6 (27.2) 7 (38.9)
Jalur terapi
0, tidak ada (%) 3 (6.25) — — 3 (13.5) —
1–5, tidak ada (%) 23 (47.95) 2 (28.5) — 11 (50) 10 (55.5)
6–10, tidak ada (%) 10 (20.8) 3 (42.5) — 4 (18.2) 3 (16.6)
11–20, tidak ada (%) 3 (6.25) 1 bahasa inggris (14.5) — — 2 (11.1)
21–30, tidak ada (%) 1 (2.1) — — — 1 (5.5)
31–40, tidak ada (%) 3 (6.25) 1 bahasa inggris (14.5) — 2 (9.1) —
41–50, tidak ada (%) 5 (10.4) — 1 (100) 2 (9.1) 2 (11.1)
3.2 Hasil Mikroarray miRNA
Distribusi gender dari delapan sampel yang dipilih untuk mikroarray dari kelompok HIs adalah sama; usia rata-rata adalah 43,25, Indeks Massa Tubuh (IMT) rata-rata adalah 26,1 kg/m 2 , dan tingkat penggunaan rokok dan alkohol masing-masing adalah 37,25% dan 25%. Informasi klinis sampel yang dipilih dari kelompok CTC(+) dan CTC(−) dalam analisis mikroarray miRNA dirangkum dalam Tabel S1 .
3.3 Analisis Data
Sebanyak 2570 miRNA disediakan melalui kontrol kualitas sebelum analisis statistik dalam perangkat lunak GeneSpring GX (v.14.9). Jumlah DEM yang signifikan secara statistik ( p < 0,05) ditentukan menurut nilai- p yang berbeda dalam setiap perbandingan kelompok dalam analisis statistik dan disajikan dalam Tabel S3 . DEM yang tumpang tindih dan berbeda dalam perbandingan kelompok ditunjukkan pada Gambar 1. Grafik plot gunung berapi DEM yang ditentukan dalam analisis ganda data mikroarray yang diperoleh dari empat kelompok ditunjukkan pada Gambar S2 . 10 DEM paling signifikan yang terdeteksi dalam empat kelompok dalam analisis data mikroarray ditunjukkan pada Tabel S4 . DEM dengan nilai- p paling signifikan secara statistik di setiap kelompok ditunjukkan dengan huruf tebal. DEM yang tumpang tindih paling signifikan dalam kelompok mCRC/HIs dan CTC(+)/HIs adalah hsa-miR-141-3p. DEM yang paling tumpang tindih dalam tiga kelompok adalah hsa-miR-15b-3p, hsa-miR-141-3p, dan hsa-miR-190a-5p. 10 DEM teratas yang tumpang tindih dan unik yang ditentukan dalam analisis kelompok ditunjukkan pada Gambar S3 . Kelompok CTC(+)/CTC(−) menunjukkan jumlah tumpang tindih DEM paling sedikit, sedangkan kelompok mCRC/HIs dan CTC(+)/HIs menunjukkan jumlah tumpang tindih DEM tertinggi ( n = 7) satu sama lain.
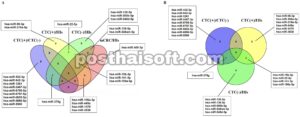
Diagram Venn DEM (FC ≥ 2 atau ≤ −2 dan p < 0,05) diidentifikasi dalam analisis mikroarray. (A) DEM umum dan tumpang tindih untuk perbandingan kelompok CTC(+)/CTC(−), CTC(+)/HIs, CTC(−)/HIs, dan mCRC/HIs. (B) DEM umum dan tumpang tindih untuk perbandingan kelompok CTC(+)/CTC(−), CTC(+)/HIs, dan CTC(−)/HIs.
3.4 Analisis Pengayaan Jalur KEGG dan GO
Analisis pengayaan KEGG dan GO dilakukan dalam basis data miRNet dengan gen target semua DEM ditemukan signifikan dalam perbandingan kelompok. Dalam analisis KEGG dan GO, DEM yang berpotongan dalam kelompok CTC(+) dan CTC(−) ( n = 37), DEM yang berpotongan dalam kelompok CTC(+) dan HIs ( n = 41), DEM yang berpotongan dalam kelompok CTC(−) dan HIs ( n = 328), dan DEM yang berpotongan dalam kelompok mCRC dan HIs ( n = 262) disertakan. 10 jalur KEGG yang paling signifikan secara statistik disajikan dalam Tabel S5 , dan 10 istilah GO:BP, GO:MF, dan GO:CC teratas ditunjukkan dalam Tabel S6 .
3.5 Analisis Bioinformatika
Analisis bioinformatika lebih lanjut dilakukan pada kelompok DEM setelah menilai irisan dan bagian uniknya, seperti yang ditunjukkan dalam diagram Venn (Gambar 1A ). Dua kelompok DEM, yang ditetapkan sebagai DEM-1 dan DEM-2, diprioritaskan dalam analisis ini sebagai kandidat miRNA yang terkait dengan status CTC dan disertakan dalam analisis in silico berikutnya . DEM-1 terdiri dari lima DEM (hsa-miR-199a-5p, hsa-miR-326, hsa-miR-378 g, hsa-miR-500b-5p dan hsa-miR-4737). MiRNA ini diidentifikasi di irisan DEM dari tiga kelompok [CTC(+)/CTC(−), CTC(−)/HIs dan mCRC/HIs] dan diprioritaskan karena mereka mengalami penurunan regulasi baik dalam sampel CTC(−) dan total mCRC dibandingkan dengan HIs. Namun, mereka mengalami peningkatan regulasi dalam sampel CTC(+) dibandingkan dengan CTC(−), sehingga mereka dipilih untuk analisis lebih lanjut dengan qPCR dalam sampel yang lebih besar. Kelompok DEM kedua (DEM-2) terdiri dari enam DEM (hsa-miR-181c-5p, hsa-miR-497-5p, hsa-miR-520e, hsa-miR-769-5p, hsa-miR-4754 dan hsa-miR-5691) dan juga diprioritaskan berdasarkan penurunan regulasi mereka dalam sampel CTC(+) dan mCRC dibandingkan dengan HI. Khususnya, mereka tidak signifikan dalam sampel CTC(−) dibandingkan dengan HI (Gambar 1A dan Tabel 2 ).
TABEL 2. DEM kandidat dikaitkan dengan status CTC melalui microarray ( p < 0,05).
Perbandingan CTC(+) dan CTC(−) CTC(−) versus HI mCRC versus HI
DEM 1 ID miRBase P Klub Sepak Bola catatanFC P Klub Sepak Bola catatanFC P Klub Sepak Bola catatanFC
hsa-miR-199a-5p MIMAT0000231 1.84E-02 7.362 2.880 4.25E-03 -15.106 -3.917 2.92E-02 -5.567 -2.477
hsa-miR-326 MIMAT0000756 3.06E-02 5.693 2.509 8.08E-03 -11.763 -3.556 3.30E-02 -4.930 -2.302
hsa-miR-378g MIMAT0018937 2.69E-03 8.663 3.115 2.69E-03 -16.454 -4.040 2.23E-02 -5.590 -2.483
hsa-miR-500b-5p MIMAT0016925 1.39E-02 6.344 2.665 1.03E-04 -30.922 -4.951 1.10E-03 -12.276 -3.618
hsa-miR-4737 MIMAT0019863 3.56E-02 7.164 2.841 5.08E-03 -14.278 -3.836 4.93E-02 -5.334 -2.415
CTC(+) versus HI mCRC versus HI
DEM 2 ID miRBase P Klub Sepak Bola LogFC P Klub Sepak Bola LogFC
hsa-miR-181c-5p MIMAT0000258 2.78E-02 -10.979 -3.457 1.74E-02 -8.354 -3.063
hsa-miR-497-5p MIMAT0002820 4.28E-02 -8.502 -3.088 1.08E-02 -7.485 -2.904
hsa-miR-520e MIMAT0002825 2.26E-02 -8.684 -3.118 1.06E-02 -6.990 -2.805
hsa-miR-769-5p MIMAT0003886 3.36E-02 -8.389 -3.069 1.75E-02 -7.264 -2.861
hsa-miR-4754 MIMAT0019894 4.94E-02 -6.831 -2.772 1.42E-02 -6.014 tahun lalu -2.588
hsa-miR-5691 MIMAT0022483 4.54E-02 -7.193 -2.847 1.24E-02 -6.332 -2,663
3.5.1 Penentuan Gen Target
Basis data mirDIP digunakan untuk menentukan gen target miRNA dalam kelompok DEM. Daftar gen yang ditargetkan oleh sedikitnya tiga miRNA dalam kelompok DEM yang relevan ditunjukkan pada Tabel S7 . Sementara dua gen target umum terdeteksi dalam DEM-1, sembilan gen umum ditemukan dalam DEM-2. Profil ekspresi gen target kelompok DEM juga dianalisis dalam dataset COAD dan READ dari basis data TCGA dan GTEx. Glycerol-3-Phosphate Dehydrogenase 2 ( GPD2 ), AKT Serine/Threonine Kinase 3 ( AKT3 ), CREB3 Regulatory Factor ( CREBRF ) dan Polypyrimidine Tract Binding Protein 3 ( PTBP3 ) ditemukan signifikan secara statistik ( p < 0,05) di kedua dataset (Gambar 2 ). Selain itu, ekspresi diferensial gen AKT3 dan Pleiomorphic Adenoma Gene 1 ( PLAG1 ) hanya signifikan secara statistik dalam analisis stadium patologis ( p < 0,05) (Gambar S4 ). Terakhir, hanya PLAG1 yang signifikan secara statistik (log-rank p = 0,0052) dalam analisis OS dalam database TCGA dan GTEx (Gambar S4 ). PLAG1 adalah satu-satunya gen yang ditemukan signifikan secara statistik dalam analisis stadium patologis dan OS (Gambar S4 ).

Profil ekspresi gen target yang terkait dengan kelompok DEM dalam kumpulan data COAD dan READ. Warna merah dan abu-abu masing-masing mewakili sampel tumor dan sampel normal. Signifikansi statistik ditunjukkan dengan tanda bintang merah ( p < 0,05).
3.5.2 Interaksi Regulasi DEM dengan TF
Kami juga memeriksa interaksi miRNA-TF dalam database TransmiR, dan analisis pengayaan sembilan miRNA menunjukkan bahwa 13 TF mungkin memengaruhi miRNA (Tabel S8 ).
3.5.3 Penentuan Target lncRNA DEM
Tiga puluh lima lncRNA yang berbeda diidentifikasi dengan menetapkan bukti eksperimental yang kuat dan lemah dalam alat RNAInter (Tabel S9 ). lncRNA Small Nuclear RNA Host Gene 12 ( SNHG16 ) ditetapkan sebagai lncRNA yang paling banyak ditargetkan dalam kelompok DEM ( n = 4).
3.5.4 Analisis Pengayaan Jalur
Kami menganalisis pengayaan kelompok DEM dalam kategori jalur Kyoto Encyclopedia of Genes and Genomes (KEGG) menggunakan basis data DIANA-miRPath (v.3.0). Analisis DIANA-miRPath menunjukkan bahwa sebagian besar miRNA diidentifikasi memiliki peran dalam jalur terkait kanker. Kategori jalur KEGG yang signifikan dan miRNA berkorelasi disajikan dalam peta panas yang dihasilkan dalam DIANA-miRPath (Gambar S5 ). “Interaksi ECM-reseptor” (ID jalur KEGG: hsa04512), “proteoglikan dalam kanker” (ID jalur KEGG: hsa05205), dan “jalur pensinyalan Hippo” (ID jalur KEGG: hsa04390) ditemukan umum dalam 2 kelompok DEM.
3.5.5 Analisis Pengayaan Fungsional
Analisis pengayaan fungsional kelompok DEM dalam IPA mengungkapkan hubungan signifikan dengan beberapa penyakit. Sebanyak empat puluh empat kategori penyakit dikaitkan dengan setidaknya satu miRNA dalam kelompok DEM-1. Khususnya, CRC ditemukan menjadi anotasi fungsional umum teratas yang dikaitkan dengan tiga miRNA (hsa-miR-199a-5p, hsa-miR-326, dan hsa-miR-500b-5p) ( p = 1.22E-02) (Tabel S10 , Gambar 3A ). MiRNA ini selanjutnya dimasukkan dalam studi validasi. Lebih jauh, total 120 kategori penyakit dikaitkan dengan setidaknya satu miRNA dalam kelompok DEM-2, dan delapan anotasi fungsional dikaitkan dengan setidaknya tiga miRNA. miRNA Hsa-miR-181a-5p, hsa-miR-497-5p, dan hsa-miR-520e ditemukan berinteraksi dengan CRC, dengan tingkat signifikansi peringkat kedelapan ( p = 4.03E-02) (Tabel S10 , Gambar 3B ). Anotasi fungsional dari sedikitnya 3 miRNA dalam kelompok DEM ditunjukkan pada Tabel S10 .

Jaringan menampilkan kelompok DEM dan hubungannya dengan penyakit dan fungsi biologis paling signifikan ( p < 0,05). Plot dibuat oleh perangkat lunak IPA (QIAGEN GmbH, Hilden, Jerman) (A) Kelompok DEM-1 (B) Kelompok DEM-2.
3.5.6 Perbandingan DEM dengan Dataset TCGA
Profil ekspresi dari 2 kelompok DEM dianalisis dengan data RNA-seq TCGA (kumpulan data COAD dan READ) menggunakan basis data CancerMIRNome. Profil ekspresi miRNA hsa-miR-378 g dan hsa-miR-4737 dalam DEM-1 dan miRNA hsa-miR-520e, hsa-miR-4754, dan hsa-miR-5691 dalam DEM-2 tidak ditentukan dalam kumpulan data. Hsa-miR-199a-5p dan hsa-miR-500b-5p dalam kelompok DEM-1 dan hsa-miR-181c-5p dan hsa-miR-769-5p dalam kelompok DEM-2 ditemukan kompatibel dengan kumpulan data COAD dan READ ( p < 0,05). Namun, tidak ada DEM yang signifikan secara statistik dalam kumpulan data yang sama melalui analisis kelangsungan hidup Kaplan-Meier (KM) (Tabel 3 ).
TABEL 3. Profil ekspresi kelompok DEM dengan data RNA-seq dalam dataset COAD dan READ.
DEM miRNA Adenokarsinoma usus besar (COAD)
catatanFC P Kata sifat p AUC ROC hal
DEM-1 hsa-miR-199a-5p -0,812 1.23E-02 1.56E-02 0,79 9.56E-46
hsa-miR-326 2.690 2.21E-06 3.75E-06 0.9 1.72E-98
hsa-miR-500b-5p -1,333 3.67E-03 4.87E-03 0.71 4.16E-25
DEM-2 hsa-miR-181c-5p -0,025 9.40E-01 9.46E-01 0.52 4.12E-01
hsa-miR-497-5p 0.467 1.84E-01 2.03E-01 0.66 1.54E-14
hsa-miR-769-5p -1,062 1.60E-06 2.74E-06 0,93 1.52E-104
DEM miRNA Adenokarsinoma rektum (READ)
catatanFC P Kata sifat p AUC ROC hal
DEM-1 hsa-miR-199a-5p -0,641 2.68E-01 3.06E-01 0.72 1.10E-11
hsa-miR-326 3.605 1.09E-06 2.46E-06 1 1.60E-57
hsa-miR-500b-5p -3.051 1.34E-06 2.98E-06 0,95 4.82E-46
DEM-2 hsa-miR-181c-5p -0,594 2.35E-01 2.74E-01 0,74 1.95E-13
hsa-miR-497-5p 0.714 1.31E-01 1.59E-01 0,79 5.56E-19
hsa-miR-769-5p -1.436 2.08E-04 3.62E-04 0,98 5.89E-54
Catatan: Hasil dengan nilai p < 0,05 yang signifikan ditunjukkan dengan huruf tebal dalam tabel.
Singkatan: AUC, area di bawah kurva; ROC, karakteristik operasi penerima.
3.6 Validasi miRNA terpilih dengan qPCR
Profil ekspresi hsa-miR-199a-5p, hsa-miR-326, dan hsa-miR-500b-5p divalidasi oleh qPCR dalam total sampel 48 mCRC dan 50 HI (Tabel S2 ). Ketiga miRNA terpilih ini menunjukkan penurunan regulasi yang signifikan secara statistik ( p < 0,05) pada pasien CTC(+) jika dibandingkan dengan pasien CTC(−) dan HI (Gambar 4A ). Selain itu, akurasi diagnostik ketiga miRNA sebagai kandidat biomarker untuk membedakan mCRC CTC(+) dari mCRC CTC(−) dan HI dievaluasi dengan analisis kurva ROC, yang mengungkapkan nilai AUC di atas 0,7 (Gambar 4B ). Kami juga membandingkan pola ekspresi miRNA di seluruh dataset miRNA microarray, qPCR, dan TCGA COAD dan READ. Nilai logFC dan p untuk perbandingan ini disajikan pada Tabel 4 dan Gambar 5 .

Ekspresi qPCR yang dinormalisasi dari miRNA tertentu yang mengalami penurunan regulasi secara signifikan dan analisis kurva ROC-nya (A) hsa-miR-199a-5p (B) hsa-miR-326 (C) hsa-miR-500b-5p ( p < 0,05, AUC > 0,7
TABEL 4. Perbandingan hasil microarray dan qPCR untuk tiga miRNA terpilih dalam kelompok CTC(+)/CTC(−), CTC(−)/HIs, dan mCRC/HIs.
miRNA Susunan qPCR
P Klub Sepak Bola catatanFC P Klub Sepak Bola catatanFC
CTC(+)/CTC(−)
hsa-miR-199a-5p 1.84E-02 7.362 2.88 0,0048 pukul 0,0048 0.783 -0,36
hsa-miR-326 3.06E-02 5.693 2.51 0,0005 0.22 -2,18
hsa-miR-500b-5p 1.39E-02 6.344 2.67 0,0013 0.284 -1,82
CTC(−)/HI
hsa-miR-199a-5p 4.25E-03 -15.11 -3,92 0,0001 0.299 -1,74
hsa-miR-326 8.08E-03 -11,76 -3,56 0,001 0.354 -1,5
hsa-miR-500b-5p 1.03E-04 -30,92 -4,95 0,0044 tahun 0.212 2.24
mCRC/HI
hsa-miR-199a-5p 2.92E-02 -5.567 -2,48 < 0,0001 0.184 -2,45
hsa-miR-326 3.30E-02 -4,93 -2,3 < 0,0001 0.243 -2,04
hsa-miR-500b-5p 1.10E-03 -12,28 -3,62 < 0,0001 0.154 -2,7

Perbandingan nilai logFC untuk tiga miRNA terpilih di seluruh kumpulan data yang berbeda: Analisis mikroarray dan qPCR membandingkan kelompok HI dan mCRC, sementara kumpulan data TCGA-COAD dan TCGA-READ membandingkan kelompok HI dan CRC (termasuk mCRC).
4 Diskusi
Penelitian terbatas telah menyelidiki evaluasi keberadaan CTC menggunakan tanda tangan miRNA berbasis darah, dan baru-baru ini, hal ini telah menjadi topik penelitian yang menarik di kalangan peneliti kanker [ 19 , 21 , 22 ]. Penelitian ini bertujuan untuk menentukan tanda tangan miRNA yang beredar terkait dengan status CTC pada mCRC.
Dalam analisis data mikroarray, DEM-1 (hsa-miR-199a-5p, hsa-miR-326, hsa-miR-378 g, hsa-miR-500b-5p dan hsa-miR-4737) ditentukan dalam perbandingan CTC(+)/CTC(−), CTC(−)/HIs dan mCRC/HIs. DEM-2 terdeteksi dalam perbandingan CTC(+)/HIs dan mCRC/HIs (hsa-miR-181c-5p, hsa-miR-497-5p, hsa-miR-520e, hsa-miR-769-5p, hsa-miR-4754 dan hsa-miR-5691) terungkap. Semua DEM yang disebutkan di atas menunjukkan penurunan regulasi dibandingkan dengan HIs. Akan tetapi, DEM-1 ditemukan mengalami peningkatan regulasi pada individu CTC(+) dibandingkan dengan mereka yang CTC(−). Selain itu, tiga DEM (hsa-miR-199a-5p, hsa-miR-326, dan hsa-miR-500b-5p) dari kelompok DEM-1, yang juga ditemukan signifikan dalam dataset TCGA dan dikaitkan dengan CRC dalam IPA, dianalisis oleh qPCR. Hasilnya konsisten dengan data mikroarray untuk perbandingan CTC(−)/HIs dan mCRC/HIs. Mengingat peran penilaian CTC yang menjanjikan dalam utilitas klinis, hasil ini signifikan dan dapat dikaitkan dengan ukuran sampel yang lebih besar dari kelompok validasi.
Ekspresi hsa-miR-199a-5p, diklasifikasikan dalam kelompok DEM-1 dan diverifikasi melalui qPCR, menunjukkan fungsi penekan tumor karena penurunan regulasinya dalam berbagai jenis kanker [ 23 – 25 ]. Selain itu, Hu et al. menemukan bahwa ekspresi hsa-miR-199a-5p menurun dalam jaringan dan lini sel CRC [ 26 ]. Terakhir, hsa-miR-199a-5p telah diindikasikan sebagai biomarker yang menjanjikan untuk neoplasia CRC [ 17 , 27 ]. Hasil qPCR dari hsa-miR-326 juga memvalidasi microarray. Ekspresi rendah hsa-miR-326 telah dilaporkan secara signifikan terkait dengan perkembangan yang buruk, perkembangan tumor, dan risiko metastasis dalam berbagai jenis kanker [ 28 ]. Selain itu, literatur melaporkan bahwa hsa-miR-326 dapat bertindak sebagai penekan tumor dan dikaitkan dengan prognosis tumor pada berbagai jenis kanker [ 28-30 ] . Selain itu, Bao et al. mengungkap bahwa hsa-miR-326 dapat menghambat proliferasi sel CRC dan menginduksi apoptosis dengan secara langsung menghambat Faktor Transkripsi E2F 1 ( E2F1 ) [ 31 ]. Khususnya, kami mengamati ketidakkonsistenan antara data kami dan dataset TCGA untuk profil ekspresi hsa-miR-326, yang dapat dikaitkan dengan fakta bahwa data TCGA sebagian besar mencakup individu dengan tumor primer (Tabel 3 ). MiRNA tervalidasi lainnya, hsa-miR-500b-5p, belum terdokumentasi dengan baik dibandingkan dengan miRNA lainnya. Rong et al. mengindikasikan bahwa hsa-miR-500b-5p menghambat perkembangan karsinoma sel skuamosa oral [ 32 ]. Dengan demikian, hasil kami menjanjikan dan memerlukan penelitian lebih lanjut untuk memahami peran hsa-miR-500b-5p dalam etiologi CRC. Selain itu, hsa-miR-378 g dan hsa-miR-4737, yang diidentifikasi dalam kelompok DEM-1, tidak mengalami disregulasi signifikan dalam data TCGA-COAD dan READ dan tidak diprioritaskan dalam studi validasi primer kami. Hsa-miR-378 g, yang termasuk dalam famili miR-378, disarankan untuk bertindak sebagai penekan tumor dengan memengaruhi banyak jalur seluler, seperti proliferasi sel, diferensiasi, dan apoptosis [ 33 – 35 ]. Telah dilaporkan bahwa hsa-miR-378 g dapat menjadi biomarker non-invasif untuk mendiagnosis dan mengobati pasien CRC [ 36 ]. Gungormez dkk. menemukan penurunan regulasi hsa-miR-378 g untuk pertama kalinya pada sampel jaringan kanker usus besar stadium II dengan miRNA microarray, tetapi data tersebut tidak divalidasi oleh qPCR [ 37 ]. Terakhir, miRNA lain yang termasuk dalam kelompok DEM-1, hsa-miR-4737, menunjukkan profil ekspresi yang sangat berbeda dalam berbagai jenis kanker. Gaballah dkk. menemukan peningkatan ekspresi hsa-miR-4737 dalam vesikel ekstraseluler kecil yang berasal dari garis sel kanker prostat [ 38]. Pada tahun 2021, Stang dkk. melakukan analisis mikroarray miRNA pada sampel darah dari pasien CRC, dan analisis bioinformatika mereka menentukan bahwa ekspresi hsa-miR-4737 menurun pada kelompok pasien mCRC [ 39 ]. Hasil mereka konsisten dengan temuan kami tetapi kurang dikonfirmasi melalui qPCR. Data yang mendukung temuan ini dapat diakses di basis data GEO dengan nomor akses GSE180202.
Hsa-miR-181c-5p, dalam kelompok DEM-2 dan diverifikasi dalam kumpulan data TCGA, ditetapkan sebagai anggota keluarga miR-181 dan memainkan peran penekan tumor dalam berbagai jenis kanker. Slattery dan koleganya menemukan bahwa ekspresi hsa-miR-181c-5p berkurang secara signifikan dalam sampel jaringan adenokarsinoma kolon dibandingkan dengan jaringan kolon normal ( p < 0,001) [ 40 ]. Abd ElAziz et al. menemukan bahwa ekspresi hsa-miR-181c-5p meningkat pada karsinoma hepatoseluler in vitro dan in vivo dan menginduksi karsinogenesis. Meskipun demikian, hsa-miR-181c telah terbukti memiliki ekspresi yang berkurang pada neuroblastoma metastatik, kanker payudara, glioblastoma, dan kanker lambung dan berfungsi sebagai penekan tumor [ 41 ]. MiRNA lainnya, hsa-miR-497-5p, yang bertentangan dengan dataset microarray dan TCGA kami, memainkan peran penting dalam menekan pertumbuhan sel CRC dengan menghambat Insulin Receptor Substrate 1 ( IRS1 ) [ 42 ]. melaporkan bahwa hsa-miR-497 memiliki peran penting dalam menghambat ekspresi Insulin-like Growth Factor 1 Receptor ( IGF1-R ) dan aktivasi PI3K/Akt, sehingga menekan proliferasi, kelangsungan hidup, dan invasi pada sel kanker usus besar manusia [ 43 ]. hsa-miR-769-5p termasuk dalam kelompok DEM-2 dan diverifikasi oleh dataset TCGA, yang menunjukkan peran ganda dalam berbagai jenis kanker. Sebuah penelitian menunjukkan bahwa ekspresi hsa-miR-769-5p meningkat pada karsinoma hepatoseluler dan ekspresi tinggi ini dikaitkan dengan prognosis yang buruk. Selain itu, hsa-miR-769-5p ditemukan untuk meningkatkan pertumbuhan dan metastasis sel karsinoma hepatoseluler [ 44 ]. Selain itu, ekspresi hsa-miR-769 berkurang dalam jaringan CRC, dan tingkat ekspresi berkorelasi negatif dengan prognosis CRC [ 45 ]. Selain itu, hsa-miR-520e, hsa-miR-4754, dan hsa-miR-5691 miRNA dalam kelompok DEM-2 tidak diverifikasi dalam data TCGA COAD dan READ. Meskipun demikian, jumlah penelitian tentang mekanisme regulasi hsa-miR-520e, hsa-miR-4754, dan hsa-miR-5691 dalam kanker terbatas dan memerlukan penyelidikan lebih lanjut. Lv et al. menemukan bahwa hsa-miR-520e menekan pertumbuhan dan invasi sel CRC dengan menekan Astrocyte Elevated Gene 1 ( AEG-1 ) [ 46 ]. Ekspresi hsa-miR-520e dilaporkan meningkat pada jaringan kanker kolon dengan qPCR [ 47 ]. Slattery et al. menemukan bahwa ekspresi hsa-miR-4754 berkurang secara signifikan pada adenoma kolon dibandingkan dengan jaringan kolon normal ( p < 0,001) [ 40 ]. Selain itu, Yang et al. menunjukkan bahwa hsa-miR-4754 dapat digunakan sebagai biomarker diagnostik dalam stadium patologis adenokarsinoma paru-paru [ 48]. Dalam analisis komparatif pustaka sekuens RNA, Watahiki et al. mengidentifikasi hsa-miR-5691 sebagai gen yang menunjukkan ekspresi diferensial signifikan dalam sampel pasien kanker prostat non-metastatik [ 49 ]. Terakhir, Lai et al. melaporkan bahwa gen ini mungkin merupakan DEM potensial untuk kekambuhan kanker payudara [ 50 ].
Analisis bioinformatika kami mengungkapkan GPD2 sebagai target prediksi umum dari tiga miRNA yang diatur turun (hsa-miR-199a-5p, hsa-miR-326, dan hsa-miR-500b-5p) yang divalidasi dalam analisis qPCR (Tabel S7 ). Meskipun kami belum menganalisis ekspresi GPD2 dalam sampel kami, ekspresi berlebih GPD2 dalam jaringan tumor yang diperiksa dalam data TCGA mendukung temuan kami (Gambar 2 ). Kami berencana untuk mengonfirmasi hal ini dalam pekerjaan kami di masa mendatang. GPD2 adalah enzim mitokondria yang memainkan peran penting dalam metabolisme sel kanker dan keseimbangan redoks [ 51 ]. Studi menunjukkan bahwa ekspresi berlebih GPD2 meningkatkan pertumbuhan tumor dan menekan ferroptosis [ 52 ]. Penelitian terbaru menyoroti potensi inhibitor GPD2 sebagai pendekatan terapeutik untuk kanker, dan menggunakan strategi berbasis miRNA dapat menghasilkan hasil yang menjanjikan yang memerlukan penyelidikan lebih lanjut [ 53 ].
Selain itu, Ribosomal Protein S6 Kinase A3 ( RPS6KA3 ) adalah target umum yang diprediksi dari empat miRNA dalam kelompok DEM-2 (hsa-miR-181c-5p, hsa-miR-497-5p, hsa-miR-520e, hsa-miR-5691). Cai et al. melaporkan bahwa ekspresi RPS6KA6 berkurang pada CRC dan bahwa perubahan ini terkait dengan fitur klinis-patologis dan OS [ 54 ]. Kami biasanya mengharapkan miRNA dan gen targetnya menunjukkan pola ekspresi yang berlawanan. Namun, dalam beberapa kasus, mereka dapat menjalankan fungsinya dalam kompleks, yang mengarah ke perubahan serupa dalam arah ekspresi untuk gen targetnya [ 55 ]. Situasi ini dapat relevan untuk mengatur RPS6KA3 oleh regulator miRNA yang diusulkan, yang memerlukan penyelidikan lebih lanjut dalam studi validasi di masa mendatang.
AKT3 dan PLAG1 adalah gen prioritas lain yang diprediksi menjadi target dari setidaknya tiga DEM yang mengalami disregulasi dalam DEM-2. AKT3 berfungsi sebagai onkogen, dan ekspresi berlebihan AKT3 menyebabkan penurunan regulasi p53 , p21 , dan p27 , dan peningkatan regulasi Cyclin D1, Bcl2, dan XIAP [ 56 ]. PLAG1 , yang termasuk dalam keluarga faktor transkripsi zinc finger PLAG, adalah onkogen yang terkait dengan berbagai jenis kanker [ 57 ]. Selain itu, PLAG1 adalah satu-satunya gen yang ditemukan signifikan secara statistik dalam stadium patologis dan analisis OS. Lebih jauh, lncRNA yang ditargetkan oleh jumlah miRNA tertinggi ( n = 4) adalah SNHG16 . Wang et al. mengamati bahwa SNHG12 meningkatkan pertumbuhan sel dan menghambat apoptosis sel dalam sel CRC, yang menunjukkan peran biomarkernya yang berharga untuk CRC [ 58 ].
Studi ini memiliki beberapa keterbatasan. Pertama, validasi DEM yang tersisa dan relevansi fungsionalnya dalam CRC memerlukan investigasi komprehensif lebih lanjut. Kedua, karena metode AdnaTest mendeteksi CTC hanya berdasarkan tiga penanda mRNA spesifik kolon ( CEA , EGFR , EpCAM ), CTC dengan profil yang berbeda untuk heterogenitas CTC tidak dapat dideteksi. Ketiga, penelitian ini tidak menyertakan kelompok pasien nmCRC, yang dapat menjadi area penelitian masa depan yang menjanjikan. Menilai profil ekspresi miRNA kandidat pada pasien nmCRC yang dikelompokkan berdasarkan status CTC akan memberikan wawasan berharga tentang potensi biomarker mereka dalam metastasis. Terakhir, profil ekspresi DEM yang diidentifikasi tidak dianalisis dalam jenis sampel tertentu (seperti serum, plasma, dan jaringan). Menurut analisis statistik dan bioinformatika, miRNA yang terkait dengan status CTC diidentifikasi sebagai kandidat untuk penelitian lebih lanjut kami. Studi validasi skala besar, analisis fungsional, dan studi lebih lanjut harus menyelidiki hasil studi secara komprehensif.
5 Kesimpulan
Sebagai kesimpulan, hasil studi kami menyoroti potensi manfaat miRNA yang beredar sebagai metode pelengkap untuk mengidentifikasi status CTC pada mCRC. Setelah divalidasi lebih lanjut dan dibedakan secara fungsional, temuan ini menjanjikan untuk menilai risiko metastasis secara akurat pada pasien CRC, mengarahkan pasien ke perawatan yang tepat berdasarkan status risiko mereka, dan mengembangkan aplikasi pengobatan translasi baru untuk mCRC.
Kontribusi Penulis
Berkcan Doğan: konseptualisasi; perolehan dana; investigasi; metodologi; visualisasi; penulisan – persiapan draf asli. Dilek Pirim: konseptualisasi; perolehan dana; investigasi; metodologi; administrasi proyek; penulisan – tinjauan dan penyuntingan. Özgen Işık: konseptualisasi; investigasi; sumber daya; penulisan – tinjauan dan penyuntingan. Türkkan Evrensel: konseptualisasi; investigasi; sumber daya; penulisan – tinjauan dan penyuntingan.
Ucapan Terima Kasih
Penelitian ini didukung oleh Unit Proyek Penelitian Ilmiah Universitas Bursa Uludag dan Dewan Penelitian Ilmiah dan Teknologi Turki ( TÜBİTAK ) dengan Nomor Hibah 323S056. Penulis ingin mengucapkan terima kasih kepada TÜBİTAK atas dukungannya. Kami juga berterima kasih kepada anggota lab kami Fatih Atilla Bağcı atas kontribusinya dalam melakukan eksperimen qPCR.
Pernyataan Etika
Penelitian ini dilakukan sesuai dengan prinsip-prinsip Deklarasi Helsinki. Persetujuan diberikan oleh Komite Etik Universitas Bursa Uludag (2011-KAEK-26/117).
Konflik Kepentingan
Penulis menyatakan tidak ada konflik kepentingan.
